
科目: 来源: 题型:
【题目】下列溶液:①pH=0的盐酸,②0.5mol·L-1的盐酸溶液,③0.1mol·L-1的氯化铵溶液,④0.1mol·L-1的氢氧化钠溶液,⑤0.1mol·L-1的氟化钠溶液,由水电离的H+浓度由大到小的顺序正确的是
A. ①②③④⑤B. ③⑤④②①C. ①②③⑤④D. ⑤③④①②
查看答案和解析>>
科目: 来源: 题型:
【题目】人造地球卫星用到的一种高能电池--银锌蓄电池,其电池的电极反应式为:2Zn+2OH--2e-===2ZnO+H2↑,Ag2O+H2O+2e === 2Ag+2OH- 。据此判断锌是( )
A.负极,并被氧化B.正极,并被还原
C.负极,并被还原D.正极,并被氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应A+a B(g)![]() C(g)+2 D(g)(a为化学计量数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图所示。下列说法正确的是
C(g)+2 D(g)(a为化学计量数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图所示。下列说法正确的是

A. T2< T1,P2< P1
B. 增加B的物质的量,B的转化率一定增大
C. 若a=2,则A为固态或液态物质
D. 该反应的正反应为吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】t ℃,体积固定的密闭容器中,发生反应A(g)+3B(g)![]() 2C(g),开始充入1 mol A和3 mol B,达平衡后再充入2 mol C,则平衡
2C(g),开始充入1 mol A和3 mol B,达平衡后再充入2 mol C,则平衡
A. 正向移动 B. 逆向移动
C. 不移动 D. 再次达新平衡时,C的体积分数减小
查看答案和解析>>
科目: 来源: 题型:
【题目】右图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述不正确的是

A. 加入催化剂, 该化学反应的活化能和反应热都改变
B. b曲线是加入催化剂时的能量变化曲线
C. 该反应的热化学方程式为:N2(g) + 3H2(g) ![]() 2NH3(g) ΔH = -92kJ·mol-1
2NH3(g) ΔH = -92kJ·mol-1
D. 在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 =2Q1
查看答案和解析>>
科目: 来源: 题型:
【题目】在相同的A、B密闭容器中分别充入2 mol SO2和1 mol O2,使它们在一定温度下反应,并达新平衡:2SO2+O2![]() 2SO3(g)。若A容器保持体积不变,B容器保持压强不变。当A中SO2的转化率为25%时,B中SO2的转化率为
2SO3(g)。若A容器保持体积不变,B容器保持压强不变。当A中SO2的转化率为25%时,B中SO2的转化率为
A. 25%B. 大于25%
C. 小于25%D. 无法判断
查看答案和解析>>
科目: 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热ΔH=-3677 kJ/mol(P被氧化为P4O10),下列有关P4S3的说法不正确的是()

A. 分子中每个原子最外层均达到8电子稳定结构
B. P4S3中硫元素为-2价,磷元素为+3价
C. 一个P4S3分子中含有三个非极性共价键
D. 热化学方程式为:P4S3(s)+8O2(g)=P4O10(s)+3SO2(g) ΔH=-3677 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在500℃时隔绝空气加热完全分解,回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和_________。
(2)为检验分解产物的成分,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
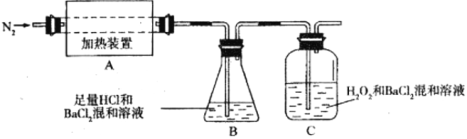
①为验证A中残留物是否含有FeO,需要选用的试剂有_________。
A.KSCN溶液 B.稀硫酸 C.浓盐酸 D.KMnO4溶液
②装置B中BaCl2溶液的作用是为了检验分解产物中是否有_________气体生成,若含有该气体,观察到的现象为___________________。
③若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则b_________a(填“大于”、“小于”或“等于”)
④实验中,观察到C中有白色沉淀生成,则C中发生反应的离子方程式为________________。
(3)为测定某固体样品中(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的含量,某实验小组做了如下实验:MnO4-+Fe2++H+=Mn2++Fe3++H2O(方程式未配平)
测定步骤:
步骤一:准确称量20.00g硫酸亚铁铵晶体,配制成100mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,用0.1000mol·L-1KMnO4溶液滴定至终点,重复两次,平均消耗KMnO4溶液16.00mL。
①步骤二达到滴定终点的标志为________________________;
②产品中(NH4)2Fe(SO4)2·6H2O的质量分数为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com