
科目: 来源: 题型:
【题目】醇的官能团名称是______,结构简式为______;羧酸的官能团名称是______,结构简式为_______。二者在一定条件下发生反应的类型是______,写出乙酸和乙醇反应的化学方程式___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H2SO3+I2+H2O == H2SO4+2HI,将0.1mol Cl2通入100mL含等物质的量的HI与H2SO3的混合溶液中,有一半的HI被氧化,则下列说法正确的是
A. 物质的还原性:HI>H2SO3>HCl
B. H2SO3的物质的量浓度为0.6 mol·L-1
C. 若再通入0.05mol Cl2,恰好能将HI和H2SO3完全氧化
D. 通入0.1mol Cl2发生反应的离子方程式为:5Cl2+4H2SO3+2I-+4H2O == 4SO42-+I2+10Cl-+16H+
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知:CH4(g)+4NO2( g)=4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ·mol-l;CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) △H=-1160 kJ·mol-1,该条件下CH4(g)还原NO2(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式:__________。
(2)已知在448 ℃时,反应H2(g)+I2(g) ![]() 2HI(g)的平衡常数K1为49,则该温度下反应反应
2HI(g)的平衡常数K1为49,则该温度下反应反应![]() H2(g)+
H2(g)+![]() I2(g)
I2(g) ![]() HI(g)的平衡常数K3为___________________________。
HI(g)的平衡常数K3为___________________________。
(3)在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①)该反应的化学平衡常数表达式为K=________。
②该反应为________(填“吸热”或“放热”)反应。
③能判断该反应达到化学平衡状态的依据是________。
A.容器中压强不变 B.混合气体中c(CO)不变 C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
④某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________ ℃。
⑤在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol·L-1,c(H2)为1.5 mol·L-1,c(CO)为1 mol·L-1,c(H2O)为3 mol·L-1,则下一时刻,反应将________(填“正向”或“逆向”)进行。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某溶液中只存在OH-、H+、CH3COO-、Na+四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Na+)>c(CH3COO-)>c(OH-)>c(H+)②c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
③c(CH3COO-)=c(Na+)>c(H+)=c(OH-)④c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
(1)若溶液中只溶解了一种溶质,则该溶质是________,上述四种离子浓度的大小顺序为________(填编号)。
(2)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好反应,则混合前两溶液的物质的量浓度大小关系为c(NaOH)________c(CH3COOH)(填“大于”“小于”或“等于”,下同).
(3)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好是中性,则混合前两溶液的物质的量浓度大小关系为c(NaOH)________c(CH3COOH)(填“大于”“小于”或“等于”),混合后溶液中的各离子浓度的大小关系为_______________________。
(4)25℃时,现有浓度均为0.10 mol·L-1的2种溶液:① 醋酸、② 氢氧化钠。下列说法正确的是______(填字母)。
a.①中有CH3COO-发生水解,促进水的电离
b.②中由水电离出的c(H+)=1.0×10-13 mol·L-1
c.①和②等体积混合后:c(OH-)=c(H+)+c(CH3COOH)
d. ①和②混合后,所得溶液呈中性:c(Na+)>c(CH3COO-)
查看答案和解析>>
科目: 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50 s的平均速率为v(PCl3)=0.0032mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积固定的密闭容器中充入一定量的X、Y两种气体,一定条件下发生反应并达到平衡:3X(g) + Y(g)![]() 2Z(g) △H<0。若测得平衡时X的转化率为37.5 %,Y的转化率是X的2/3,则下列叙述正确的是
2Z(g) △H<0。若测得平衡时X的转化率为37.5 %,Y的转化率是X的2/3,则下列叙述正确的是
A. 若以X表示的反应速率为0.2 mol/(L·s),则以Z表示的反应速率为0.3 mol/(L·s)
B. 充入氦气增大容器内的压强,Y的转化率提高
C. 升高温度,平衡向正反应方向移动
D. 起始时刻n(X) : n(Y)= 2 : 1
查看答案和解析>>
科目: 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A. 用惰性电极电解NaH2PO2溶液,其阳极反应式为:2H2O-4e-=O2↑+4H+
B. H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C. 将H3PO2溶液加入到酸性重铬酸钾溶液中,H3PO2的还原产物可能为H3PO4
D. H3PO2溶于水的电离方程式为H3PO2![]() H++ H2PO2-
H++ H2PO2-
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中,哪项是淀粉、纤维素和糖原的共同特征 ( )
A. 都是细胞内储存能量的物质 B. 都含有C、H、O、N 4种元素
C. 其组成单体都是葡萄糖 D. 都是还原糖
查看答案和解析>>
科目: 来源: 题型:
【题目】可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g) ![]() CH4(g)+2O2(g) ΔH=+802KJ/mol,下图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线。下列说法正确的是
CH4(g)+2O2(g) ΔH=+802KJ/mol,下图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线。下列说法正确的是
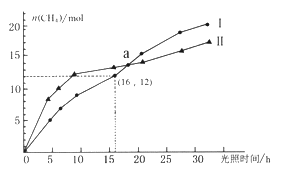
A. 0-15h内,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好
B. 反应开始后的30h内,第Ⅰ种催化剂的作用下,反应吸收的热量多
C. a点时,CO2的转化率相等
D. 0-16h内,v(O2)=1.5mol/(L·h)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com