
科目: 来源: 题型:
【题目】铝及其合金在生活、生产中有广泛应用。
(1)最新研究表明:氢氧化铝溶于氢氧化钠溶液中生成Na[Al(OH)4]。则氢氧化铝在水中发生酸式电离的电离方程式为________________________________。
(2)目前,国内对真空碳热还原-氯化法冶炼铝的研究较多,利用该方法冶炼金属铝,既节能又环保。
已知:①Al2O3(s)+AlCl3(g)+3C(s)=====3AlCl(g)+3CO(g) △H1
②3AlCl(g)====2Al(l)+AlCl3(g) △H2
③Al(l)====Al(s) △H3
则Al2O3(s)+3C(s)====2Al(s)+3CO(g) △H4=___________(用含△H1、△H2、△H3的代数式表示)。
(3)已知:Al4C3是真空碳热还原-氯化法冶炼铝的中间产物,它与水反应生成气体Y,Y是含氢量最大的烃。向2L恒容密闭容器中充入2mol Y和2mol水蒸气,一定条件下发生反应a Y(g)+bH2O(g) ![]() c CO(g)+dH2(g) △H。测得Y的平衡转化率α(Y)与温度、压强的关系如图所示。
c CO(g)+dH2(g) △H。测得Y的平衡转化率α(Y)与温度、压强的关系如图所示。
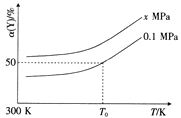
①上述反应的△H_______0(填“>”“<”或“=”)。
②图象中,x_________0.1(填“>”“<”或“=”)。
③在T0K、0.1MPa时,上述反应的平衡常数K=____________。
④提高上述反应的反应速率的措施有_______________________________ (任填二项)。
⑤从上述反应体系中分离出H2(还含有少量CO)作为合成氨的原料气,为避免CO使催化剂中毒,原料气在通入合成塔之前需与适量NH3混合,并用[Cu(NH3)2]Ac溶液吸收CO,反应原理为[Cu(NH3)2]Ac(aq)+CO(g)+NH3(g) ![]() [Cu(NH3)3]Ac·CO(aq) △H<0。若从温度、压强两方面考虑,用[Cu(NH3)2]Ac溶液吸收CO的适宜条件是________________________。
[Cu(NH3)3]Ac·CO(aq) △H<0。若从温度、压强两方面考虑,用[Cu(NH3)2]Ac溶液吸收CO的适宜条件是________________________。
(4)我国首创的海水电池以铝板为负极,以接触空气的铁铂合金网为正极,以弱碱性的海水为电解质溶液,电池总反应为4Al+3O2+6H2O===4Al(OH)3。试写出海水电池的正极反应式:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将2 mol SO2和2 mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g) ![]() 2SO3(g),平衡时,SO3为n mol,相同温度下,分别按下列配比在相同容积的密闭容器中放入起始物质,平衡时,SO3的物质的量大于n mol的是( )
2SO3(g),平衡时,SO3为n mol,相同温度下,分别按下列配比在相同容积的密闭容器中放入起始物质,平衡时,SO3的物质的量大于n mol的是( )
A. 2 mol SO2和1 mol O2B. 4 mol SO2和1 mol O2
C. 2 mol SO2、1 mol O2和2 mol SO3D. 2 mol SO3
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下按如图安装好实验装置,在锥形瓶内盛6.5 g锌粒(颗粒大小基本相同),通过分液漏斗加入40 mL 2.5 mol·L-1的硫酸溶液,将产生的H2收集在一个注射器中,用时10 s时恰好收集到气体的体积为50 mL(若折合成0 ℃、101 kPa条件下的H2体积为44.8 mL),在该温度下,下列说法不正确的是( )

A. 可以通过测定锌粒减少质量来测定反应速率
B. 忽略锥形瓶内溶液体积的变化,用H+来表示10 s内该反应的速率为0.01 mol·L-1·s-1
C. 忽略锥形瓶内溶液体积的变化,用Zn2+来表示10 s内该反应速率为0.01 mol·L-1·s-1
D. 用H2来表示10 s内该反应的速率为0. 000 2 mol·s-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中,正确的是
A. 使用催化剂是为了加快反应速率,提高原料的利用率
B. 燃烧一定都是放热反应
C. 燃烧必须要有氧气参与反应
D. 电解水和氢气在氧气中燃烧是可逆反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在 2A(g) + B(g) 3C(g) + 4D(g)反应中,下面表示的反应速率最快的是
A. v (A)=0.5mol/(Ls) B. v (B)=1.8 mol/(Lmin)
C. v (C)=0.8mol/(Ls) D. v (D)=1.0 mol/(Ls)
查看答案和解析>>
科目: 来源: 题型:
【题目】Cu2SO3·CuSO3·2H2O是一种深红色固体(以下用M表示)。某学习小组拟测定胆矾样品的纯度,并以其为原料制备M。
已知:①M不溶于水和乙醇,100℃时发生分解反应;
②M可由胆矾和SO2为原料制备,反应原理为3Cu2++6H2O+3SO2![]() Cu2SO3·CuSO3·2H2O↓+8H++SO42-。
Cu2SO3·CuSO3·2H2O↓+8H++SO42-。
I.测定胆矾样品的纯度。
(1)取w g胆矾样品溶于蒸馏水配制成250mL溶液,从中取25.00mL于锥形瓶中,加入指示剂,用c mol·L-1EDTA(简写成Na4Y)标准溶液滴定至终点(滴定原理:Cu2++Y4-====CuY2-),测得消耗了V mL EDTA标准溶液。则该胆矾样品的纯度为____________%(用含c、V、w的代数式表示)。如果滴定管装液前没有用EDTA标准溶液润洗,测得的结果会_________ (填“偏高”“偏低”或“无影响”)。
Ⅱ.制备M。实验装置如下图所示:

(2)实验室用70%硫酸与亚硫酸钠粉末在常温下制备SO2。上图A处的气体发生装置可从下图装置中选择,最合适的是________(填字母)。

(3)装置D中的试剂是____________。装置B中水浴加热的优点是____________________。
(4)实验完毕冷却至室温后,从锥形瓶中分离产品的操作包括:__________、水洗、乙醇洗、常温干燥,得产品Cu2SO3·CuSO3·2H2O。检验产品已水洗完全的操作是_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,体积不变的密闭容器中有可逆反应A(g)+ B(g) ![]() 2C(g)+D(s),可以判断反应达到平衡是( )
2C(g)+D(s),可以判断反应达到平衡是( )
A. 单位时间内反应nmol B同时生成2nmol C
B. 容器内气体的物质的量不再变化
C. A的生成速率与B的生成速率相等
D. 容器内气体的密度不再变化
查看答案和解析>>
科目: 来源: 题型:
【题目】《本草纲目》中的“石碱”条目下写道:“采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面。”下列说法错误的是
A. “石碱”中含有离子键 B. “石碱”中含有极性共价键
C. “石碱”是离子化合物 D. “石碱”中含有非极性共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列措施能明显增大原反应的化学反应速率的是( )
A.Na与水反应时增大水的用量
B.将稀H2SO4改为98%的浓H2SO4与Zn反应制取H2
C.恒温、恒容条件下,在工业合成氨反应中,增加氢气的量
D.在H2SO4与NaOH两溶液反应时,增大压强
查看答案和解析>>
科目: 来源: 题型:
【题目】五种短周期主族元素的部分信息如下表所示:
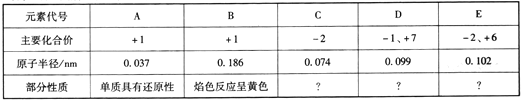
(1)E在元素周期表中的位置是____________________。
(2)在BDC溶液中滴加酚酞溶液,溶液先变红后褪色,原因是__________________(用离子方程式表示)。
(3)25℃时,pH均为10的BCA溶液和B2E溶液中,水电离出的c(OH-)之比为____________。
(4)下列事实中,能说明D的非金属性比E强的是________ (填字母)。
a.D的简单氢化物比E的稳定 b.AD的酸性比A2E的强
c.D的单质的沸点低于E的单质 d.D2与A2E能发生置换反应
(5)500℃时,向容积为1L的恒容密闭容器中充入2mol EC3气体,在催化剂作用下发生反应,经过10min恰好达到平衡,测得平衡浓度c(C2)=0.75mol·L-1。
①反应从开始到平衡时的平均反应速率v(EC2)=____________。
②EC3的平衡转化率为____________。
③其他条件不变,再向容器中充入少量EC3气体,则EC3的平衡转化率会________ (填“增大”“减小”或“不变”)。
(6)在B2E2C3溶液中滴加BAEC4溶液,会析出黄色沉淀并逸出刺激性气体,反应的离子方程式为____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com