
科目: 来源: 题型:
【题目】已知N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1。则下列热化学方程式中正确的是
A. ![]() N2H4(g)+
N2H4(g)+![]() O2(g)=
O2(g)=![]() N2(g)+H2O(l) ΔH=-267 kJ·mol-1
N2(g)+H2O(l) ΔH=-267 kJ·mol-1
B. ![]() N2H4(g)+
N2H4(g)+![]() O2(g) =
O2(g) = ![]() N2(g)+H2O(g) ΔH=+267 kJ·mol-1
N2(g)+H2O(g) ΔH=+267 kJ·mol-1
C. 2N2H4(g)+2O2(g)=2N2(g)+4H2O(g) ΔH=-1068 kJ·mol-1
D. N2(g)+2H2O(l) = N2H4(g)+O2(g) ΔH=+534 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1 mol时,下列说法不正确的是

A. 溶液的质量变化:甲减小,乙增大
B. 溶液pH变化:甲减小,乙增大
C. 相同条件下产生气体的体积:V甲=V乙
D. 电极反应式:甲中阴极:Cu2++2e-==Cu,乙中负极:Mg-2e-==Mg2+
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味的气体放出,符合这一情况的是
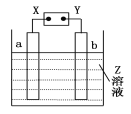
a极板 | b极板 | X电极 | Z | |
A | 锌 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列反应中,HNO3既表现出氧化性,又表现出酸性的是
A. 3Cu+8HNO3(稀) =3Cu(NO3)2+2NO↑+4H2O↑
B. CuO+2HNO3=Cu(NO3)2+H2O
C. 4HNO3(浓) ![]() 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
D. H2S+2HNO3(浓) ![]() S↓+2NO2+2H2O
S↓+2NO2+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位。请回答下列问题:

(1)图中X是________;Ⅰ在小麦种子中主要是指__________。
(2)在病毒中,携带遗传信息的物质是________________(填序号)。
(3)图中A、B分别代表何种元素?A:______,B:______。
(4)导致地球上生物多种多样的直接原因是[ ] _________(填序号和名称)结构的多样性。
(5)物质Ⅱ在人体细胞中的主要载体是________,该分子中______________决定了物质Ⅱ的多样性。
查看答案和解析>>
科目: 来源: 题型:
【题目】表示细胞四种有机物的组成,依据主要功能,分析回答:
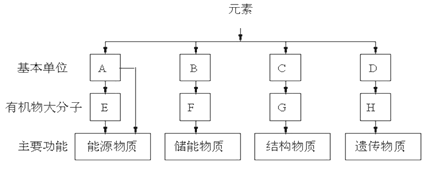
(1)A是指______;E在动物中是指_________,植物中主要是指_________。
(2)F是指_____,它是由B(脂肪酸和甘油)形成的;除此之外,脂质还包括_____和_____。
(3)C是指________;通式是__________,C形成G过程的反应叫_________。
(4)D是指_________,D形成____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】叠氮化钠(NaN3)是一种无色晶体,易溶于水,微溶于乙醇,不溶于乙醚,广泛应用于汽车安全气囊。某硝酸工厂拟通过下列方法处理尾气并制备叠氮化钠。

(1)NO和NO2混合气体与NaOH溶液反应可以合成NaNO2,写出该反应的化学方程式___,生成1mol NaNO2时转移电子______mol
(2)已知NaN3阳离子与阴离子个数比为1:1,则NaN3中所含的化学键为______和______,1mol该阴离子中所含的电子总数为______mol
(3)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3![]() K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56 L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56 L。
①该反应中的氧化剂为______还原剂为______(填化学式)
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克______?(写出计算过程,保留一位小数,不考虑固体的体积)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组欲设计使用如下装置探究:铜和一定量的浓硝酸反应是否有一氧化氮产生。(假设气体体积均为标准状况,导气管中气体体积忽略不计,不考虑浓硝酸的挥发,且忽略反应中的溶液体积变化)

试回答下列问题:
(1)铜粉的作用是___________________;将铜粉分散在是石棉绒中的原因_____________。
(2)在铜和浓硝酸反应前,关闭k3,打开k1、k2 ,挤压打气球,经A、B、C反应后,进入D中的气体是_____(填化学式)。
(3)关闭k1、k2,打开k3,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。则D中一定发生反应的离子方程式为:____________;
(4)E装置中发生反应的化学方程式为_____________________________。
(5)从E装置所得溶液中取出25.00mL,用0.1000 mol/L的NaOH溶液进行中和,当恰好呈中性时消耗NaOH溶液18.00mL,则E中所得硝酸的物质的量浓度为_________mol/L,若实验测得F装置所收集到的气体体积为139.00 mL,则气体的成分为_________(填化学式),则铜和一定量的浓硝酸反应有______ mL NO生成。
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子的最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且元素Y的基态原子核外电子p电子比s电子多5个。
(1)Z的基态原子的核外电子排布式为_____________。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯()裂化生成苯和丙烯。
①1 mol丙烯分子中含有σ键与π键数目之比为_____________。
②苯分子中碳原子的杂化轨道类型为_____________。
③Z的一种氧化物ZO5中,Z的化合价为+6价,则其中过氧键的数目为_________个。

(3)W、X、Y三种元素的电负性由小到大的顺序为_______(请用元素符号回答)。
(4)ZY3的熔点为1 152 ℃,其在熔融状态下能够导电,据此可判断ZY3晶体属于_________(填晶体类型)。
(5)ZX2晶体的晶胞结构如图所示,每个Z原子周围最近的X原子数目为________。若该化合物的相对分子质量为M,晶胞边长为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为_____________g/cm3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com