
科目: 来源: 题型:
【题目】
PBAT(聚己二酸/对苯二甲酸丁酯)可被微生物几乎完全降解,成为包装、医疗和农用薄膜等领域的新兴材料,可由聚合物PBA和PBT共聚制得,一种合成路线如下:
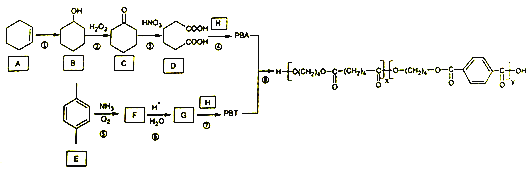
已知: ![]()
回答下列问题:
(1)B的化学名称为_________,C所含官能团的名称为_________。
(2)H的结构简式为__________________。
(3)②、④的反应类型分别为__________________、__________________。
(4)⑤的化学方程式为___________________________。
(5)写出所有的与D互为同分异构体且满足以下条件的结构简式_________。
①能与 NaHCO3溶液反应; ②能发生银镜反应
③能发生水解反应 ④核磁共振氢谱四组峰,峰面积比为1:6:2:1
(6)设计由丙烯为起始原料制备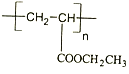 的单体的合成路线_________(其它试剂任选)。
的单体的合成路线_________(其它试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳、氮、铜形成的单质及它们形成的化合物有重要研究和应用价值,回答下列问题:
(1)邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结简式如图所示。
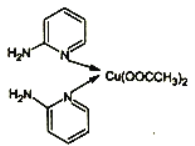
①基态Cu原子的价电子排布式为_________,在元素周期表中铜位于_________区(填“s”“p”“d”或“ds”)。
②C、N、O三种元素的第一电离能由大到小的顺序为_________。
③邻氨基吡啶的铜配合物中,Cu2+的配位数是_________,N原子的杂化类型为_________。
(2)C60是富勒烯族分子中稳定性最高的一种,N60是未来的火箭燃料,二者结构相似。
①有关C60和N60的说法中正确的是_________。
A.C60和N60均属于分子晶体 B.N60的稳定性强于N2
C.C60中碳原子是sp3杂化 D.C60易溶于CS2、苯
②近年来,科学家合成了一种具有“二重结构”的球形分子,它是把足球形分子C60容纳在足球形分子Si60中,则该分子中含有的化学键类型为___________ (填“极性键”“非极性键”)。
(3)原子坐标参数和晶胞参数是晶胞的两个基本参数。
①图中原子坐标参数分别为:A(0,0,0),B(1/2,1/2,0),C(1/2,0,1/2),则D的原子坐标参数为_________。

②图为铜的晶胞,铜原子半径为Rnm,NA是阿伏加德罗常数的值,则铜晶体的密度为_________g·cm-3(用含R、NA的式子表示)

查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.1gH2和4gO2反应放出71.45kJ热量,则氢气的燃烧热为142.9 kJmol﹣1
B.在稀溶液中,H+(aq)+OH﹣(aq)═H2O(1)△H=﹣57.3 kJmol﹣1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量大于57.3kJ
C.HCl和NaOH反应的中和热△H=﹣57.3 kJmol﹣1,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJmol﹣1
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热
查看答案和解析>>
科目: 来源: 题型:
【题目】用如图所示装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中各项所列对应关系均正确的一组是
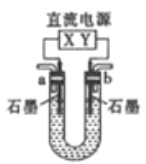
选项 | X极 | 实验前U形管中液体 | 通电后现象及结论 |
A | 正极 | Na2SO4溶液 | U形管两端滴入酚酞后,a管中呈红色 |
B | 正极 | AgNO3溶液 | b管中电极反应式是4OH--4e-=O2↑+2H2O |
C | 负极 | CuCl2溶液 | b管中有气体逸出 |
D | 负极 | NaOH溶液 | 溶液PH降低 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】质量分数为90%的硫酸溶液和质量分数为10%的硫酸溶液等体积混合后溶质的质量分数
A. 大于50%
B. 等于50%
C. 小于50%
D. 不能做上述估计
查看答案和解析>>
科目: 来源: 题型:
【题目】石油化工生产中,利用裂解反应可以获得重要化工原料乙烯、丙烯。一定条件下,正丁烷裂解的主反应如下:
反应I C4H10(g)![]() CH4(g)+CH3CH-CH3(g) △H1;
CH4(g)+CH3CH-CH3(g) △H1;
反应Ⅱ C4H10(g)![]() C2H6(g)+CH2=CH2(g) △H2;
C2H6(g)+CH2=CH2(g) △H2;
回答下列问题:
(1)正丁烷、乙烷和乙烯的燃烧热分别为Q1kJ·mol-1、Q2kJ·mol-1、Q3kJ·mol-1,反应Ⅱ的△H2=______________。
(2)一定温度下,向容积为5L的密闭容器中通入正丁烷,反应时间(t)与容器内气体总压强(p)数据如下:
t/min | 0 | a | 2a | 3a | 4a |
p/MPa | 5 | 7.2 | 8.4 | 8.8 | 8.8 |
①该温度下,正丁烷的平衡转化率a=__________;反应速率可以用单位时间内分压的变化表示,即v=![]() ,前2a min内正丁烷的平均反应速率
,前2a min内正丁烷的平均反应速率![]() =__________MPa·min-1。
=__________MPa·min-1。
②若平衡时甲烷、乙烯的体积分数分别为![]() 、
、![]() ,则该温度下反应I的压力平衡常数Kp=_________MPa(用平衡分压代替平衡浓度计算,分压一总压×物质的量分数,保留三位有效数字)。
,则该温度下反应I的压力平衡常数Kp=_________MPa(用平衡分压代替平衡浓度计算,分压一总压×物质的量分数,保留三位有效数字)。
③若反应在恒温、恒压条件进行,平衡后反应容器的体积_________8.8L(填“>”“<”或“=”)。
④实际生产中发现高于640K后,乙烯和丙烯的产率随温度升高增加幅度减小,可能的原因是__________(任写1条)。
(3)一种丁烷燃料电池工作原理如图所示。
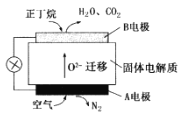
①A电极上发生的是反应_________(填“氧化“或“还原”)。
②写出B电极的电极反应式:______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】中和热的测定是高中化学中重要的定量实验。取50mL、0.55mol/L的NaOH溶液与50mL、0.25mol/L的H2SO4溶液置于如图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从如图所示实验装置看,其中尚缺少的一种玻璃用品是_____________,除此之外,装置的一个明显错误是___________________________________________________。

(2)NaOH溶液稍过量的原因是_______________________________________________。
(3)若改用60mL、0.25mol/L的H2SO4溶液和50mL、0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量_____________(填“相等”或“不相等”),若实验操作均正确,则所求中和热_______________(填“相等”或“不相等”)。
(4)倒入NaOH溶液的正确操作是__________
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次性迅速倒入
(5)实验数据如下表:
温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
①近似认为0.55mol/L NaOH溶液和0.25mol/L H2SO4溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃),则中和热△H=__________(取小数点后一位)。
②上述实验的结果与57.3kJ/mol有偏差,产生偏差的原因可能是____________。
A.实验装置保温、隔热效果差
B.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
C.做实验的当天室温较高
D.量取H2SO4时仰视读数
查看答案和解析>>
科目: 来源: 题型:
【题目】钛白粉(TiO2)广泛应用于涂料、化妆品、食品以及医药等行业。利用黑钛矿石[主要成分为(Mg0.5Fe0.5)Ti2O5,含有少量Al2Ca(SiO4)2]制备TiO2,工艺流程如下。已知: TiOSO4易溶于水,在热水中易水解生成H2TiO3,回答下列问题:
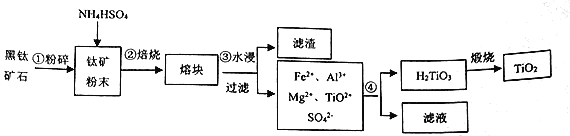
(1)(Mg0.5Fe0.5)Ti2O5中钛元素的化合价为_________,实验“焙烧”所需的容器名称是_________,“滤渣”的主要成分是__________________(填化学式)。
(2)制取H2TiO3的化学方程式为__________________。
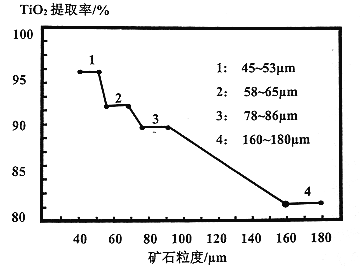
(3)矿石粒度对TiO2的提取率影响如图,原因是____________。
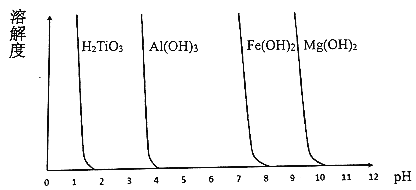
(4)相关的金属难溶化合物在不同pH下的溶解度(s,mol·L-1)如图所示,步骤④应该控制的pH范围是_________(填标号)
A.1~2 B.2~3 C.5~6 D.10~11
(5)常用硫酸铁铵[NH4Fe(SO4)2]滴定法测定钛白粉的纯度,其步骤为:用足量酸溶解ag二氧化钛样品,用铝粉做还原剂,过滤、洗涤,将滤液定容为100mL,取20.00mL,以NH4SCN作指示剂,用标准硫酸铁铵溶液滴定至终点,反应原理为: Ti3++Fe3+=Ti4++Fe2+
①滴定终点的现象为_____________。
②滴定终点时消耗bmol· L-1 NH4Fe(SO4)2溶液VmL,则TiO2纯度为_________。 (写表达式)
查看答案和解析>>
科目: 来源: 题型:
【题目】葡萄糖酸亚铁((C6H11O7)2Fe)是常用的补铁剂,易溶于水,几乎不溶于乙醇。用下图装置制备FeCO3,并利用FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。回答下列问题:

(1)a的名称为_________。
(2)打开a中K1、K3,关闭K2,一段时间后,关闭K3,打开K2。在_________(填仪器标号)中制得碳酸亚铁。实验过程中产生的H2作用有_________、____________。(写2条)
(3)将制得的碳酸亚铁浊液过滤、洗涤。如过滤时间过长会发现产品部分变为红褐色。用化学方程式说明原因____________。
(4)将葡萄糖酸与碳酸亚铁混合,加入乙醇、过滤、洗涤、干燥。加入乙醇的目的是_________________。
(5)用 NaHCO3溶液代替Na2CO3溶液制备碳酸亚铁,同时有气体产生,离子方程式为______________,此法产品纯度更高,原因是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com