
科目: 来源: 题型:
【题目】下列是三种有机物的结构简式,下列说法正确的是( )
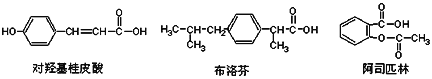
A. 三种有机物都能发生水解反应
B. 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
C. 三种物质中,其中有两种互为同分异构体
D. 三种物质在一定条件下,均可以被氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是 ( )

A. 正极反应中有CO2生成
B. 微生物促进了反应中电子的转移
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】K、Ka、KW分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是( )
A. 在500℃、20 MPa条件下,在5 L密闭容器中进行合成氨的反应,使用催化剂后K增大
B. 室温下Ka(HCN) < Ka(CH3COOH),说明CH3COOH电离产生的c(H+)一定比HCN电离产生的c(H+)大
C. 25℃时,pH均为4的盐酸和NH4I溶液中KW不相等
D. 2SO2+O2![]() 2SO3达平衡后,改变某一条件时K不变,SO2的转化率可能增大、减小或不变
2SO3达平衡后,改变某一条件时K不变,SO2的转化率可能增大、减小或不变
查看答案和解析>>
科目: 来源: 题型:
【题目】萜类化合物广泛分布于植物、昆虫及微生物体内,是多种香料和药物的主要成分。I是一种萜类化合物,它的合成路线如下:


回答下列问题:
(1)按官能团分类,A的类别是______。
(2)A→C的反应类型是______。
(3)C→D、E→F的化学方程式分别是______、______。
(4)写出下列物质的结构简式:B______、H______。
(5)F→G的反应中,乙酸酐的作用______。
(6)十九世纪末O.Wallach发现并提出了“异戊二烯法则”,即自然界中存在的萜类化合物均可以看作是异戊二烯的聚合体或衍生物,为表彰他对萜类化合物的开创性研究,1910年被授予诺贝尔化学奖。请以CH3CH2OH、CH3MgI、CH3CH2MgBr为有机原料,结合题目所给信息,选用必要的无机试剂,补全异戊二烯(![]() )的合成路线____________________。
)的合成路线____________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】Na2S2O4俗称保险粉,常用做纺织工业的漂白剂、脱色剂等。某科研小组制备并探究其性质。
资料:Na2S2O4易溶于水,具有极强的还原性,易被空气氧化,在碱性介质中稳定。
Ⅰ.制备Na2S2O4(加热等辅助仪器略去)

(1)仪器①的名称是______。
(2)B装置用于制备Na2S2O4。第一步反应:Zn+2SO2 ![]() ZnS2O4;第二步,加入NaOH溶液,于28~35℃下反应生成Na2S2O4,该步反应的化学方程式为______。
ZnS2O4;第二步,加入NaOH溶液,于28~35℃下反应生成Na2S2O4,该步反应的化学方程式为______。
(3)B装置反应前,先进行的实验操作是______。
(4)反应后除去B中的沉淀,在滤液中加入一定量的NaCl固体搅拌,有Na2S2O4晶体析出。加入NaCl固体的作用是______。
Ⅱ.探究Na2S2O4的性质
(5)隔绝空气加热Na2S2O4固体完全分解得到固体产物Na2SO3、Na2S2O3和SO2,但科研小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是______。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液、KMnO4溶液)
(6)制备纳米级银粉:用NaOH溶液溶解Na2S2O4,加入一定量的AgNO3溶液,生成纳米级的银粉。在制备银粉的反应中,氧化剂和还原剂的物质的量之比为2︰1,且生成的含硫物质只有一种,写出该反应的离子方程式______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积为1 L的密闭容器中(体积不变)充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) 测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
CH3OH(g)+H2O(g) 测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
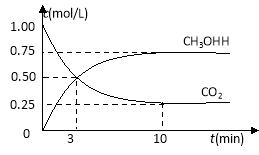
A.3min前v正>v逆,3min后v正<v逆
B.进行到3分钟时,正反应速率和逆反应速率相等
C.10分钟后容器中各物质浓度不再改变
D.达到平衡后,升高温度,正反应速率增大、逆反应速率减小
查看答案和解析>>
科目: 来源: 题型:
【题目】小明化验单上“葡萄糖”一项结果为4.94×10-3mol·L-1。这里的“4.94×10-3mol·L-1”表示葡萄糖的( )
A.体积B.物质的量
C.摩尔质量D.物质的量浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】氮氧化物的存在会破坏地球环境,人们一直在积极探索改善大气质量的有效措施。已知:N2(g)+O2(g)![]() 2NO(g) △H=+181.5 kJ·mol-1
2NO(g) △H=+181.5 kJ·mol-1
(1)写出NO2转化为HNO3的化学方程式______。
(2)氮氧化物是形成臭氧层空洞、光化学烟雾、______(列举一种)等大气污染现象的物质之一。北京市为防治大气污染,采取的措施有______(写两点即可)。
(3)NOx在平流层使O3浓度减少,形成臭氧层空洞,其中一种反应机理可用下图表示,写出其总反应的化学方程式______。

(4)某科研小组尝试利用固体表面催化工艺进行NO的分解。若用![]() 、
、![]() 、
、![]() 和
和![]() 分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如下图所示。从吸附到解吸的过程中,能量状态最低的是______(填字母序号)。
分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如下图所示。从吸附到解吸的过程中,能量状态最低的是______(填字母序号)。

(5)温度为T1时,在容积为1L的恒容密闭容器中充入0.6mol的NO2,达平衡时c(O2)=0.2mol/L,仅发生反应:2NO2(g)![]() 2NO(g)+O2 (g)(△H>0)。实验测得:v正=v (NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO) c(O2),k正、k逆为速率常数,仅受温度影响。当温度改变为T2时,若k正=k逆,则T1______T2(填“>”或“<”),得出该结论的理由是______。
2NO(g)+O2 (g)(△H>0)。实验测得:v正=v (NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO) c(O2),k正、k逆为速率常数,仅受温度影响。当温度改变为T2时,若k正=k逆,则T1______T2(填“>”或“<”),得出该结论的理由是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁铵(NH4)2Fe(SO4)26H2O又称莫尔盐,是浅绿色晶体。用硫铁矿(主要含FeS2、SiO2等)制备莫尔盐的流程如下:

已知:FeS2与H2SO4不反应。相应物质的溶解度曲线如下图。
(1)FeS2中S元素的化合价为______。
(2)硫铁矿焙烧的主反应是:4FeS2+11O2![]() 2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有______(写两点即可)。
2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有______(写两点即可)。
(3)加H2SO4酸浸,发生反应的离子方程式为______。
(4)“还原”时,Fe3+可通过反应Ⅰ、Ⅱ被FeS2还原。反应Ⅰ为:FeS2 +14Fe3+ +8H2O===15Fe2++ 2SO42—+16H+反应Ⅱ的离子方程式为:______。
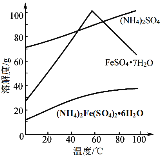
(5)得到莫尔盐晶体的操作是:蒸发浓缩、结晶、过滤、洗涤。结晶、过滤时选择的适宜温度为60℃,解释选择该温度的原因______。
(6)为证明所得莫尔盐晶体中含有Fe2+和NH4+,实验方法是取其少量溶液于一支试管中,______,证明含有Fe2+和NH4+。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com