
科目: 来源: 题型:
【题目】如图是某研究性学习小组设计的对一种废旧合金各成分(含有Cu、Fe、Si三种成分)进行分离、回收再利用的工业流程,通过该流程能得到常用的单质、聚铁(碱式硫酸铁的聚合物)、铁红(Fe2O3)和绿矾(FeSO4·7H2O)。
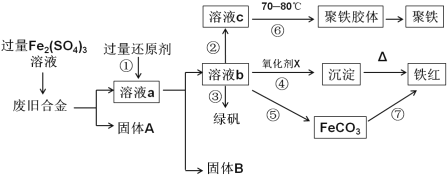
(1)①中过量的还原剂应是____________________。
(2) 向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为_______________________。
(3)②中加入H2O2,并调节pH值得到溶液c,在⑥中,将溶液c控制到70-80℃的目的是________。
(4)在③中,蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有_________________________。
(5)在④中的氧化剂X是________________________。
(6)在⑤中,向溶液b加入了NH4HCO3溶液,得到FeCO3沉淀,写出离子反应方程式 ______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮氧化物(NOx)、CO2和SO2等气体会造成环境问题。对燃煤废气进行化学方法处理,可实现绿色环保、节能减排、废物利用等目的。
(1)已知氢气与甲醇的燃烧热分别为285.8kJ·mol-1、726.5 kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为___________________________________
(2)已知在一定温度下将6molCO2和8mol H2充入容器为2L的密闭容器中发生如下反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H2=-49.0 kJ·mol-1,则
①该反应自发进行的条件是 _______________(填“低温”“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是 _____________(填字母)
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的物质的量之比保持不变
c.CO2和H2的转化率相等 d.3v正(H2)=v逆(CH3OH)
e.1mol CO2生成的同时有3mol H—H键断裂
③H2的物质的量随时间变化曲线如图实线所示,仅改变某一条件再进行实验,测得H2物质的量随时间变化曲线如图虚线所示。与实线相比,虚线改变的条件可能是__________________

(3)如图是某甲醇燃料电池工作的示意图。质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1H2SO4溶液。电极a上发生的电极反应式为 _____________________,当电池中有1mol e-发生转移时左右两侧溶液的质量之差为____g(假设反应物耗尽,忽略气体的溶解)。

查看答案和解析>>
科目: 来源: 题型:
【题目】为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如下:

请回答:
(1)仪器a的名称是_____________。
(2)装置B中冰水的作用是_________。
(3)该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸钠的质量分数偏高的是______。
A.样品分解不完全
B.装置B、C之间缺少CO2的干燥装置
C.产生CO2气体的速率太快,没有被碱石灰完全吸收
D.反应完全后停止加热,通入过量的空气
查看答案和解析>>
科目: 来源: 题型:
【题目】分别称取2.39g(NH4)2SO4和NH4Cl固体混合物两份。
(1)将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]:n(NH4Cl)为___________。

(2)另一份固体混合物中NH4+与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=_____(溶液体积变化忽略不计)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作对应的现象不符合事实的是
|
|
|
|
A.少量二氧化硫通入氯化钡溶液中,产生白色沉淀亚硫酸钡 | B.在新制Cu(OH)2悬浊液中加入少量的葡萄糖,加热,产生砖红色沉淀 | C.将少量钠投入到无水乙醇中,钠表面有气泡产生 | D.在盛水的烧杯中加入氯化钠固体,小灯泡会逐渐亮起来 |
A. AB. BC. C...D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A.常温下,浓硫酸不与铜反应,是因为铜被钝化
B.可用铁罐来进行储存、运输冷的浓硫酸
C.SO3具有氧化性,SO2只有还原性
D.SO2、Cl2的漂白原理相同
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组欲探究含硫物质的性质。
(探究一)用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱:

(1)装置连接顺序为_____________(用字母表示),F中反应的离子方程式是_______________
(2)可证明H2SO3的酸性强于HClO的实验现象是_____________________________。
(探究二)
(3)某小组同学为探究SO2的漂白性性质,用下图所示装置进行实验,

观察到如下现象:i中红色褪去;ii中无变化。从实验中可知使品红的水溶液褪色的微粒可能是_________________________________。
(4)该小组同学又对SO2与氯水的反应进行探究。
①用注射器吸入一定量的饱和氯水和SO2,振荡,静置,再吸入少量品红溶液,发现品红溶液不褪色。②改变氯水用量,重复①操作,发现品红溶液红色褪去,你认为②中品红溶液褪色的原因可能是______________, 设计一个实验(说明操作方法、现象及结论)来验证你的假设___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关溶液中离子存在和转化的表达合理的是( )
A.向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-=A2-+H2O
B.标准状况下,将1.12LCO2气体通入1L0.1mol/L的NaAlO2溶液中:CO2+2H2O+AlO2—=Al(OH)3↓+HCO3-
C.由水电离出的c(H+)=1×10-12mol/L的溶液中可能大量存在K+、I-、Mg2+、NO3-
D.向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-=NH3·H2O+Al(OH)3↓+2BaSO4↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com