
科目: 来源: 题型:
【题目】为分析某盐的成分, 做了如下实验:
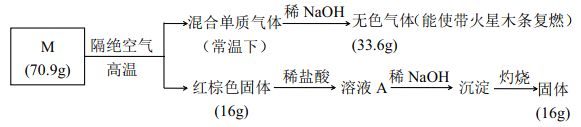
请回答:
(1)盐 M 的化学式是_________;
(2)被 NaOH 吸收的气体的电子式____________;
(3)向溶液 A 中通入H2S 气体, 有淡黄色沉淀产生, 写出反应的离子方程式________ (不考虑空气的影响)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ·mol-1)

下列关于元素R的判断中一定正确的是( )
A. R的最高正价为+3价
B. R元素位于元素周期表中第ⅡA族
C. R元素的原子最外层共有4个电子
D. R元素基态原子的电子排布式为1s22s2
查看答案和解析>>
科目: 来源: 题型:
【题目】钒(23V)是我国的丰产元素,广泛应用于催化及钢铁工业,有“化学面包”、金属“维生素”之称。回答下列问题:
(1)钒原子的核外电子排布式为________________,在元素周期表中的位置为______。
(2)V2O5常用作SO2转化为SO3的催化剂。基态S原子电子占据最高能级的电子云轮廓为________形;气态SO3以单分子形式存在,其分子的立体构型为_______形;固体SO3的三聚体环状结构如图所示,该结构中S—O键长有a、b两类,b的键长大于a的键长的原因为______________。

(3)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子中V的杂化轨道类型为___________;也可得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,则偏钒酸钠的化学式为_____________。

(4)钒的某种氧化物晶胞结构如图所示。该氧化物的化学式为__________,若它的晶胞参数为x nm,则晶胞的密度为__________ g/cm3。

查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C三种常见单质,其有关反应如图所示:

已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血红色。
(1)写出B与水反应的离子方程式_______________________________
(2)A+B→D反应化学方程式___________________________________
(3)F→D的离子方程式是:____________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】甲胺铅碘(CH3NH3PbI3)可用作全固态钙钛矿敏化太阳能电池的敏化剂,由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C—O | H—O | N—H | C—N |
键能/(kJ/mol) | 351.5 | 463 | 393 | 293 |
则该反应的ΔH=________kJ/mol。
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①下列说法不能判断该反应达到化学平衡状态的是________。
A.体系中气体的密度保持不变
B.CO的消耗速率与CH3OH的消耗速率相等
C.体系中CO的转化率和H2的转化率相等
D.体系中CH3OH的体积分数保持不变
②平衡时,M点CH3OH的体积分数为10%,则CO的转化率为________。
③某同学认为上图中Y轴表示温度,你认为他判断的理由是______________________。
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,同时生成I2,写出发生的化学反应方程式__________________。
(4)HI的制备:将0.8molI2(g)和1.2molH2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)![]() 2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:
2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:
时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7/span> |
HI体积分数 | 26% | 42% | 52% | 57% | 60% | 60% | 60% |
①该反应的平衡常数K=_____________。
②反应达到平衡后,在7min时将容器体积压缩为原来的一半,请在图中画出c(HI)随时间变化的曲线_______________。

查看答案和解析>>
科目: 来源: 题型:
【题目】取8.54 g含有Na2CO3、NaOH、Ba(NO3)2的固体混合物溶于足量水中,向反应后的试管中逐滴滴加1.00 mol·L-1的盐酸,加入盐酸的体积和沉淀质量的关系如图所示。

(1)混合物中Ba(NO3)2的物质的量至少为________mol。
(2)X的最大值为_________mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】在外界提供相同电量的条件,Cu2+或Ag+分别按Cu2++2e→Cu或Ag++e-→Ag在电极上放电,若析出铜的质量为1.92g,则析出银的质量为
A.1.62gB.6.48gC.3.24gD.12.96g
查看答案和解析>>
科目: 来源: 题型:
【题目】为了验证干燥的氯气无漂白性,湿润的氯气具有漂白性,某同学设计实验如下图。其中B、C、D、E、F分别盛有饱和食盐水、浓硫酸。干燥红色布条、浓硫酸、湿润红色布条。

请回答:
(1)E中浓硫酸的作用____________。
(2)将F中的湿润布条换成卷曲的细铜丝,并用酒精灯加热,可看到的现象是_____________。
(3)若用装置A制取2.24L(标况)氯气,消耗10mol/L浓盐酸的体积明显大于40mL,造成该结果的可能原因有______________。
A.浓盐酸的挥发 B.随反应进行盐酸浓度下降
C.加热时火力不够猛 D.MnO2固体过量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com