
科目: 来源: 题型:
【题目】2NO2(红棕色)![]() N2O4(无色) ΔH<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是( )
N2O4(无色) ΔH<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是( )

A. b点达到了平衡状态
B. b点对应的时刻改变的条件是将注射器的活塞向外拉
C. d点:v(正)<v(逆)
D. 若在c点将温度降低,其透光率将增大
查看答案和解析>>
科目: 来源: 题型:
【题目】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式
固体B_________________;沉淀D __________________;
溶液E_________________________________________。
(3)写出①、④两个反应的化学方程式
①__________________________________;④_____________________________。
(4)写出②、③两个反应的离子方程式
②_________________________________;③______________________________。
(5)设计实验检验溶液F中所含溶质:______________________________________
(6)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3__________________________Fe2O3____________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定质量的镁铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示。
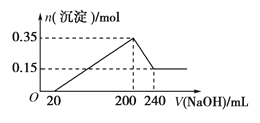
(1)加入NaOH 0~ 20mL 时发生反应离子方程式___________________,
加入NaOH 20~ 200mL 时发生反应离子方程式___________________,
加入NaOH 200~ 240mL 时发生反应离子方程式___________________,
(2)镁和铝的总质量为________g
(3)硫酸的物质的量浓度为___________ mol/L
(4)生成的氢气在标准状况下的体积为__________L
查看答案和解析>>
科目: 来源: 题型:
【题目】CH4-CO2催化重整不仅可以得到合成气CO和H2,还对温室气体的减排具有重要意义。
已知:C(s)+2H2(g)=CH4(g) △H1 K1 C(s)+O2(g) =CO2(g) △H2 K2 ;C(s)+![]() O2(g) =CO(g) △H3 K3;CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H K(其中△H为焓变,K为平衡常数)下列说法正确的是
O2(g) =CO(g) △H3 K3;CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H K(其中△H为焓变,K为平衡常数)下列说法正确的是
A. △H=2△H3-2△H2-△H1
B. K=2K3-K2-K1
C. 若平衡时c(CH4):c(CO2):c(CO):c(H2)=1:1:1:1,则K一定等于1(mol/L)2
D. 减小压强可增大CH4(g)和CO2(g)的平衡转化率
查看答案和解析>>
科目: 来源: 题型:
【题目】海带中含有丰富的碘,有人设计如下步骤:①将海带灼烧成灰,在灰中加水搅拌;②加四氯化碳充分振荡静置;③通入氯气;④过滤;⑤用分液法分离液体混合物。合理操作的先后顺序是
A. ①②③④⑤ B. ①④②③⑤
C. ①②④③⑤ D. ①④③②⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】KIO3可采用电解法制备,装置如图所示。下列叙述正确的是

A. 通电后阴极的电极反应式2H2O+2e-=2OH-+H2↑
B. 电解过程中通过阳离子交换膜的离子主要为K+,其迁移方向是从右到左
C. 电解过程中阳极附近pH增大
D. 当电路中通过1mol电子的电量时,会有0.5mol的KIO3生成
查看答案和解析>>
科目: 来源: 题型:
【题目】香豆素-3-羧酸是香豆素的重要衍生物,工业上利用一种常见石油化工原料A(C2H4)合成香豆素-3-羧酸,合成路线如下(部分产物及条件未列出):

已知:①B能发生银镜反应,D属于常见的高分子,G分子中含有2个六元环
②RCHO+CH2(COOR′)2![]() RCH=C(COOR′)2
RCH=C(COOR′)2
③RCOOR′+R″OH![]() RCOOR″+R′OH
RCOOR″+R′OH
回答下列问题:
(1)B的化学名称是__________。
(2)香豆素-3-羧酸含有的含氧官能团名称是________,反应①—④中属于取代反应的是________。
(3)反应⑦的化学方程式为________________________________________。
(4)下列有关说法正确的是___________ (填标号)。
a.核磁共振仪可测出E有5种类型的氢原子
b.质谱仪可检测F的最大质荷比的值为236
c.G分子中的所有碳原子可能共面
d.化合物W在一定条件下可发生加聚反应
(5)H是 的同系物,相对分子质量比
的同系物,相对分子质量比 多14,其同分异构体分子结构具有下列特征:①含有苯环;②能发生水解反应和银镜反应。满足上述条件的H同分异构体共有___________种(不含立体异构),核磁共振氢谱出现4组峰的结构简式为____________。
多14,其同分异构体分子结构具有下列特征:①含有苯环;②能发生水解反应和银镜反应。满足上述条件的H同分异构体共有___________种(不含立体异构),核磁共振氢谱出现4组峰的结构简式为____________。
(6)观察上述流程,结合相关信息,设计只允许四步由A合成香豆素-3-羧酸的合成路线。请写出合成路线_________。(二元羧酸可部分酯化)
查看答案和解析>>
科目: 来源: 题型:
【题目】随着现代工业的发展,二氧化碳污染的处理成为科学研究的重点,回答下列问题:
I.有人提出利用H2还原CO2使其转化为有机化工的主要原料乙烯。
(1)查阅资料:H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为l41lkJ/mol,lmolH2O(1)转化为H2O(g)需吸收44kJ的热量。则反应6H2(g)+2CO2(g) ![]() C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
△H=___________kJ/mol。
(2)下图是探究不同温度对CO2的转化率和催化剂的催化效率影响的示意图。

①生产中通常选用的温度最好是___________,理由是___________。
②图中表示的化学平衡常数:M___________N(填>、=、<)
③250℃时,在2L密闭容器中分别充入6molH2和2 molCO2,到达平衡时体系中C2H4的体积分数为___________。
Ⅱ.CO在一定条件下,能与H2合成二甲醚:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。
(1)在1L的密闭容器中分别充入2.5molH2与 bmol CO2发生反应,在不同温度下达到平衡状态时测得实验数据如下表:

①到达平衡时若升高温度,则上述平衡___________方向移动(填“正反应”或“逆反应”)。
②转化率:x___________y(填>、=、<)
(2)新型高效的二甲醚燃料电池工作时总反应式:CH3OCH3+3O2=2CO2+3H2O。
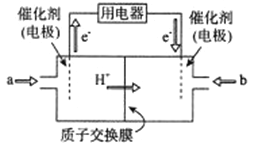
①该电池的负极是___________(填a或b),负极电极反应式为___________;
②利用该电池冶铝,若制得金属铝54g理论上消耗二甲醚___________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】硅及其化合物在材料领域中应用广泛,下列说法正确的是( )
A.制取普通玻璃是以纯碱、黏土、石英砂为主要原料
B.二氧化硅是太阳能转换为电能的常用材料
C.石棉(CaMg3Si4O12)表示为CaO·3MgO·4SiO2
D.水晶、玻璃、陶瓷的主要成分都属于硅酸盐制品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com