
科目: 来源: 题型:
【题目】已知:元素X、Y的核电荷数分别是a和b,它们的离子Xm+和Yn-的核外电子排布相同,则下列关系式中正确的是( )
A.a-m=b+nB.a+m=b-n
C.a-n=b+mD.a+n=b-m
查看答案和解析>>
科目: 来源: 题型:
【题目】MOH强碱溶液和等体积、等浓度的HA弱酸溶液混合后,溶液中有关离子的浓度应满足的关系是( )。
A.c(M+)>c(OH-)>c(A-)>c(H+)B.c(M+)>c(A-)>c(H+)>c(OH-)
C.c(M+)>c(A-)>c(OH-)>c(H+)D.c(M+)>c(H+)>c(A-)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学需用480 mL 0.5 mol·L-1Na2CO3溶液,在实验室进行配制。
(1)该同学用托盘天平应称量________g Na2CO3粉末,使用容量瓶前必须进行的一步操作是______。
(2)下图是该同学配制的一些关键步骤和操作图。
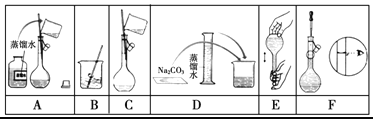
配制过程的先后顺序为(用字母A~F填写)________________。
(3)步骤A通常称为洗涤,如果没有步骤A,则配得溶液的浓度将________(填“偏高”、“偏低”、“不变”);步骤F如果俯视刻度线,配得溶液的浓度将_______(填“偏高”、“偏低”、“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物A(仅含三种元素,摩尔质量为198g·mol-1)具有高效的消毒作用,是一种新型非氮高效消毒剂。为探究化合物A的组成与性质,设计并完成以下实验:取3. 96g化合物A溶于水中,一段时间后全部转化为B(红褐色沉淀)、C(一种碱)和气体单质D(可使带火星的木条复燃),向溶液中加入100mL 0.6mol/L稀硫酸,再加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将沉淀洗涤后充分灼烧,得到红棕色固体粉末1.60g。将所得溶液在一定条件下蒸发可得到一种纯净的不含结晶水的盐。
(1)化合物A所含有的元素:_______________(用元素符号表示)。
(2)化合物A与H2O反应的离子方程式:__________________。
(3)化合物A可由FeCl3和KClO在强碱性条件下制得,其反应的离子方程式:_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(含有质量分数为8%的TeO2、少量Ag、Au)为原料制备单质碲的一种工艺流程如下,(已知TeO2微溶于水,易溶于强酸和强碱),下列有关说法不正确的是
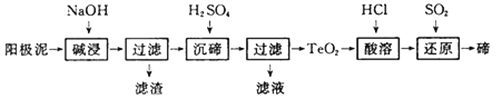
A. 将阳极泥研磨、反应适当加热都有利于提高“碱浸”的速率和效率
B. “碱浸”时发生主要反应的离子方程式为TeO2+2OH-=TeO32-+H2O
C. “沉碲”时为使碲元素沉淀充分,应加入过量的硫酸
D. 若提取过程碲元素的回收率为90%,则处理1kg这种阳极泥最少需通入标准状况下SO2 20.16L
查看答案和解析>>
科目: 来源: 题型:
【题目】含有6.02×1023个H3PO4 中氧原子的物质的量是( )
A. 1.00 mol B. 0.50 mol C. 4mol D. 0.125 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】化学上常见的混合物分离或提纯的基本装置如下:
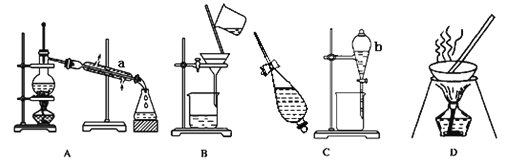
(1)写出仪器名称:a___________,b__________。
(2)从海带提取碘的操作如下,除特殊说明外,请在空白处填上装置中的序号:将干海带进行灼烧,海带灰中含有较多KI,将海带灰溶于水,然后__________得到澄清滤液;向滤液中加入硫酸和H2O2混合溶液,得到棕褐色含有单质碘的水溶液。该反应的离子方程式为:__________________。向碘的水溶液中加入适量CCl4,进行___________操作将上下两层溶液分开。将含有碘的CCl4溶液置于蒸馏烧瓶内进行___________操作,可以粗略从CCl4溶液中分离出碘。
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒温、体积为2 L的密闭容器中加入1 mol CO2和3 mol H2,发生如下的反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。可认定该可逆反应在一定条件下已达到化学平衡状态的是
CH3OH(g)+H2O(g) ΔH<0。可认定该可逆反应在一定条件下已达到化学平衡状态的是
A. 容器中CO2、H2、CH3OH、H2O的物质的量之比为1∶3∶1∶1
B. v正(CO2)=v逆(H2O)
C. 容器内混合气体密度保持不变
D. 3 mol HH键断裂同时断裂3 mol HO键
查看答案和解析>>
科目: 来源: 题型:
【题目】用CH4催化还原NOx可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ΔH=574 kJ·mol1
4NO(g)+CO2(g)+2H2O(g) ΔH=574 kJ·mol1
②CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) ΔH=1 160 kJ·mol1
2N2(g)+CO2(g)+2H2O(g) ΔH=1 160 kJ·mol1
下列说法不正确的是
A. 由反应①可推知:CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(l) ΔH=Q,Q>574 kJ·mol1
4NO(g)+CO2(g)+2H2O(l) ΔH=Q,Q>574 kJ·mol1
B. 等物质的量的甲烷分别参加反应①、②,反应转移的电子数不同
C. 若用标准状况下4.48 L CH4还原NO2至N2,则放出的热量为173.4 kJ
D. 若用标准状况下4.48 L CH4还原NO2至N2,则整个过程中转移的电子总物质的量为1.6 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com