
科目: 来源: 题型:
【题目】对于苯乙烯(![]() )有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
)有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
A. ①②③④⑤ B. ①②⑤⑥ C. ①②④⑤⑥ D. 全部正确
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列物质既能使溴水褪色,又能使酸性KMnO4溶液褪色,并且化学反应原理相同的是( )
A. CH2=CH2B.SO2C.H2D. CH3CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】能正确表示下列反应的离子反应方程式为( )
A. Ba(OH)2溶液中加入少量NaHCO3溶液:HCO3-+Ba2++OH-=BaCO3![]() +H2O
+H2O
B. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:3Ba2++3SO42-+2Al3++6OH-═2BaSO4↓+2Al(OH)3↓
C. NH4HCO3稀溶液与过量的KOH溶液反应:HCO3-+OH-=CO32-+H2O
D. 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化碳的有效回收利用,既能够缓解能源危机,又可减少温室效应的影响,具有解决能源问题及环保问题的双重意义。请回答下列问题:
(1)CO2的电子式为___________。
(2)Zn/ZnO热化学循环还原CO2制CO的原理如下图:
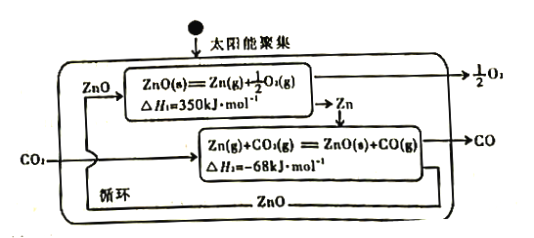
①从循环结果看,能量转化的主要方式是_________________________________。
②反应2CO2(g)=2 CO(g) +O2(g) △H=___________kJ·mol-1。
(3)二甲醚是重要的有机中间体,在一定条件下利用CO2与H2可直接合成二甲醚:
2CO2(g)+6H2(B)![]() CH3OCH3(g)+3H2O(g),当n(H2)/n(CO2)=3时,实验测得CO2的平衡转化率随温度及压强变化如下图所示。
CH3OCH3(g)+3H2O(g),当n(H2)/n(CO2)=3时,实验测得CO2的平衡转化率随温度及压强变化如下图所示。
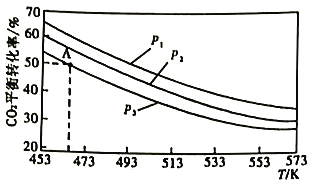
①该反应的△H___________0(填“>”或“<")。
②上图中的压强(p)由大到小的顺序为___________。
③若在1L密闭容器中充入0.2molCO2和0.6molH2,CO2的平衡转化率对应上图中的A点,则在此温度下,该反应的化学平衡常数为___________(保留整数)。
④合成二甲醚过程中往往会生成一氧化碳,合成时选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。硅铝比与产物选择性如下图所示。
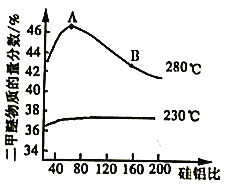
图中A点和B点的化学平衡常数比较:KA___________KB(填“>、=、<")。根据以上两条曲线,写出其中一条变化规律:____________________________________________。
(4)利用电化学原理将H2O和CO2转化为O2和燃料(C3H8O)的实验装置如下图所示。a电极的电极反应式为_________________________________。
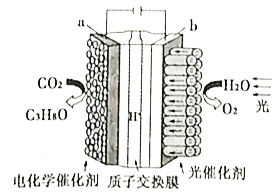 .
.
查看答案和解析>>
科目: 来源: 题型:
【题目】“变废为宝”是化工的重要主题。工业上可用电子工业中刻蚀线路板的酸性废液(主要成分有CuCl2,FeCl2等)制备碱式碳酸铜Cu2(OH)2CO3],其制备过程如下图所示:
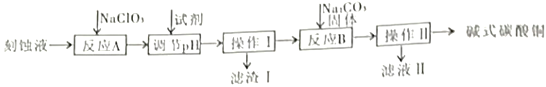
查阅资料得知,一定浓度的Cu2+、Fe2+、Fe3+生成氢氧化物沉淀的pH如下表:
金属离子 | Cu2+ | Fe2+ | Fe3+ |
开始沉淀的pH | 4.2 | 6.5 | 1.4 |
沉淀完全的pH | 6.7 | 9.7 | 3.7 |
(1)电子工业中用FeCl3溶液制作铜制印刷电路板,该反应的离子方程式为___________。
(2)操作I、操作Ⅱ所用的玻璃仪器除烧杯外还需要______________________。
(3)氯酸钠的作用是____________________________________________;反应A中氧化剂与还原剂物质的量之比是___________。
(4)调节pH的范围为___________,可以选择的试剂是___________(填序号)。
A.氨水 B.硫酸铜 C.氧化铜 D.氢氧化铜
(5)已知滤液Ⅱ中含有碳酸氢钠,写出生成碱式碳酸铜的离子方程式:___________。
(6)若废液中CuCl2的含量为13.5%,则1吨废液理论上可提炼碱式碳酸铜________吨。
查看答案和解析>>
科目: 来源: 题型:
【题目】生活中使用的购物袋的材料多为聚乙烯,工农业生产中使用的塑料也是聚乙烯。下列有关说法正确的是( )
A.聚乙烯的单体能够使溴的四氯化碳溶液褪色
B.聚乙烯既可以人工合成,也可以从自然界中获取
C.聚乙烯与乙烯的性质相似
D.用纯净的乙烯合成的聚乙烯是纯净物
查看答案和解析>>
科目: 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)="0.100" mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如右图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是

A. pH=2.5的溶液中:c(H2C2O4)+ c(C2O42-)> c(HC2O4-)
B. c(Na+)="0.100" mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+ c(C2O42-)
C. c(HC2O4-)= c(C2O42-)的溶液中:c(Na+)>0.100 mol·L-1+ c(HC2O4-)
D. pH=7的溶液中:c(Na+)>2c(C2O42-)
查看答案和解析>>
科目: 来源: 题型:
【题目】利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是( )

A. a管发生吸氧腐蚀,b管发生析氢腐蚀
B. 一段时间后,a管液面高于b管液面
C. a处溶液的pH增大,b处溶液的pH减小
D. a、b两处具有相同的电极反应式:Fe-2e-===Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. pH值小于7的雨水称为酸雨B. 工厂将烟囱造高能减小对环境的污染
C. 全球气温变暖是因为SO2的大量排放D. 油电混动车的大量推广可减轻环境的污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com