
科目: 来源: 题型:
【题目】在容积为2L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示200 ℃、100 ℃下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示200 ℃、100 ℃下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
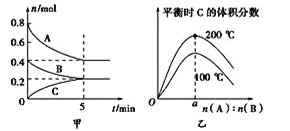
A. 200℃时,反应从开始到平衡的平均速率v(B)=0.04mol·L-1·min-1
B. 若在图甲所示的平衡状态下再向体系中充入He,此时v正> v逆
C. 由图乙可知,反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=1
zC(g)的ΔH<0,且a=1
D. 200℃时,向容器中充入2molA和1molB,达到平衡时A的体积分数小于0.5
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述错误的是( )
A. 17gH2O2所含非极性键数目为0.5NA
B. 标准状况下,H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA
C. n(H2CO3)和n(HCO3-)之和为1mol的NaHCO3溶液中,含有Na+数目为NA
D. 100gCaS和CaSO4的混合物中含有32g硫,则含有的氧原子数为1.75NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子中,因发生氧化还原反应而不能大量共存的是( )
A. K+、H+、Fe2+、NO3-B. Fe3+、Ba2+、SO42-、NO3-
C. Al3+、Na+、SO42-、CO32-D. Fe3+、H+、SO42-、ClO﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是三种有机物的结构简式,下列说法正确的是( )
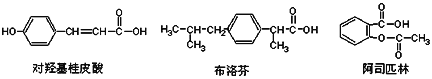
A. 三种有机物都能发生水解反应
B. 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
C. 三种物质中,其中有两种互为同分异构体
D. 三种物质在一定条件下,均可以被氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。请你结合下列有关图示和所学知识回答:
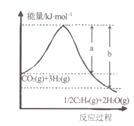
I.用CO2催化加氢可以制取乙烯:CO2(g)+3H2(g)![]() 1/2C2H4(g)+2H2O(g)。
1/2C2H4(g)+2H2O(g)。
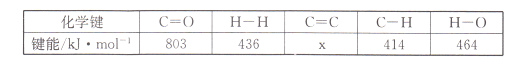
(l)若该反应体系的能量随反应过程变化关系如图所示,则该反应△H =___________(用含a、b的式子表示);又知:相关化学键的键能如下表所示,实验测得上述反应的△H =-152 kJ/mol,则表中的x= ___。
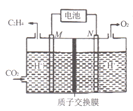
(2)以稀硫酸为电解质溶液,利用太阳能电池将CO2转化为乙烯的工作原理如图所示。则M极上的电极反应式为____。
II.用CO2催化加氢还可以制取二甲醚:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)△H =-122.5kJ/mol,某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
CH3OCH3(g)+3H2O(g)△H =-122.5kJ/mol,某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
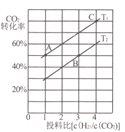
(3)图中T1、T2分别表示反应温度,判断T1、T2大小关系的依据是____;图中A、B、C三点对应的平衡常数分别为KA、KB、Kc,其三者大小的关系是____。
(4)T1温度下,将6molCO2和12molH2充入2L的密闭容器中,经过5min反应达到平衡,则0~5min内的平均反应速率υ(H2)=_______,平衡常数K=__(列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知一定温度下,X(g)+2Y(g)![]() mZ(g);ΔH =-akJ/mol(a>0)现有甲、乙两容积相等且固定的密闭容器,在保持该温度下,向密闭容器甲中通入1molX和2molY,达平衡状态时,放出热量bkJ;向密闭容器乙中通入2molX和4molY,达平衡状态时,放出热量ckJ,且2b < c,则下列各值关系正确的是
mZ(g);ΔH =-akJ/mol(a>0)现有甲、乙两容积相等且固定的密闭容器,在保持该温度下,向密闭容器甲中通入1molX和2molY,达平衡状态时,放出热量bkJ;向密闭容器乙中通入2molX和4molY,达平衡状态时,放出热量ckJ,且2b < c,则下列各值关系正确的是
A. a = b B. 2a < c C. m > 3 D. m < 3
查看答案和解析>>
科目: 来源: 题型:
【题目】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体中原子间通过______________________作用形成面心立方密堆积,其中M原子的配位数____________。
(2)元素Y的含氧酸中,酸性最强的是________________(写化学式),该酸根离子的立体构型为______________________。
(3)M与Y形成的一种化合物的立方晶胞如图所示。
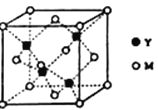
①该化合物的化学式为______________________,已知晶胞参数a=0.542 nm,此晶体的密度为__________________________g·cm–3。(只写出计算式,阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是:_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
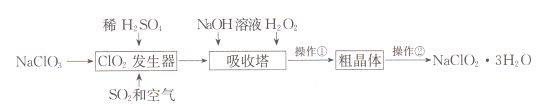
已知:①HC1O2可视为强酸,NaClO2的溶解度随温度升高而增大。②ClO2的沸点为283K,纯ClO2易分解爆炸。回答下列问题:
(1)ClO2发生器中发生反应的离子方程式为____;向其中鼓入空气的作用可能是____。
(2)吸收塔中发生反应的化学方程式为____;为防止生成的NaClO2被继续还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是____(填序号)。
A.Na2O2 B.Na2S C. FeCl2 D.KMnO4
(3)操作①的实验方法依次是_____、_____、过滤;操作②实验方法是_____。
(4)akg NaClO3理论上可制___ kg NaClO2·3H2O。
查看答案和解析>>
科目: 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6molSO2和3molO2,乙容器恒温恒容,充入6molSO3,丙容器恒温恒压,充入6molSO3,充分反应达到平衡,下列说法正确的是
2SO3(g)ΔH<0,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入6molSO2和3molO2,乙容器恒温恒容,充入6molSO3,丙容器恒温恒压,充入6molSO3,充分反应达到平衡,下列说法正确的是
A. 乙中SO3的体积分数大于丙
B. 转化率:α甲(SO2)+α乙(SO3)=1
C. 乙和丙中的SO2的生成速率相同
D. 甲和丙中反应的化学平衡常数相同
查看答案和解析>>
科目: 来源: 题型:
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)![]() 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:

① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1 000℃)>K(810℃) 上述①~④中正确的有( )
A. 4个 B. 3个 C. 2个 D. 1个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com