
科目: 来源: 题型:
【题目】如图1是细胞中化合物含量的扇形图,图2是活细胞中元素含量的柱形图,下列说法不正确的是( )

A. 若图1表示细胞鲜重,则A、B分别是水、蛋白质;图2中a、b、c依次表示碳、氧、氢
B. 若图1表示细胞干重,则A化合物的是蛋白质
C. 若图1表示正常细胞,则A化合物中不含图2中的b
D. 若图1表示完全脱水的细胞,则此时含量最多的元素为图2中的b
查看答案和解析>>
科目: 来源: 题型:
【题目】聚醋酸乙烯酯是黏合剂,应用广泛。下面是该有机物的合成路线:
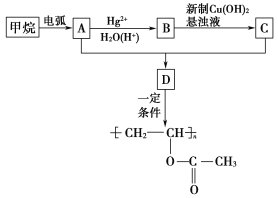
提示:①甲烷在电弧的作用下生成炔烃。
②CH3C≡CH![]() CH3CH2CHO(未配平)。
CH3CH2CHO(未配平)。
请回答下列问题:
(1)甲烷合成A的化学反应中原子利用率为________。
(2)B的结构简式为________。
(3)B生成C的反应中除新制Cu(OH)2悬浊液外还需要的条件是________。
(4)A与C反应生成D的反应类型是________。
(5)写出由D生成 反应的化学方程式:____________________________________________________。
反应的化学方程式:____________________________________________________。
(6)写出能既能溴水褪色又能使紫色石蕊溶液变红的D的同分异构体的结构简式:_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。
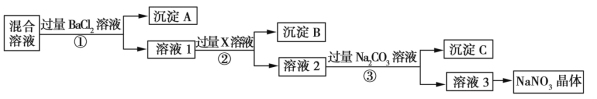
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X___,沉淀A____。
(2)上述实验流程中①②③步均要进行的实验操作是___(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是______________________________。
(4)按此实验方案得到的溶液3中肯定含有______(填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的___(填化学式),之后若要获得NaNO3晶体,需进行的实验操作是____(填操作名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)6.02×1023个氢氧根离子的物质的量是________mol,其摩尔质量为________。
(2)在标准状况下,0.01 mol某气体的质量为0.44 g,则该气体的密度为________g·L1(保留小数点后两位),该气体的相对分子质量为________。
(3)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是________,CO的体积分数是________,CO的质量分数是________,C和O原子个数比是________,混合气体的平均相对分子质量是________,密度是________g·L1。
查看答案和解析>>
科目: 来源: 题型:
【题目】摩尔盐的成分为(NH4)2Fe(SO4)2·6H2O(M=392g·mol-1),常作氧化还原滴定剂。学校购买了一批摩尔盐样品(假设杂质不参与反应),某学习小组拟设计实验方案测定其纯度:
方案1:沉淀法。甲同学准确称量一定质量样品溶于适量的蒸馏水,滴加适量BaCl2溶液至S042-完全沉淀,经过滤、洗涤、干燥,称得BaSO4质量。
(1)检验SO42-是否完全沉淀的操作是____________________________________________。
方案2:滴定法。乙同学准确称取mg摩尔盐样品溶于蒸馏水配制成250mL溶液,量取25.00mL所配制溶液于锥形瓶中,滴加适量的稀硫酸,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液的体积为VmL。
(2)用KMnO4溶液滴定时应选用___(填“酸式”或“碱式”)滴定管,写出滴定反应的离子方程式:_________。
(3)该样品的纯度为_________________________________。
(4)若用待测液润洗锥形瓶,测得结果___________(填“偏高”“偏低”或“无影响”)。
方案3:量气法。丙同学准确称量4.0g样品按下图所示装置进行实验。

(5)①橡胶管L的作用是______________________。
②B中液体可以是___________(填字母)。
a.饱和食盐水 b四氯化碳 c.煤油 d饱和氯化铵溶液
③当A中样品完全反应后,待装置冷却至室温,测得NH3的体积为448mL(已折合成标准状况)。根据上述数据计算,该产品的纯度为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)13 g C2H2(g)完全燃烧生成CO2和H2O(l)时,放出659 kJ的热量,写出表示该物质燃烧热的热化学方程式___________________________。
(2)已知反应:Cl2+2HBr===Br2+2HCl。
Ⅰ.当有0.2 mol HCl生成时放出8.1 kJ的热量。
Ⅱ.其能量变化示意图如图:

则该反应的热化学方程式为_____________________________________。由上述数据判断断开1 mol H—Cl 键与断开 1 mol H—Br键所需能量相差约为________kJ。
(3)已知:①2CO(g)+O2(g) ===2CO2(g) ΔH=-566 kJ·mol-1
②Na2O2(s)+CO2(g) ===Na2CO3(s)+1/2O2(g) ΔH=-226 kJ·mol-1
则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为________。
(4)已知CO 、H2 、CH4 的燃烧热分别为283 kJ·mol-1、286 kJ·mol-1、890 kJ·mol-1。若将a mol CH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,且CO2和水的物质的量相等时,则放出热量(Q)的取值范围是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:P4(g)+6Cl2(g)===4PCl3(g) ΔH=a kJ·mol-1,
P4(g)+10Cl2(g)===4PCl5(g) ΔH=b kJ·mol-1,
又知形成或拆开1 mol化学键放出或吸收的能量称为该化学键的键能。P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ·mol-1,PCl3中P-Cl键的键能为1.2c kJ·mol-1。下列叙述正确的是
A. P-P键的键能大于P-Cl键的键能
B. 可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C. Cl-Cl键的键能为(b-a+5.6c)/4 kJ·mol-1
D. P-P键的键能为(5a-3b+12c)/8 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,充分燃烧一定量的丁烷生成二氧化碳和气态水时放出热量Q kJ(Q>0)。经测定完全吸收生成的CO2需消耗5 mol·L-1的KOH溶液100 mL,恰好生成正盐。则此条件下反应C4H10(g)+13/2O2(g)![]() 4CO2(g)+5H2O(g)的ΔH为( ) kJ·mol-1
4CO2(g)+5H2O(g)的ΔH为( ) kJ·mol-1
A. +8Q B. +16Q C. -8Q D. -16Q
查看答案和解析>>
科目: 来源: 题型:
【题目】I.双氧水(主要成分H2O2)是常见的氧化剂、还原剂。
(1)如下图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式____________。
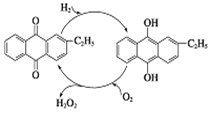
(2)H2O2可看作二元弱酸,写出它在水中第一步电离的方程式______________________________。
II.A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。
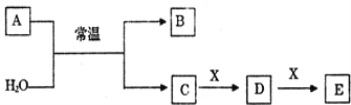
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:__________________________________________________________________________________。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则X可能为______________________(填代号)。
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.Na[Al(OH)4]
(3)若A为淡黄色粉末,则A的电子式为____________________。若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为__________(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为________________________________,E是__________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(2分)N2H4是一种高效清洁的火箭燃料.0.25mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量.则下列热化学方程中正确的是( )
A.![]() N2H4(g)+
N2H4(g)+![]() O2(g)=
O2(g)=![]() N2(g)+H2O(l)△H=+257kJmol﹣1
N2(g)+H2O(l)△H=+257kJmol﹣1
B.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣133.5kJmol﹣1
C.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=+534kJmol﹣1
D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com