
科目: 来源: 题型:
【题目】现有一种泉水,取0.5 L这种泉水作为样品,经测定该样品中含有48.00 mg的Mg2+。
(1)该泉水中Mg2+的物质的量的浓度是________________
(2)为使该泉水样品所含的Mg2+全部沉淀,应加入1mol/L NaOH溶液的体积是______
查看答案和解析>>
科目: 来源: 题型:
【题目】用中和滴定法测定某烧碱样品(含有氯化钠的杂质)的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,样品可放在________称量。配制溶液选用________(填编号字母)
A.小烧杯中 B.洁净纸片上
C.500 mL容量瓶 D.500 mL试剂瓶
(2)为了避免测定过程中样品部分与空气中二氧化碳反应导致结果偏差,滴定时,用0.2000 mol/L的盐酸标准液来滴定待测溶液,可选用________(填编号字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
(3)滴定过程中,眼睛应注视_____________,若用酚酞做指示剂,滴定终点的标志是____________,滴定结果是________(偏大,偏小,不变),理由______________________。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是________mol/L,烧碱样品的纯度是____________。
滴定次数 | 待测溶液体积 (mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
查看答案和解析>>
科目: 来源: 题型:
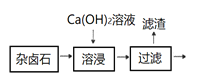
【题目】难溶性杂卤石(K2SO4MgSO42CaSO42H2O)在水中存在如下平衡K2SO4MgSO42CaSO42H2O (s)![]() 2Ca2++2K++ Mg2++4SO42-+2H2O,为能充分利用钾资源,用足量的饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾。工艺流程是:首先需要溶浸与分离,见下图:
2Ca2++2K++ Mg2++4SO42-+2H2O,为能充分利用钾资源,用足量的饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾。工艺流程是:首先需要溶浸与分离,见下图:
(1)不同温度下,K+的浸出浓度与溶浸时间的关系如下图,由图可得,随着温度升高①________________;②______________。

(2)为了提高浸出效率,可采取的措施是:________;过滤用到的玻璃仪器名称是:______。
(3)滤渣主要成分有_________和_________以及未溶杂卤石,用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石、浸出K+的原因: _________________________________。
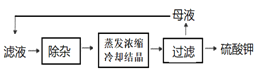
(4) 溶浸与分离过滤后,滤液中的主要杂质离子是______,进一步“除杂”环节见下图。可先加入______溶液,经搅拌等操作后,过滤,再加入_________溶液调滤液pH至中性。
(5)中过滤得到的母液中含有大量的_____(填写化学式),检验其中溶质阴离子的方法是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,利用置换反应X+Y=W+Z,可实现物质之间的转化
(1)若X为Mg,W为C,则Z为_________。
(2)若X为SiO2,W为CO,该反应在工业的用途是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢化锂(LiH)在干燥的空气中能稳定存在,遇水或酸能够引起燃烧。某活动小组准备使用下列装置制备LiH固体。
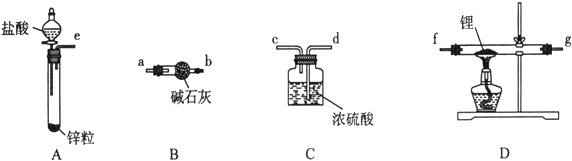
甲同学的实验方案如下:
(1)仪器的组装连接:上述仪器装置按气流从左到右连接顺序为________________,加入药品前首先要进行的实验操作是____________(不必写出具体的操作方法);其中装置B的作用是___________。
(2)添加药品:用镊子从试剂瓶中取出一定量金属锂(固体石蜡密封),然后在甲苯中浸洗数次,该操作的目的是____________________,然后快速把锂放入到石英管中。
(3)通入一段时间氢气后加热石英管,通氢气的作用是___________________________;在加热D处的石英管之前,必须进行的实验操作是__________。
(4)加热一段时间后,停止加热,继续通氢气冷却,然后取出LiH,装入氮封的瓶里,保存于暗处。采取上述操作的目的是为了避免LiH与空气中的水蒸气接触而发生危险,反应方程式为_____________。
(5)准确称量制得的产品0.174g,在一定条件下与足量水反应后,共收集到气体470.4 mL(已换算成标准状况),则产品中LiH与Li的物质的量之比为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)填空
①除去硝酸钾中混有的少量氯化钠,操作步骤为:制成热饱和溶液、_______、过滤;
②分离四氯化碳和水的操作名称为_________;
③除去氢气中氯化氢的操作名称为 ________;
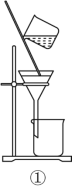
(2)从如图装置中选择
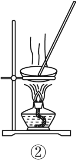
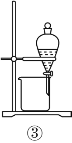
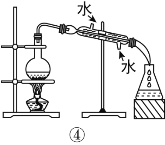
![]()
①除去水中的氯离子,所需装置序号为_______;
②除去铜粉中的锌粉,所需装置序号为 _______。
查看答案和解析>>
科目: 来源: 题型:
【题目】盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关一定物质的量浓度溶液的配制说法中正确的是( )

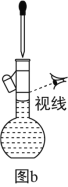
(1)为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用胶头滴管滴加蒸馏水至刻度线
(2)利用图a配制0.10molL-1NaOH 溶液
(3)利用图b配制一定浓度的NaCl溶液
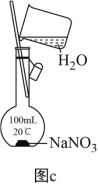
(4)利用图c配制一定物质的量浓度的NaNO3溶液
(5)用容量瓶配制溶液时,若加水超过刻度线,立即用滴管吸出多余液体
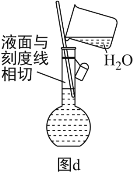
(6)配制溶液的定容操作可以用图d表示
A. (2)(5)B. (1)(4)(6)
C. (1)D. (1)(3)(5)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)K2Cr2O7的水溶液中存在如下平衡:Cr2O72-(aq)+H2O(l)![]() 2CrO42-(aq)+2H+(aq),平衡常数表达式__________,已知:(在水溶液中K2Cr2O7为橙红色,K2CrO4为黄色)往上述溶液中加入足量氢氧化钠,溶液呈________色;向已加入氢氧化钠的溶液中,再加入过量硫酸,溶液呈__________色。
2CrO42-(aq)+2H+(aq),平衡常数表达式__________,已知:(在水溶液中K2Cr2O7为橙红色,K2CrO4为黄色)往上述溶液中加入足量氢氧化钠,溶液呈________色;向已加入氢氧化钠的溶液中,再加入过量硫酸,溶液呈__________色。
(2)在KMnO4与H2C2O4反应中,可通过测定________________来测定该反应的速率;写出酸性条件下KMnO4与H2C2O4(弱酸)反应,产生二氧化碳气体、水和Mn2+的离子反应方程式:__________________;此反应开始反应缓慢,随后反应迅速加快,其原因是______(填字母)。
A.KMnO4溶液中的H+起催化作用
B.生成的CO2逸出,使生成物浓度降低
C.反应中,生成的Mn2+起催化作用
D.在酸性条件下KMnO4的氧化性增强
查看答案和解析>>
科目: 来源: 题型:
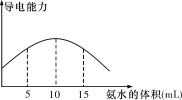
【题目】(1)取20 mL pH=3的CH3COOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度(分子电离的百分数)为______________,加入0~10 mL的氨水导电能力增强的原因_________________________。
(2)将醋酸铵固体溶于水,配成0.1 mol·L-1溶液,已知醋酸的电离平衡常数为Ka,一水合氨的电离平衡常数为Kb,实验发现两者近似相等,请写出醋酸铵水解的离子方程式______________________,水解平衡常数的表达式____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com