
科目: 来源: 题型:
【题目】实脸室取等物质的量的KClO3分别发生下述反应:
反应一:有催化剂存在时,受热分解得到氧气;
反应二:不使用催化剂,加热至743K左右,得到KClO4和KCl。
下列关于①和②的说法正确的是( )
A. 两个反应中都只有一种元素化合价发生改变
B. 两个过程生成KCl的物质的量相同
C. 发生氧化反应的元素相同
D. 发生还原反应的元素相同
查看答案和解析>>
科目: 来源: 题型:
【题目】煤燃烧过程中加入石灰石可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是燃烧过程中产生的CO又会与CaSO4发生化学反应,降低了脱硫效率。发生的两个相关反应的热化学方程式如下:
反应Ⅰ:CaSO4(s)+CO(g)![]() CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1
反应Ⅱ:CaSO4(s)+4CO(g)![]() CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1
CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1
已知:①反应Ⅰ和反应Ⅱ同时发生 ②反应Ⅰ的速率大于反应Ⅱ的速率
下列反应过程能量变化示意图正确的是
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目: 来源: 题型:
【题目】已知分解1molKClO3放出热量38.8kJ,在MnO2下加热,KClO3的分解分为两步:
①2KClO3+4MnO2![]() 2KCl+2Mn2O7 慢
2KCl+2Mn2O7 慢
②2Mn2O7![]() 4MnO2+3O2 快
4MnO2+3O2 快
下列有关说法不正确的是
A. 1molKClO3所具有的总能量高于1molKCl所具有的总能量
B. 1gKClO3 ,1gMnO2,0.1gMn2O7混合加热,充分反应后MnO2质量仍为1g
C. KClO3分解速率快慢主要取决于反应①
D. 将固体二氧化锰碾碎,可加快KClO3的分解速率
查看答案和解析>>
科目: 来源: 题型:
【题目】将4 mol A 气体和2 mol B 气体在2 L的容器中混合并在一定条件下发生反应:2A(g)+B(g) ![]() 2C(g)。若2s末测得C的浓度为 0.6 mol·L-1,现有下列几种说法:
2C(g)。若2s末测得C的浓度为 0.6 mol·L-1,现有下列几种说法:
①2s内,用物质A表示的反应的平均速率为0.6 mol·L-1·s-1;
②2s末,体系中混合气体的压强是起始的0.9倍;
③2 s末,物质A的转化率为30 %;
④2 s末,物质C的体积分数约为22.2%。
⑤2s内,分别用A、B、C表示的反应速率其比值是14:7:6
其中正确的是
A. ①④⑤ B. ②③④ C. ①③④ D. ③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于氧化还原反应的叙述正确的是
A.H2还原CuO的反应只属于还原反应
B.置换反应都是氧化还原反应,所以,3CO+Fe2O3![]() 2Fe+3CO2既是置换反应又是氧化还原反应
2Fe+3CO2既是置换反应又是氧化还原反应
C.3O2![]() 2O3是氧化还原反应
2O3是氧化还原反应
D.复分解反应一定不是氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2CO3(aq)与盐酸反应过程中的能量变化示意图如下,下列选项正确的是
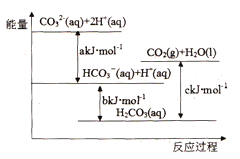
A. H2CO3(aq)=CO2(g)+H2O(l)为放热反应
B. CO32-(aq)+ H+(aq)=HCO3-(aq) △H=akJ/mol
C. HCO3-(aq)+H+(aq)= CO2(g)+H2O(l) △H=(c-b)kJ/mol
D. CO32-(aq)+ 2H+(aq)= CO2(g)+H2O(l) △H=(a+b-c)kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式______,____。
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448 mL气体,则该漂白粉中所含有效成份的质量为_____________(假设漂白粉中的其它成份不与硝酸反应)。
(2)将14 g Na2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶液的体积为400 mL。试计算:原混合物中Na2O的质量为______g,所得溶液的物质的量浓度为______ mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式或叙述正确的是
A. 已知HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-57.3kJ·mol-1
B. 500℃、30 MPa下,N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g)放热46.2 kJ
2NH3(g) ΔH=-92.4 kJ·mol-1将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g)放热46.2 kJ
C. 已知氢气的燃烧热为286 kJ·mol-1,则2H2O(g)===2H2(g)+O2(g) ΔH=+572 kJ·mol-1
D. 甲烷的燃烧热为890.3 kJ·mol-1,则表示甲烷燃烧热的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com