
科目: 来源: 题型:
【题目】(1)发射卫星的火箭推进器中大多使用燃料偏二甲肼,其化学式C2H8N2。试计算:
①偏二甲肼的摩尔质量是________;480 g偏二甲肼的物质的量为________。
②偏二甲肼中碳原子与氮原子的个数之比是________,物质的量之比是________;1 mol偏二甲肼中含有的氢原子数目是________。
(2)据报道,加利福尼亚大学的科研人员发现了世界上最强的酸。这种强酸的化学式是CHB11Cl11。其中11个硼原子和1个碳原子排列成20面体,这是目前化合物中化学性质最为稳定的原子组合。请回答下列问题:
①这种超强酸由________种元素组成。
②用NA表示阿伏加德罗常数的数值,那么1 mol该超强酸中含有的氯原子数目为________,若称取该超强酸1 049 g,则其中含硼原子的数目为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷、石墨、氢气燃烧的反应热:CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1=-890.3kJ/mol
C(石墨)+O2(g)=CO2(g) ΔH2=―393.5kJ/mol
H2(g)+1/2O2(g)=H2O(l) ΔH3=―285.8kJ/mol,
则由石墨生成甲烷的反应热:C(石墨)+2H2(g)=CH4(g) ΔH 4= _________________。
(2)体积相同,pH均等于1的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m________n(填>、<、= )
(3)常温下,某一元酸HA的Ka=2×10-6,则0.5 mol/L该酸溶液的PH =______。
(4)取浓度相等的NaOH和HCl溶液,以3∶2体积比相混和,所得溶液的pH等于12,则原溶液的浓度为_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液态烃,0.1 mol该烃在足量的氧气中完全燃烧,生成0.6 mol CO2和0.3 molH2O;回答下列问题:
(1)A的电子式________,B的结构简式________。
(2)等质量的A、B完全燃烧时消耗O2的物质的量A_______B(填“>”、“<”或“=”)
(3)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:_________________,反应类型:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】由CO2、CO、H2组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2、CO的体积比可为( )
A. 13∶8∶29B. 22∶1∶14
C. 29∶8∶13D. 13∶16∶57
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关表示正确的是( )
A.过氧化钙(CaO2)的电子式:![]()
B.某微粒的结构示意简图为![]() ,则该元素在周期表中位于第三周期、VIA族
,则该元素在周期表中位于第三周期、VIA族
C.H2CO3的电离方程式:H2CO32H++CO32﹣
D.葡萄糖的结构简式:C6H12O6
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液一定呈中性的是
A. pH=7
B. pH=3的盐酸与pH=11的氨水等体积混合后
C. 0.1mol/LNaOH溶液与0.05mol/LH2SO4溶液混合后
D. C(OH-)=![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列数量的各物质所含原子数按由大到小的顺序排列是________。
①0.5 mol氨气
②标准状况下22.4 L氦气
③4 ℃时9 mL水
④0.2 mol磷酸钠(Na3PO4)
(2)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
①该气体的物质的量为________mol。
②该气体所含原子总数为________个。
③该气体在标准状况下的体积为________L。
④该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为________mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。
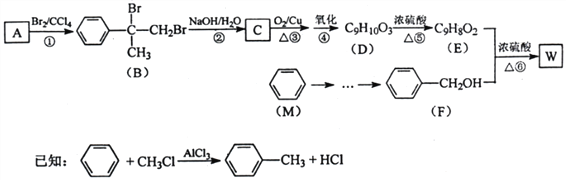
请回答下列问题:
(1)F的化学名称是_______________,①的反应类型是_______________。
(2)B中含有的官能团是_______________(写名称),
(3)D聚合生成高分子化合物的化学方程式为________________。
(4)反应③的化学方程式是___________________。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为_________________。
(6)分子式C9H10O2的有机物,其结构中含有苯环且可以与饱和NaHCO3溶液反应放出气体的同分异构体有__________________种(不考虑立体异构)。
(7)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(无机试剂任选)。____________
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】(15分)氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中 AlN的含量,某实验小组设计了如下两种实验方案。
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图C装置中球形干燥管的作用是 。
(2)完成以下实验步骤:组装好实验装置,首先 ___________ ,再加入实验药品。接下来的实验操作是 ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是 。
(3)若去掉装置B,则导致测定结果 (填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见 。
【方案2】按以下步骤测定样品中A1N的纯度:
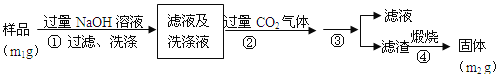
(4)步骤②生成沉淀的离子方程式为___________________。
(5)步骤③的操作是 。A1N的纯度是 (用m1、m2表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com