
科目: 来源: 题型:
【题目】已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系。
(1)若A为金属铝,B为氧化铁,该反应的一种用途是_______________。
(2)若A是一种能使湿润的红色石蕊试纸变蓝的气体,且该反应是工业上制取硝酸的重要反应之一,该反应的化学反应方程式为____________________________。
(3)若A是淡黄色粉末,常用作供氧剂,C为强碱,则该反应的化学反应方程式为_______。
(4)若A、B、D都是有机化合物,其中A、B是家庭厨房中常见调味品的主要成分,且A 的相对分子质量比B大14。
①该反应的化学反应方程式为_____________________。
②某种以B为反应物的新型电池如图所示,该电池的负极的电极反应式为_________。

(5)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl—,该反应的离子方程式为________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】高分子化合物材料PET聚酯和PMMA的合成路线如图:
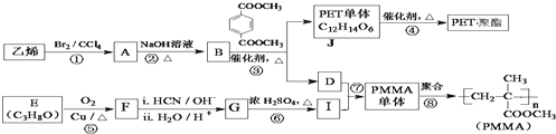
已知:
Ⅰ.RCOOR′+R″![]() OH
OH![]() RCO18OR″+R′OH(R、R′、R″代表烃基)
RCO18OR″+R′OH(R、R′、R″代表烃基)
Ⅱ.![]()
![]()
![]() (R、R′代表烃基)
(R、R′代表烃基)
(1)PMMA单体的化学名称 _________________。
(2)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为________________。反应⑤、⑥的反应类型____________ 、________________。
(3)G的分子式_____________,G中官能团的名称_____________、______________,2分子G可形成环状化合物,写出化学方程式 ____________。
(4)I的某种同分异构体与I具有相同官能团,且为顺式结构,其结构简式是 _____________。
(5)写出与F互为同分异构体且含单官能团的两种有机物的结构简式 ___________________。
(6)写出由PET单体制备PET聚酯并生成B的化学方程式 ______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C的氧化物是导致酸雨的主要物质之一,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子.
(1)写出基态E原子的价电子排布式 .
(2)B、C、D三元素第一电离能由小到大的顺序为(用元素符号表 示) ;A与C形成CA3型分子,分子中C原子的杂化类型为 ,分子的立体结构为 ;C的单质与 BD化合物是等电子体,据等电子体的原理,写出BD化合物的电子式 ; A2D由液态形成晶体时密度 (填增大,不变或减小),分析主要原因(用文字叙述)
(3)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为(用元素符号表示) ;若相邻D原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为 g/cm3(用含a、NA的符号表示).

查看答案和解析>>
科目: 来源: 题型:
【题目】2020年新春之际,出现了罕见的新型冠状病毒肺炎,威胁着人们的身体健康。以下消毒剂可以有效地灭活病毒,走进了百姓的生活中。下列叙述中,不正确的是
A.高锰酸钾(KMnO4)是电解质
B.H2O2分子中所有原子都达到了8电子结构
C.次氯酸钠(NaClO)是离子化合物
D.医用酒精是体积分数为75%的乙醇溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】已知0.5L的NaCl溶液中含有0.5molNa+。下列关于该溶液的说法不正确的是( )
A. 该溶液中溶质的物质的量浓度为1 mol·L-1
B. 该溶液中含有58.5gNaCl
C. 配制1000mL该溶液需用58.5gNaCl
D. 量取100mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1mol
查看答案和解析>>
科目: 来源: 题型:
【题目】100mL0.3mol/LNa2SO4溶液和100mL0.2mol/LAl2(SO4)3溶液混合后,溶液中SO42-的物质的量浓度约为:( )
A. 0.2mol/LB. 0.25mol/LC. 0.45mol/LD. 0.50mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究铜与6molL-1硝酸反应的气态产物中是否含NO2,进行如下实验。
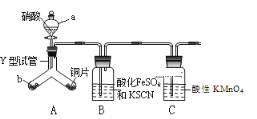
已知:FeSO4+NO ![]() [Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量2+时突显明显棕色。
[Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量2+时突显明显棕色。
(1)实验前需检验装置的气密性,简述操作_____________________________________。
(2)仪器a的名称____________
(3)实验开始时先将Y形试管向盛有块状固体b的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是_________;
(4)证明有NO2的实验现象___________________________________
(5)装置C的作用________,反应离子方程式____________。
(6)测定化学试剂绿矾(FeSO4·7H2O)纯度的方法:称取绿矾3.000g置于锥形瓶中,加入100mL蒸馏水,加入10mLH2SO4和5mLH3PO4,用0.1000molL-1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL。KMnO4溶液盛放在棕色_____式(填“酸”或“碱”)滴定管中,列式计算绿矾的纯度_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知硫酸钠晶体(Na2SO4·10H2O)中钠离子数目3.01×1023,请计算填空:
(1)钠离子的物质的量是_____,硫酸钠晶体的物质的量是______。
(2)所含硫酸根离子的物质的量是______,硫酸根离子的数目是______。
(3)所含结晶水的物质的量是____,所含氧原子的物质的量是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:
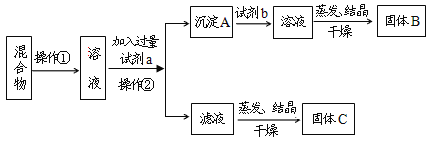
(1)操作①的名称是_____,操作②的名称是____。
(2)试剂a是_____(填化学式,下同),试剂b是____,固体B是_____。
(3)加入试剂a所发生反应的化学方程式为_______________________。加入试剂b所发生反应的化学方程式为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com