
科目: 来源: 题型:
【题目】探究2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O反应速率的影响因素,有关实验数据如下表所示:下列说法不正确的是( )
实验编号 | 温度 | 催化剂用量(g) | 酸性KMnO4溶液 | H2C2O4溶液 | KMnO4溶液褪色平均时间 min | ||
体积(mL) | 浓度mol·L-1 | 体积(mL) | 浓度 mol·L-1 | ||||
1 | 25 | 0.5 | 4 | 0.1 | 8 | 0.2 | 12.7 |
2 | 80 | 0.5 | 4 | 0.1 | 8 | 0.2 | a |
3 | 25 | 0.5 | 4 | 0.01 | 8 | 0.2 | 6.7 |
4 | 25 | 0 | 4 | 0.01 | 8 | 0.2 | b |
A. a<12.7,b>6.7
B. 用KMnO4表示该反应速率,v(实验3)<v(实验1)
C. 用H2C2O4表示该反应速率,v(实验1)约为7.87×10-5 mol·L-1·min-1
D. 可通过比较收集相同体积CO2所消耗的时间来判断反应速率快慢
查看答案和解析>>
科目: 来源: 题型:
【题目】欲测定金属镁的相对原子质量,请利用如图给定的仪器组成一套实验装置(每个仪器只能使用一次,假设气体的体积可看作标准状况下的体积)。

填写下列各项(气流从左到右):
(1)各种仪器连接的先后顺序是___接___、___接___、___接___、_____接___(用小写字母表示)。
(2)连接好仪器后,要进行的操作有以下几步,其先后顺序是____(填序号)。
①待仪器B中的温度恢复至室温时,测得量筒C中水的体积为V0 mL;
②擦掉镁条表面的氧化膜,将其置于天平上称量,得质量为w g,并将其投入试管B中的带孔隔板上;
③检查装置的气密性;
④旋开装置A上分液漏斗的活塞,使其水顺利流下,当镁完全溶解时再关闭这个活塞,这时A中共放入水V1mL。
(3)根据实验数据可算出金属镁的相对原子质量,其数学表达式为____。
(4)若试管B的温度未冷却至室温,就读出量筒C中水的体积,这将会使所测定镁的相对原子质量数据____(填“偏大”“偏小”或“无影响”)。
(5)仔细分析上述实验装置后,经讨论认为结果会有误差,于是又设计了如图所示的实验装置。
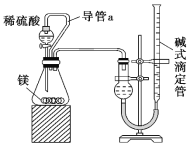
装置中导管a的作用是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在标准状况下①6.72L CH4②3.01×1023个HCl分子③13.6g H2S④0.2mol NH3,体积最大的是____,密最大的是度___,质量最小的是___,氢原子个数最多的是____。(填写序号)
(2)等温等压下,质子数相等的CO、N2两种气体,质量之比为____,体积之比为____,摩尔质量之比____。
(3)某物质在一定条件下加热分解,产物都是气体。分解方程式为:3A=B+3C+2D。测得生成的混合气体的平均相对分子质量为2a,则A的摩尔质量为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳、氮广泛分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途。
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s) + 6C(s) + 2N2(g)![]() Si3N4(s) + 6CO(g) ΔH=-1591.2 kJ/mol则该反应每转移1mol e-,可放出的热量为________
Si3N4(s) + 6CO(g) ΔH=-1591.2 kJ/mol则该反应每转移1mol e-,可放出的热量为________
(2)高温时,用CO还原MgSO4可制备高纯MgO
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是:____________
②由MgO制成的Mg可构成“镁—次氯酸盐”电池,其装置示意图如图,该电池的正极反应式为____________

(3)某研究小组将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g) + H2O(g)![]() CO2(g) + H2(g),得到如下数据:
CO2(g) + H2(g),得到如下数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
CO | H2O | CO | H2 | |||
1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
2 | 900 | 1 | 2 | 0.5 | 0.5 | — |
①实验Ⅰ中,前5min的反应速率v(CO2)=___________
②下列能判断实验Ⅱ已经达到平衡状态的是(填写选项序号)__________
a.容器内CO、H2O、CO2、H2的浓度不再变化
b.容器内压强不再变化
c.混合气体的密度保持不变
d.v正(CO)=v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如下图所示,b点v正_______v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是______________________

查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列各图曲线表征的信息。得出的结论正确的是
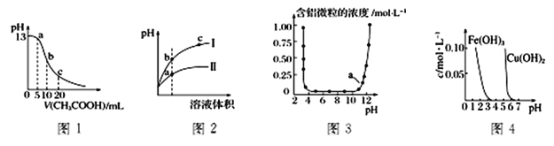
A. 图1表示常温下向体积为10mL0.1 molL-1NaOH溶液中逐滴加入0.1 molL-1CH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-)
B. 图2表示用水稀释pH相同的盐酸和NH4C1溶液时。溶液的pH变化曲线,其中Ⅰ表示盐酸,Ⅱ表示NH4C1溶液,且溶液导电性:b>c>a
C. 图3表示的是Al3+与OH-反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在Al3+
D. 由图4得出若除去Fe2(SO4)3溶液中的Cu2+,可采用向溶液中加入适量Fe2O3,调节溶液的pH 至4左右
查看答案和解析>>
科目: 来源: 题型:
【题目】通常用的漂白粉是次氯酸钙,氯化钙和氢氧化钙所组成的水合复盐,是由Cl2与消石灰制成的。有关反应如下:2Cl2+3Ca(OH)2=Ca(ClO)2·CaCl2·Ca(OH)2·H2O+H2O
(1)漂白粉的有效成分是________________________________________;
(2)漂白粉在潮湿的空气中放置会慢慢失效,有关反应的化学方程式为: _______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法中正确的是( )
①0.5mol O3与11.2L O2所含的分子数一定相等
②标准状况下,28g CO与N2的混合气体的体积约为22.4L
③通常状况下,NA个CO2分子占有的体积为22.4L
④常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
⑤常温下,4.4g CO2和N2O(不反应)混合物中所含有的电数为2.2NA
⑥标准状况下,22.4L SO3含有的分子数为NA
⑧在常温常压下,1mol O2含有的原子数为2NA
A. ①③⑥⑧B. ②④⑤⑧C. ①③⑤⑧D. ②③④⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图:
则下列叙述错误的是( )
A. A气体是NH3,B气体是CO2
B. 把纯碱及第Ⅲ步得到的晶体与某些固体酸性物质(如酒石酸)混合可制得发酵粉
C. 纯碱可广泛地用于玻璃、制皂、造纸、纺织等工业中
D. 第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中进行的反应:N2 + 3H22NH3,下列说法正确的是
A. 降低温度能加快逆反应速率
B. 保持体积不变充入N2,能加快反应速率
C. 达到平衡时,反应速率:v(正) =v(逆)=0
D. 达到平衡时,N2和H2的转化率可能达到100%
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
容器 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是
A.该反应的正方应为放热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com