
科目: 来源: 题型:
【题目】下列属于放热反应的是
A. C + CO2![]() 2CO
2CO
B. CaCO3![]() CaO + CO2↑
CaO + CO2↑
C. 2Al + Fe2O3![]() 2Fe + Al2O3
2Fe + Al2O3
D. Ba(OH)2·8H2O + 2NH4Cl=BaCl2 + 2NH3↑+ 10H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,表中的数字表示一种短周期元素,回答下列问题:

(1)画出③的原子结构示意图:____________________。
(2)③、④、⑦、⑧四种元素所形成的气态氢化物中最稳定的是__________(填化学式)。
(3)①在元素周期表中的位置是____________________________。
(4)⑧、⑨元素的最高价氧化物对应水化物的酸性:____>____(用化学式表示)。_________
(5)由③、⑤和⑩组成的化合物所含化学键类型为__________,电子式为____________。
(6)④、⑤、⑥的原子半径由大到小的顺序是:____>____>____(用元素符号表示)。__________
(7)⑥单质与氢氧化钠溶液反应的化学方程式是__________________________________。
(8)已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为上表中元素组成。
①A的浓溶液与甲能发生如下图所示的反应。
②甲是常见的黑色固体单质,可为生产生活提供热能。
③乙是常见的无色气体单质。
④B是无色有刺激性气味的气体,是主要的大气污染物之一。
⑤常温下,C是一种无色液体。

回答问题:
①写出下列物质的化学式:A_____,E_____,G_____。
②写出下列反应的化学方程式:
C+E→F+乙________________________________。
B+C+乙→A________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成分的存在,请你参与并协助他们完成相关实验。
(1)取少量苹果汁,加入碘水,溶液变蓝,则苹果中含有______________。
(2)取少量苹果汁,加入新制Cu(OH)2并加热,产生红色沉淀,则苹果中含有_____________。
(3)葡萄糖在一定条件下可以得到乙醇。写出乙醇与乙酸反应的化学方程式:_____________。下列物质中可以鉴别乙酸和乙醇的是_________(填字母)。
A.碳酸钠溶液 B.水 C.紫色石蕊试液
查看答案和解析>>
科目: 来源: 题型:
【题目】一种从废甲醇催化剂(含ZnO、CuO及少量Fe2O3、石墨及MnO2等)回收铜并制取活性氧化锌的工艺流程如下:

回答下列问题:
(1)废催化剂“破碎”的目的是________,“酸浸”后“浸渣”的主要成分是________。
(2)“氧化”时Mn2+被氧化的离子方程式为________。
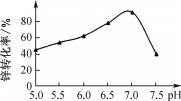
(3)“中和沉淀”时pH对锌转化为碱式碳酸锌的转化率影响如图所示:pH>7时,转化率开始减小的原因是________[用离子方程式说明,已知Zn(OH)2性质与Al(OH)3类似]。
(4)“过滤3、洗涤”时,能证明已洗涤干净的操作方法是________;所得滤液中主要溶质是________。
(5)测定“粗铜粉”中铜的质量分数的实验步骤如下:
Ⅰ.准确称取粗铜粉mg,加入足量HCl和H2O2使其完全溶解(Cu+H2O2+2H+=Cu2++2H2O,Zn及Fe也同时溶解)。
Ⅱ.将溶液煮沸1~2min,除去过量的H2O2。
Ⅲ.依次滴入适量氨水、醋酸及NH4HF2溶液,以排除Fe3+的干扰。然后加入稍过量的KI(2Cu2++4I-=2CuI↓+I2),再加入1mL淀粉溶液作指示剂,用cmol·L-1Na2S2O3标准溶液滴定至蓝色消失(I2+2S2O32-=2I-+S4O62-)且半分钟内不变色,共消耗Na2S2O3标准溶液VmL。
①铜的质量分数为________(列出计算表达式)。
②缺少步骤Ⅱ会使测定的铜的质量分数________(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述中正确的是( )
A. 标准状况下,3.36LCCl4中含有,7.5NA个原子
B. 常温常压下,32gO2和O3的混合物中含有的氧原子数约为1.204×1024
C. CO2和标准状况下11.2LHCl具有相同的原子数
D. 1L0.1mol/L的CH3COOH溶液中,H+的数目为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】元素X的原子,其M层与K层电子数相同;元素Y的原子,其L层上有5个电子。X和Y所形成的稳定化合物的式量为( )
A. 100B. 90C. 88D. 80
查看答案和解析>>
科目: 来源: 题型:
【题目】现有四组分散系:①汽油和水形成的混合液②含有泥沙的食盐水③溶有碘(I2)的氯化钾溶液④乙二醇和丙三醇混合溶液(乙二醇和丙三醇的部分物理性质见表)。
物质 | 熔点/℃ | 沸点/℃ | 密度/gcm-3 | 溶解性 |
乙二醇 | 11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
请用如图所示的仪器分离以上各混合液,仪器和方法不能对应的是( )

A. ①—c—分液B. ②—a—萃取
C. ③—c—萃取D. ④—a—蒸馏
查看答案和解析>>
科目: 来源: 题型:
【题目】对于Zn+H2SO4→ZnSO4+H2↑+Q的化学反应,下列叙述不正确的是
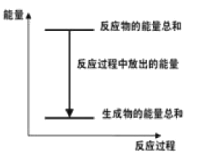
A.反应过程中能量关系如图所示
B.Q的值与反应的计量系数有关
C.若将反应设计成原电池锌为负极
D.若将其设计为原电池,当有32.5g锌溶解,正极放出的气体一定为11.2L
查看答案和解析>>
科目: 来源: 题型:
【题目】硼、铝、镓、铟、铊是第ⅢA族元素,它们在工农业生产中应用非常广泛。
(1)基态硼原子的核外电子排布图为______________________。
(2)I1(Mg)___________I1(Al)(填“大于”或“小于”),其原因是______________________。
(3)三氯化铝加热到177.8℃时,会升华为气态二聚氯化铝(Al2Cl6,其中铝原子和氯原子均达8电子稳定结构),请写出二聚氯化铝(Al2Ci6)的结构式:______________________,其中铝原子轨道采用___________杂化。
(4)BF4-的空间构型为___________,与BF4-互为等电子体的分子是___________ (写化学式,任写一种即可)。
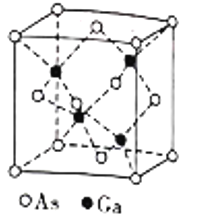
(5)镓(Ga)可与砷(As)形成砷化(GaAs)晶体,该晶体的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________。Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,阿伏加德罗常数值为NA,则晶胞中Ca与As原子的核间距为___________pm。(列出字母表达式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com