
科目: 来源: 题型:
【题目】(1)某气态氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的摩尔质量为___。
(2)已知CO、SO2的混合气体质量共18.4g,标准状况下休积为8.96L,则可推知该混合气体的平均相对分子质量为___。
(3)标准状况下9.03×1023个CH4所占的体积为___,与___个NH3含有相同数目的氢原子。
(4)与16gN2H4所含有分子数相同的氧气的体积(标准状况)是___L。
(5)质量比为51:28的NH3、CO所含质子数之比为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应mX(g) +nY(g) ![]() pZ(g) 在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间的关系如图所示。下述判断正确的是
pZ(g) 在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间的关系如图所示。下述判断正确的是

A. T1<T2 ,P1>P2
B. T1<T2 ,m+n<p
C. m+n>p ,正反应放热
D. P1>P2,正反应吸热
查看答案和解析>>
科目: 来源: 题型:
【题目】咖啡酸具有止血功效,存在于多种中药中,其结构简式如图: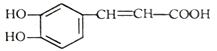 ,下列说法不正确的是
,下列说法不正确的是
A. 咖啡酸可以发生取代、加成、氧化、酯化、加聚反应
B. 1mol咖啡酸最多能与4molH2反应
C. 咖啡酸分子中所有原子可能共面
D. 蜂胶的分子式为C17H16O4,在一定条件下可水解生成咖啡酸和一种一元醇A,则醇A的分子式为C8H12O
查看答案和解析>>
科目: 来源: 题型:
【题目】某结晶水合物的化学式为R·nH2O,其相对分子质量为M。25℃时,将ag该晶体溶于bg水中恰好可形成VmL饱和溶液。下列关系中正确的是( )
A. 饱和溶液的物质的量浓度为![]() mol·L-1
mol·L-1
B. 饱和溶液中溶质的质量分数为![]() %
%
C. 25℃时R的溶解度为![]() g
g
D. 饱和溶液的密度为![]() g·L-1
g·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】若用AG表示溶液的酸度,其表达式为:AG=lg[ ]。室温下,实验室里用0.10 mol/L 的盐酸溶液滴定10 mL 0.10 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
]。室温下,实验室里用0.10 mol/L 的盐酸溶液滴定10 mL 0.10 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是

A. 该滴定过程可选择酚酞作为指示剂
B. C点加入盐酸的体积为10mL
C. 若B点加入的盐酸溶液体积为5mL,所得溶液中:c(M+)+2c(H+)=c(MOH)+2c(OH)
D. 滴定过程中从A点到D点溶液中水的电离程度逐渐增大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列描述中正确的是( )
A. 标准状况下,22.4LCCl4含有的分子数约为6.02×1023个
B. 1L氢气一定比1L氧气质量少
C. 含有6.02×1023个Fe3+的Fe2(SO4)3中SO42﹣的物质的量为3mol
D. 1molAl3+带有的正电荷数为1.806×1024个
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置进行脱硫,将硫化氢气体转化成硫沉淀。已知甲、乙池中发生的反应为(右图):下列说法正确的是( )

A. 该装置中电能转化为光能
B. 电路中每转移0.2mol电子,甲池溶液质量变化 3.4g,乙池溶液质量保持不变
C. 光照时乙池电极上发生的反应为:H2S+I3-=3I-+S+2H+
D. 甲池中碳棒上发生的电极反应为:AQ+2H+-2e-=H2AQ
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期W、X、Y、Z、Q五种元素的原子序数依次递增,W和Z位于同一主族。已知W的氢化物可与Q单质在光照条件下反应生成多种化合物,且Y、Q形成一种共价化合物,X的最高价氧化物对应的水化物可与Z单质反应产生常见的还原性气体单质E。下列说法不正确的是( )
A. X、Z的最高价氧化物相互化合,生成的产物可用作防火剂
B. Y、Q形成的化合物是强电解质
C. W、X、Q三种元素都能形成多种氧化物
D. 电解X、Q元素组成的化合物的饱和溶液常被用于实验室制备E单质
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物A是农药生产中的一种中间体,其结构简式如图,下列叙述不正确的是( )

A. 有机物A属于芳香族化合物
B. 有机物A和NaOH的醇溶液共热可发生消去反应
C. 有机物A和浓硫酸混合加热,可以发生消去反应
D. 1molA和足量的NaOH溶液反应,最多可以消耗 3molNaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)如下图所示,左室容积为右室的两倍,温度相同,现分别按照如图所示的量充入气体,同时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡,下列说法正确的是_____

A.第一次平衡时,SO2的物质的量右室更多
B.通入气体未反应前,左室压强和右室一样大
C.第一次平衡时,左室内压强一定小于右室
D.第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2的物质的量的2倍还要多
(2)NH3合成常见的化肥尿素【化学式为CO(NH2)2】分为三步,其中第一步为:2NH3(g)+CO2(g)![]() NH2COONH4(s) ΔH= -159.5kJ/mol,对于这个反应,在2L等容密闭容器中充入2molNH3和1molCO2,平衡时放出127.6kJ的热量,若反应温度不变,在该容器中充入2.8molNH3和1.4molCO2,到达平衡时,c(NH3)为___________。
NH2COONH4(s) ΔH= -159.5kJ/mol,对于这个反应,在2L等容密闭容器中充入2molNH3和1molCO2,平衡时放出127.6kJ的热量,若反应温度不变,在该容器中充入2.8molNH3和1.4molCO2,到达平衡时,c(NH3)为___________。
(3)①室温下,在0.5mol/L纯碱溶液中加入少量水,由水电离出的c(H+)×c(OH-)_________。(填“变大”、“变小”、“不变”)
②已知Ksp(Ag2CrO4)=1.0×10-12,向0.2mol/L的AgNO3溶液中加入等体积的0.00008mol/LK2CrO4溶液,则溶液中的c(CrO42-)=___________。
③室温下,0.1mol/LNaHCO3溶液的pH值______0.1mol/LNa2SO3溶液的pH值(填“>”、“<”、“=”)已知:
H2CO3 | K1=4.3×10-7 | K2=5.6×10-11 |
H2SO3 | K1=1.54×10-2 | K2=1.02×10-7 |
(4)有一种可充电电池Na—Al/FeS,电池工作时Na+的物质的量保持不变,并且是用含Na+的导电固体作为电解质,已知该电池正极反应式为2Na++FeS+2e—=Na2S+Fe,则该电池在充电时,阳极发生反应的物质是____________,放电时负极反应式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com