
科目: 来源: 题型:
【题目】电池是人类生产和生活中的重要能量来源,下列有关电池的叙述正确的是( )
A. 锌锰干电池工作一段时间后碳棒变细
B. 铅蓄电池放电时铅在负极被氧化成二氧化铅
C. 太阳能电池的主要材料是高纯度的二氧化硅
D. 氢氧燃料电池产物为水,属于环境友好电池
查看答案和解析>>
科目: 来源: 题型:
【题目】乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值。

① 称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;
请回答:
⑴ 滴定时,将KMnO4标准液装在右图中的 (填“甲”或“乙”)滴定管中。
⑵ 本实验滴定达到终点的标志可以是 。
⑶ 通过上述数据,计算出x= 。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知地球上元素原子各电子层最多能容纳的电子数为2n2(n表示电子层序数),若X星球上的元素原子各电子层最多能容纳的电子数为n(n+1),n表示电子层数,该星球上元素原子的电子排布的其他规则与地球相同,回答下列问题:
(1)X星球上的质子数为5的元素原子最外层电子数为___个;
(2)X星球上的质子数为9的元素原子的结构示意图为___,该元素属于___元素(填“金属”或“非金属”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】A~E是核电荷数均小于20的元素,其结构或性质信息如表:
元素 | A | B | C | D | E |
性质或结构信息 | 其原子核内只有1个质子 | 其单质在空气中体积含量最多 | 其原子M层有3个电子 | 食盐中的金属元素 | 单质在常温、常压下是黄绿色的气体 |
请根据表中的信息回答下列问题:
(1)D离子的结构示意图:___,B原子的电子式:___,E离子的电子式:___。
(2)和B元素的氢化物所含电子数相同的分子有多种,写出任意2种:_________。
(3)A元素与E元素组成的化合物的电离方程式:____。
(4)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是___;写出钾离子的电子式:____。

查看答案和解析>>
科目: 来源: 题型:
【题目】(1)实验测得,5 g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,试写出甲醇燃烧的热化学方程式:_________________________________________。
(2)下图为N2(g)和O2(g)生成NO (g)过程中的能量变化:

则N≡N键的键能为________kJ·mol-1。根据上图写出N2(g)和O2(g)生成NO(g)的热化学方程式:_____________________________________________________________
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知: C(石墨,s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1①
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:________________________________________________________________________。
(4)接触法制硫酸工艺中,其主反应在450 ℃并有催化剂存在下进行:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-190 kJ·mol-1。
2SO3(g) ΔH=-190 kJ·mol-1。
①该热化学反应方程式的意义是___________________________________________________
②已知单质硫16 g燃烧放热为149 kJ,写出硫燃烧热的热化学方程式:_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】电解饱和食盐水是一项重要的化学工业,请完成下列计算:
(1)当电解产生0.2molNaOH时,能收集到标准状况下的H2____L。
(2)已知室温时饱和食盐水的溶质质量分数为0.265,取200g饱和食盐水进行电解,当NaCl反应了一半时停止电解,
①求出所得混合溶液中NaCl的质量。_____
②求出所得混合溶液中NaOH的质量分数。____(写出计算过程,保留3位小数)
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物F(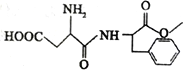 )是一种应用广泛可食用的甜味剂,俗称蛋白糖,它的一种合成路线如图所示
)是一种应用广泛可食用的甜味剂,俗称蛋白糖,它的一种合成路线如图所示

已知:①A能发生银镜反应
②
③R-CN![]() R-COOH
R-COOH
请回答下列问题:
(1)D中官能团的名称为___________,F的分子式为___________。
(2)A的名称为___________,反应③的反应类型为___________。
(3)反应④的化学方程式为___________。
(4)反应⑤中的另一种生成物是水,则X的结构简式为___________。
(5)D有多种同分异构体,请写出一种符合下列条件的有机物的结构简式___________;
①苯环上有2个取代基
②与D具有相同的官能团
③核破共振氢谱为6组峰且峰面积比为2:2:2:2:2:1
(6)丙烯酸是重要的有机合成原料及合成树脂单体,请写出以CH3CHO为原料合成丙烯酸的合成路线___________(其它试剂任选)
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用下列两种方法制取氯气:①用含HCl 146g的浓盐酸与足量的MnO2反应;②用87g MnO2与足量的浓盐酸反应,则所得Cl2质量
A. ①比②多B. ②比①多C. 一样多D. 无法比较
查看答案和解析>>
科目: 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如图:

(1)粗盐中含CaCl2、MgCl2等杂质,写出精制过程中发生反应的化学方程式是__,__。
(2)如果粗盐中SO42-含量较高,必须添加钡式剂除去SO42-,该钡试剂可以是__。
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(3)电解过程中所发生反应的化学方程式为___,与电源正极相连的电极附近产生的气体是__,检验该气体可使用___试纸,现象是试纸变为___色。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com