
科目: 来源: 题型:
【题目】工业上可由乙苯生产苯乙烯:![]() ,下列有关说法正确的是
,下列有关说法正确的是
A. 乙苯和苯乙烯均能发生取代反应、加聚反应和氧化反应
B. 用溴水可以区分苯乙烯和乙苯
C. 1 mol苯乙烯最多可与4 mol氢气加成,加成产物的一氯代物共有5种
D. 乙苯和苯乙烯分子中共平面的碳原子数最多都为7
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是三大工业用酸之一,在冶金、石油工业、制药、国防等方面都要用到硫酸。将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。试回答:
(1)加入少量水的原因是_________________________________________________。
(2)生成的黑色物质是______________(写出化学式)。
(3)“体积膨胀,并放出有刺激性气味的气体(SO2)”,写出对应的化学方程式:_________________________________________________。
(4)上述现象体现了浓硫酸的_________________(填序号)
①酸性 ②吸水性 ③脱水性 ④强氧化性
(5)向80mL浓硫酸中加入5.6g铜,加热一段时间后至不再反应为止,实验测得反应中共有1.12L(标准状况下)SO2气体生成,该反应的化学方程式为_____________________________________,反应中转移电子______mol,铜剩余_______g,该反应中浓硫酸体现了___________和__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在25℃时,纯水的电离度为α1,pH=3的醋酸中水的电离度为α2,pH=11的氢氧化钠溶液中水的电离度为α3。若将上述醋酸溶液和氢氧化钠溶液等体积混合,所得溶液中水的电离度为α4,则下列关系正确的是
A. α1<α3<α2<α4 B. α3<α2<α1<α4 C. α2=α3<α1<α4 D. α2=α3<α4<α1
查看答案和解析>>
科目: 来源: 题型:
【题目】四氯化锡可用作媒染剂。利用如图装置可以制备四氯化锡(部分夹持装置已略去)。

有关信息如下表:
化学式 |
|
|
摩尔质量( | 190 | 261 |
熔点 | 246 | -33 |
沸点 | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)装置甲中仪器![]() 的名称为_____________。
的名称为_____________。
(2)用装置甲制取氯气,![]() 被还原为
被还原为![]() ,该反应的离子方程式为___________。
,该反应的离子方程式为___________。
(3)将如图装置连接好,先检查装置气密性,再慢慢滴入浓盐酸,待观察到___________(填现象)后,开始加热装置丁,锡熔化后适当增大氯气流量,继续加热装置丁,此时继续加热装置丁的目的是:①促进氯气与锡反应;②_________________________。
(4)如果缺少装置乙,可能发生的副反应的化学方程式为_______________;装置己的作用是______(填字母代号)。
A.除去未反应的氯气,防止污染空气
B.防止空气中![]() 气体进入装置戊
气体进入装置戊
C.防止水蒸气进入装置戊的试管中使产物水解
D.防止空气中![]() 进入装置戊的试管中使产物氧化
进入装置戊的试管中使产物氧化
(5)某同学认为丁装置中的反应可能产生![]() 杂质,以下试剂中可用于检测是否产生
杂质,以下试剂中可用于检测是否产生![]() 的是______(填字母代号)。
的是______(填字母代号)。
A. ![]() 溶液 B.
溶液 B. ![]() 溶液(滴有
溶液(滴有![]() 溶液) C.
溶液) C. ![]() 溶液
溶液
(6)反应中用去锡粒![]() ,反应后在戊装置的试管中收集到
,反应后在戊装置的试管中收集到![]() ,则
,则![]() 的产率为_____(保留3位有效数字)。
的产率为_____(保留3位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 在含CO32-总数为NA的Na2CO3溶液中,Na+总数为2NA
B. 标准状况下,2.24 L乙烷和丙烯的混合物中含氢原子数目为0.6NA
C. 将0.1 mol H2和0.2 mol I2(g)充入密闭容器中充分反应后,生成的H-I键数目为0.2NA
D. 常温下,电解1 L的精制食盐水,一段时间后测得溶液pH为11,则电解过程中通过导线的电子数目为0.002NA
查看答案和解析>>
科目: 来源: 题型:
【题目】乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO![]() +5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
学习小组的同学设计了如下步骤用滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.1000 mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL。
(1)上述步骤②中使用的锥形瓶是否需要事先用待测液润洗_______。(填“是”或“否”)滴定时,将酸性KMnO4标准液装在如图中的________(填“甲”或“乙”)滴定管中。

(2)本实验滴定达到终点的标志可以是________________________________。
(3)通过上述数据,求得x=________。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会________(填“偏大”、“偏小”或“不变”,下同)。
②根据上述实验计算的数据可信性不强,为了提高实验的准确性,请写出改进方法______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】等物质的量的Na2CO3·mH2O和BaCl2·nH2O的混合物3.68g,加入足量水搅拌,经充分反应后可得1.97g沉淀。则m和n值分别是
A.10和2B.7和3C.3和1D.1和2
查看答案和解析>>
科目: 来源: 题型:
【题目】(化学----选修5:有机化学基础)
![]() 是药物合成中的一种重要中间体,下面是
是药物合成中的一种重要中间体,下面是![]() 的一种合成路线:
的一种合成路线:

已知: 。
。
请回答下列问题:
(1)![]() 所含官能团的名称为___________;
所含官能团的名称为___________;![]() 的结构简式为_______________,
的结构简式为_______________,![]() 生成
生成![]() 的反应类型为_______________________。
的反应类型为_______________________。
(2)![]() 的名称是____________。
的名称是____________。
(3)由![]() 和
和![]() 合成
合成![]() 的化学方程式为______________________。
的化学方程式为______________________。
(4)![]() 的同分异构体中,能发生银镜反应且分子结构中含苯环的还有_______________种,其中核磁共振氢谱上有6组峰,峰面积之比为1:1:1:1:1:1的同分异构体的结构简式为__________(一种即可)。
的同分异构体中,能发生银镜反应且分子结构中含苯环的还有_______________种,其中核磁共振氢谱上有6组峰,峰面积之比为1:1:1:1:1:1的同分异构体的结构简式为__________(一种即可)。
(5)参照上述合成路线,以![]() 为原料(其他试剂任选),设计制备巴豆醛(
为原料(其他试剂任选),设计制备巴豆醛(![]() )的合成路线。________________________________________
)的合成路线。________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】氮是植物体内蛋白质、叶绿素的重要组成元素,氮肥能促进农作物的生长。氨是生成氮肥的原料。回答下列问题:
(1)氮气的电子式________________ ,氨的结构式__________________;
(2)氨水显碱性,写出氨水的电离方程式___________________________________________;
(3)氨催化氧化生成NO是工业制硝酸的反应之一,写出该反应的化学方程式:________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(化学---选修3:物质结构与性质)
(1)![]() 中
中![]() 原子的杂化轨道类型为____________,
原子的杂化轨道类型为____________,![]() 分子空间构型为________________。
分子空间构型为________________。
(2)已知:硼酸的电离方程式为![]() ,试依据上述反应写出
,试依据上述反应写出![]() 的结构式____________________。
的结构式____________________。
(3)钛铁矿经过![]() 等多种物质处理后会生成
等多种物质处理后会生成![]() 等中间产物。
等中间产物。
①![]() 晶体中存在_________________(填字母代号)。
晶体中存在_________________(填字母代号)。
A. 离子键 B. ![]() 键 C.
键 C. ![]() 键 D.氢键
键 D.氢键
②![]() 为粘稠状、难挥发性的强酸,而
为粘稠状、难挥发性的强酸,而![]() 是易挥发性的强酸,其原因是____________________。
是易挥发性的强酸,其原因是____________________。
(4)![]() 是离子晶体,其晶格能可通过下图的
是离子晶体,其晶格能可通过下图的![]() 循环计算得到。
循环计算得到。
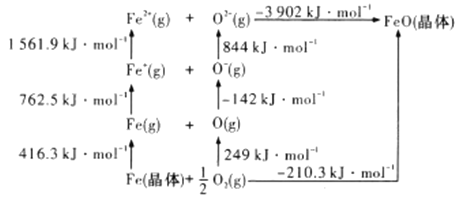
可知,![]() 原子的第一电子亲和能为___________
原子的第一电子亲和能为___________![]() ,
,![]() 晶格能为______________
晶格能为______________![]() 。
。
(5)![]() 可用于制造高温发热元件,其在高温时具有立方晶型,晶胞如图所示。
可用于制造高温发热元件,其在高温时具有立方晶型,晶胞如图所示。

已知晶胞参数为![]() ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为![]() ,则
,则![]() 原子与
原子与![]() 原子之间的最短距离为_______
原子之间的最短距离为_______![]() ;
;![]() 的密度为_______________________
的密度为_______________________![]() (列式表示)。
(列式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com