
科目: 来源: 题型:
【题目】已知Ca3(PO4)2与SiO2、C高温共热可以反应得到CaSiO3、P4蒸气和CO。反应如下:Ca3(PO4)2+SiO2+C![]() CaSiO3+P4↑+CO↑。
CaSiO3+P4↑+CO↑。
(1)配平该反应方程式,并标出电子转移方向和数目_____。
(2)该反应中被还原的元素是___,氧化产物是______。
(3)每消耗24.0g碳时,有___个电子发生转移,生成P4__g。
(4)反应所得混合气体,折算成标况下,其气体密度为____g/L(保留两位小数)。
(5)与该反应中涉及到的磷元素相同主族的氮元素,是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180 mg/L。
①写出NH4Cl的电子式____。
②为除去废水中的NH4+,向103L该污水中加入0.1 mol/LNaOH溶液,发生如下反应:NH4++OH-=NH3+H2O,则理论上需要NaOH溶液的体积为___L(计算结果保留两位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在t℃时,将agNH3完全溶于水,得到VmL溶液,设该溶液的密度为ρg·cm-3,质量分数为ω,其中含NH4+的物质的量为bmol。下列叙述中不正确的是
A.溶质的质量分数ω=![]() ×100%
×100%
B.溶质的物质的量浓度c=1000a/17Vmol·L-1
C.溶液中c(OH-)=1000b/Vmol·L-1+c(H+)
D.上述溶液中再加入VmL水后,所得溶液中溶质的质量分数小于0.5ω
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的前四周期元素,X的电子总数=周期序数=族序数,他们的单质或化合物存在如图所示的转化关系,其中甲、戊是两种最常见的金属单质,丁是非金属单质,其余为氧化物。下列说法正确的是

A. W的原子序数是Z的两倍,金属性强于Z
B. Z元素在周期表中的位置是第三周期Ⅲ族
C. 丙属于两性氧化物
D. 己的熔点高、硬度大,可用作耐火坩埚
查看答案和解析>>
科目: 来源: 题型:
【题目】达康书记又追问环保局长:那么垃圾处理中,能随便焚烧吗?焚烧垃圾会降低GDP的。在焚烧垃圾过程中发生了( )
A. 吸热的非氧化还原反应B. 吸热的氧化还原反应
C. 放热的非氧化还原反应D. 放热的氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温、恒压下,在一个可变容积的容器中发生反应:A(g)+B(g) ![]() C(g)
C(g)
(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时n(A)为________mol。
(2)若开始时放入3molA和3molB,达到平衡后,生成n(C)为________mol。
(3)若开始时放入x mol A、2mol B和1mol C,达到平衡后,A和C的物质的量分别是ymol和3amol,则x=________,y=________。平衡时,n(B)________(填序号)。
A.大于2mol B.等于2mol C.小于2mol D.可能大于、等于或小于2mol
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是________。
(5)若保持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。开始时放入1molA和1molB,达到平衡后,生成b molC,将b与a进行比较,则________(填序号)。
A.a<b B.a>b C.a=b D.不能比较
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇、氧气和强碱溶液作电解质的手机电池中的反应为2CH3OH+3O2+40H-![]() 2CO32-+6H2O,有关说法正确的是
2CO32-+6H2O,有关说法正确的是
A. 放电时,CH3OH 参与反应的电极为正极
B. 放电时,负极电极反应:CH3OH+8OH--6e-=CO32-+6H2O
C. 标准状况下,通入的11.2LO2完全反应有1mol电子转移
D. 充电时电解质溶液的pH逐渐减小
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)25 ℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如表:
热化学方程式 | 平衡常数 | |
① | 2NO2(g)+NaCl(s) | K1 |
② | 4NO2(g)+2NaCl(s) | K2 |
③ | 2NO(g)+Cl2(g) | K3 |
则该温度下,ΔH3=_______________kJmol-1;K3=_____________(用K1和K2表示)。
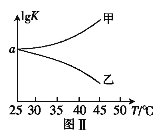
(2)25℃时,在体积为2L的恒容密闭容器中通入0.08 mol NO和0.04 molCl2发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则ΔH3 ___(填“>”“<”或“=”)0;若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图Ⅰ虚线所示,则改变的条件是_____________;在5 min时,再充入0.08 mol NO和0.04 molCl2,则混合气体的平均相对分子质量将_____________(填“增大”、“减小”或“不变”)。图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(lgK)与温度的变化关系图,其中正确的曲线是______(填“甲”或“乙”),a值为__________。25 ℃时测得反应③在某时刻,NO(g)、Cl2(g)、NOCl(g)的浓度分别为0.8、0.1、0.3,则此时v正_________v逆(填“>”“<”或“=”)

(3)在300 ℃、8 MPa下,将CO2和H2按物质的量之比1∶3 通入一密闭容器中发生CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)中反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=_____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
CH3OH(g)+H2O(g)中反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=_____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】国际计量大会第26次会议新修订了阿伏加德罗常数(NA=6.02214076×1023mol-1),并于2019年5月20日正式生效。下列说法正确的是
A. 1L0.5mol·L-1Al2Fe(SO4)4溶液中阳离子数目小于1.5NA
B. 2 mol NH3和3molO2在催化剂和加热条件下充分反应生成NO的分子数为2NA
C. 56g聚乙烯分子中含碳碳双键的数目为2NA
D. 32.5g锌与一定量浓硫酸恰好完全反应,生成气体的分子数为0.5NA
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究。
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:

①装置D的名称为___________。
②按照气流从左到右的方向,上述装置的连接顺序为___________→尾气处理装置(填仪器接口的字母编号)。
③实验前先通入一段时间N2,其目的为______________________。
④实验证明了气体产物中含有CO,依据的实验现象为______________________。
(2)固体产物成分的探究。充分反应后,A处反应管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为___________。
(3)依据(1)和(2)结论,可知A处反应管中发生反应的化学方程式为___________。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液。
步骤2:取上述溶液25.00mL,用c mol· L -1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤3中加入锌粉的目的为____________________________________________。
(5)草酸亚铁晶体样品的纯度为____________________________________________;若步骤1配制溶液时部分Fe2+被氧化,则测定结果将___________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨是重要的氮肥,合成原理为: N2(g)+3H2(g)![]() 2NH3(g) △H= —92.4 kJ/mol。在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各种物质的量变化如图,回答下列问题:
2NH3(g) △H= —92.4 kJ/mol。在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各种物质的量变化如图,回答下列问题:

(1)10 min内以NH3表示的平均反应速率:______;
(2)在10 ~20 min内:NH3浓度变化的原因可能是______________
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加NH3物质的量
(3)第1次平衡的平衡常数K1 = _________________(带数据的表达式),第2次平衡时NH3的体积分数=___________(小数点后保留一位);
(4)在反应进行至25 min时:①曲线发生变化的原因______________,② 达第二次平衡时,新平衡的平衡常数K2 ____ K1(填“大于”“等于”或“小于”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com