
科目: 来源: 题型:
【题目】某课题小组探究乙酸乙酯(CH3COOC2H5)在不同温度、不同浓度NaOH溶液中的水解速率,取四支大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积来确定水解反应的速率。
实验试剂 | 试管Ⅰ(55 ℃) | 试管Ⅱ(55 ℃) | 试管Ⅲ(55 ℃) | 试管Ⅳ(75 ℃) |
乙酸乙酯/mL | 1 | V1 | V2 | V3 |
1 mol/L NaOH mL | V4 | 3 | 0 | V5 |
蒸馏水/mL | 0 | V6 | 5 | 2 |
已知:①水解反应CH3COOC2H5 + H2O ![]() CH3COOH + C2H5OH;
CH3COOH + C2H5OH;
②CH3COOC2H5难溶于水,密度比水小。
(1)V4 = ____________。
(2)①下列说法正确的是____________________________;
A、加入水,平衡正向移动
B、加入稀盐酸可使平衡逆向移动
C、酯层体积不再改变时,反应停止
D、c(CH3COOH) = c(C2H5OH)时,反应达平衡状态
②用各物质的浓度表示水解平衡常数Kh,则表达式为____________。
(3)实验中常用饱和食盐水代替蒸馏水,目的是减小乙酸乙酯在水中的溶解度,会使实验结果更准确,______________填“能”或“不能”)用饱和Na2CO3溶液代替蒸馏水。
(4)实验中,试管Ⅳ比试管Ⅱ中的酯层减少更快,可能的原因有_______。(乙酸乙酯的沸点为77.1 ℃)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子在指定的溶液中,能大量共存的是( )
A.使pH试纸显蓝色的溶液:Cu2+、NO![]() 、Fe3+、SO
、Fe3+、SO![]()
B.与铁粉反应放出H2的无色溶液:NO![]() 、Fe2+、Na+、SO
、Fe2+、Na+、SO![]()
C.使红色石蕊试纸变蓝的溶液:SO![]() 、CO
、CO![]() 、Na+、K+
、Na+、K+
D.Na2CO3溶液:Al3+、SO![]() 、Cl-、K+
、Cl-、K+
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为_______,其沸点比NH3的_______(填“高”或“低”),其判断理由是_________________________。
(2)Fe成为阳离子时首先失去______轨道电子,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为______________________。
(3)比较离子半径:F__________O2(填“大于”等于”或“小于”)。
(4)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。

图中F和O2共同占据晶胞的上下底面位置,若两者的比例依次用x和1x代表,则该化合物的化学式表示为____________,通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=________g·cm3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(![]() ),则原子2和3的坐标分别为__________、__________。
),则原子2和3的坐标分别为__________、__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。乙醇水蒸气重整制氢的部分反应过程如图1所示:


已知:反应I和反应Ⅱ的平衡常数随温度变化曲线如图2所示:
(1)①写出反应I中的化学方程式是________________。
②若反应I在恒温恒压条件下,向体系中充入N2,乙醇的平衡转化率___(填“增大”、“减小”或“不变”),理由是___________。
(2)反应Ⅱ在进气比[n(CO):n(H2O)]不同,测得相应的CO的平衡转化率见下图3(各点对应的反应温度可能相同,也可能不同)。

①图中D、E两点对应的反应温度分别为TD和TE。判断:TD______________TE(填“<”“=”或“>”);
②当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是___(用简要的文字叙述)。
(3)已知:
a、2CH3OH(g) + CO2(g) ![]() CO(OCH3)2(g) + H2O(g) △H = -15.5 kJ/mol,该反应在0 ℃时K≈10-4.5;
CO(OCH3)2(g) + H2O(g) △H = -15.5 kJ/mol,该反应在0 ℃时K≈10-4.5;
b、2CH3OH(g) + CO2(g) + ![]() (g)
(g) ![]() CO(OCH3)2(g) +
CO(OCH3)2(g) + ![]() (g)△H = -110.7 kJ/mol。依据以上数据,文献认为反应a没有工业价值,你认为其理由是______________________;但反应b引入环氧丙烷(
(g)△H = -110.7 kJ/mol。依据以上数据,文献认为反应a没有工业价值,你认为其理由是______________________;但反应b引入环氧丙烷(![]() )可有效促进CO2与CH3OH反应生成CO(OCH3)2,其原因是_________________________________。
)可有效促进CO2与CH3OH反应生成CO(OCH3)2,其原因是_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知:![]() (g)=
(g)= ![]() (g)+H2(g) ΔH1=100.3 kJ·mol 1 ①
(g)+H2(g) ΔH1=100.3 kJ·mol 1 ①
H2(g)+ I2(g)=2HI(g) ΔH2=﹣11.0 kJ·mol 1 ②
对于反应:![]() (g)+ I2(g)=
(g)+ I2(g)=![]() (g)+2HI(g) ③ ΔH3=___________kJ·mol 1。
(g)+2HI(g) ③ ΔH3=___________kJ·mol 1。
(2)某温度下,等物质的量的碘和环戊烯(![]() )在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为_________,该反应的平衡常数Kp=_________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有__________(填标号)。
)在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为_________,该反应的平衡常数Kp=_________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有__________(填标号)。
A.通入惰性气体 B.提高温度
C.增加环戊烯浓度 D.增加碘浓度
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是__________(填标号)。

A.T1>T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L1
(4)环戊二烯可用于制备二茂铁(Fe(C5H5)2结构简式为 ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。

该电解池的阳极为____________,总反应为__________________。电解制备需要在无水条件下进行,原因为_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。回答下列问题:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧立德粉样品时,钡的焰色为__________(填标号)。
A.黄色 B.红色 C.紫色 D.绿色
(2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:

①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为______________________。回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源气体,该反应的化学方程式为______________________。
②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差。其原因是“还原料”表面生成了难溶于水的___________(填化学式)。
③沉淀器中反应的离子方程式为______________________。
(3)成品中S2的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000 mol·L1的I2KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉溶液为指示剂,过量的I2用0.1000 mol·L1Na2S2O3溶液滴定,反应式为I2+2![]() =2I+
=2I+![]() 。测定时消耗Na2S2O3溶液体积V mL。终点颜色变化为_________________,样品中S2的含量为______________(写出表达式)。
。测定时消耗Na2S2O3溶液体积V mL。终点颜色变化为_________________,样品中S2的含量为______________(写出表达式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关含碳微粒的说法,按要求填空:
(1)同温度,同浓度的Na2CO3溶液的碱性_________ NaHCO3溶液的碱性(填“大于”、“小于”或“等于”),请设计一个较简便的实验证明___________。
(2)在25 ℃时,在10 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液20 mL,溶液中含碳微粒的物质的量随溶液pH的变化如图所示。
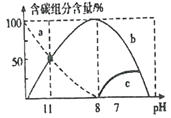
①HC1溶液滴加到一半时,溶液呈___________(填“酸性”、“碱性”或“中性”),理由是____________________(用主要的离子方程式表示)。
②关于图像下列说法正确的是_________________。
A、0.1 mol/L Na2CO3溶液中:c(Na+) + c(H+) = c(OH-) + 2c(CO32-) + c(HCO3-)
B、b曲线代表CO32-
C、pH=11时,c(HCO3-) > c(Cl-)
D、pH=11 时,c(Na+) + c(H+) = 3c(CO32-) + c(OH-)
E、在同一溶液中,H2CO3、HCO3-、CO32-能大量共存
(3)草酸(H2C2O4)溶液具有还原性,将酸性KMnO4溶液滴入草酸溶液中,会产生气泡,且紫红色褪去,写出该反应的离子方程式________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应COCl2(g) ![]() Cl2(g) + CO(g) △H>0达到平衡时各物质的浓度在不同条件下的变化状况如图所示(第10 min到14 min的COCl2浓度变化曲线未示出)。
Cl2(g) + CO(g) △H>0达到平衡时各物质的浓度在不同条件下的变化状况如图所示(第10 min到14 min的COCl2浓度变化曲线未示出)。
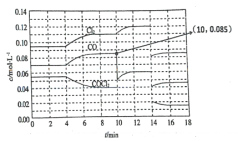
下列说法正确的是
A. 第4 min时改变的条件可能是扩大容器体积
B. 第2 min时的平衡常数K(2)大于第8 min时的平衡常数K(8)
C. 12 min时反应在温度T(8)下重新达到平衡,则此时c(COCl2) = 0.031 mol/L(结果保留两位有效数字)
D. 产物CO在2~3 min、5~6 min、12~13 min时的平均反应速率大小为:υ(5~6) > υ(2~3) > υ(12~13)
查看答案和解析>>
科目: 来源: 题型:
【题目】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
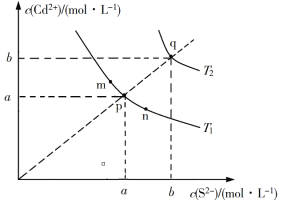
A. 图中a和b分别为T1、T2温度下CdS在水中的溶解度
B. 图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C. 向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D. 温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】T ℃,分别向10 mL浓度均为1 mol/L的两种弱酸HA、HB中不断加水稀释,并用pH传感器测定溶液pH。所得溶液pH的两倍(2pH)与溶液浓度对数(lgc)的关系如图所示。
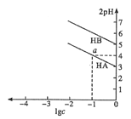
已知:pKa = -lgKa。
下列叙述正确的是
A. 弱酸的Ka随溶液浓度的降低而增大
B. a点对应的溶液中c(HA) = 0.1 mol/L,pH=4
C. 酸性:HA<HB
D. 弱酸HB的pKa≈5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com