
科目: 来源: 题型:
【题目】实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,回答下列问题:
(1)已知某温度下某反应的化学平衡常数表达式为:K=c(H2O)/[ c(CO)·c(H2)]所对应的化学反应方程式为:________。
(2)已知在一定温度下:
①C(s)+CO2(g) ![]() 2CO(g) △H1=a kJ/mol 平衡常数K1;
2CO(g) △H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g) ![]() H2(g)+CO2(g) △H2=b kJ/mol 平衡常数K2;
H2(g)+CO2(g) △H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g) ![]() CO(g)+H2(g)△H3 平衡常数K3。
CO(g)+H2(g)△H3 平衡常数K3。
则K1、K2、K3之间的关系是:________,△H3=________(用含a、b的代数式表示)。
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
该反应的正反应方向是________反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020 mol/L,在该条件下,CO的平衡转化率为:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)某温度下,纯水中c(H+)=2×10﹣7 mol/L, 则此温度下水的离子积为______.若温度不变,滴入稀盐酸使c(H+)=5×10﹣4 mol/L, 则此时c(OH﹣)=________.由水电离产生的c(H+)为________,此时温度________(填“高于”、“低于”或“等于”)
(2)①25℃时,NaHSO3溶液呈_______性,原因是_______(用离子方程式结合文字回答)
②常温下,pH=9的NaOH与pH=13的NaOH等体积混合后溶液的pH=________;
(3)25℃时,部分物质的电离平衡常数如表所示,请回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为________。
②将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl﹣、Mg2+、Ba2+、CO32﹣、SO42﹣,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.03mol(已知OH—+NH4+![]() NH3↑+H2O)
NH3↑+H2O)
(3)第三份加足量BaCl2溶液后,得干燥沉淀4.3g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.根据上述实验,以下推测不正确的是( )
A.K+一定存在B.100mL溶液中含0.01molCO32﹣
C.Cl﹣可能存在D.Ba2+和Cl﹣一定不存在
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)甲醇是可再生能源,具有开发应用的广阔前景,回答下列问题:
一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g)CH3OH(g)
①下列情形不能说明该反应已达到平衡状态的是________(填序号).
A.每消耗1mol CO的同时生成2molH2 B.混合气体总物质的量不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.生成CH3OH的速率与消耗CO的速率相等
②CO的平衡转化率(α)与温度、压强的关系如图所示.A、B两点的平衡常数K(A)________K(B)(填“>”、“=”或“<”).
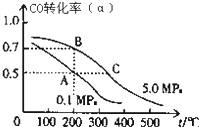
(2)已知25℃合成氨反应中,1mol N2完全转化为NH3时释放的能量为92.4 kJ。现将1mol N2和3mol H2混合置于2L密闭容器中,反应进行到2s末测得NH3为0.4mol。回答下列问题:
① 该反应的热化学方程式是________ ;
② 该反应达到平衡后,升高温度平衡向________ (填“正反应方向”、“逆反应方向”)移动;加入催化剂平衡________(填“正”、“逆”、 “不”)移动;
③ 前2s内v(H2)是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种新型的双离子可充电电池的原理如图所示,以下说法正确的是
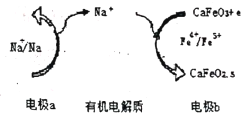
A. 电极a发生的反应为还原反应
B. 充电时a极与电源的正极相连
C. 正极发生的电极反应可能为:CaFeO3+e-=CaFeO2.5+1/2O2-
D. 放电时,每当有NA个Na+移向b极,外电路中一定转移2NA个电子
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示溶液中c(H+)和c(OH﹣)的关系,下列判断错误的是
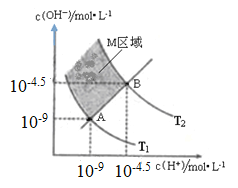
A. 两条曲线间任意点均有c(H+)×c(OH﹣)=KW
B. M区域内任意点均有c(H+)<c(OH﹣)
C. 图中T1<T2
D. XZ线上任意点均有pH=7
查看答案和解析>>
科目: 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是( )
A. 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B. 当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(O2)
C. 当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D. 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物F是一种药物合成的中间体,F的一种合成路线如下:
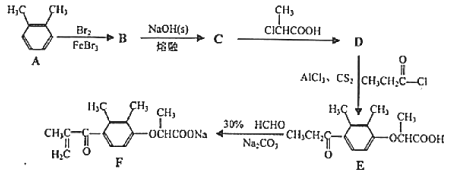
已知:
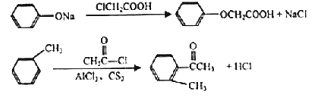
回答下列问题:
(1)![]() 的名称为____。
的名称为____。
(2)D中含氧官能团的名称为____。
(3)B→C的反应方程式为____。
(4)D→E的反应类型为____。
(5)C的同分异构体有多种,其中苯环上连有—ONa、2个—CH3的同分异构体还有____种,写出核磁共振氢谱为3组峰,峰面积之比为6:2:1的同分异构体的结构简式____。
(6)依他尼酸钠(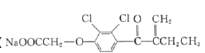 )是一种高效利尿药物,参考以上合成路线中的相关信息,设计以
)是一种高效利尿药物,参考以上合成路线中的相关信息,设计以![]() 为原料(其他原料自选)合成依他尼酸钠的合成路线。________________
为原料(其他原料自选)合成依他尼酸钠的合成路线。________________
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列十种物质:①蔗糖 ②熔融NaCl ③石墨 ④铜丝 ⑤NaOH固体 ⑥SO2 ⑦NaHSO4固体 ⑧K2O固体 ⑨液态H2SO4 ⑩饱和FeCl3溶液
(1)上述物质中可导电的是_____(填序号,下同);
(2)上述物质中不能导电,但属于电解质的是_____。
(3)⑦在水溶液中的电离方程式为__________________________________。
(4)实验室制备少量Fe(OH)3胶体所用的物质有______(填序号)和蒸馏水,反应的离子方程式为_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,氧化剂与还原剂个数的关系为2∶1的是
A.O3+2KI+H2O=2KOH+I2+O2
B.2CH3COOH+Ca(ClO)2=2HClO+(CH3COO)2Ca
C.I2+2NaClO3=2NaIO3+Cl2
D.4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com