
科目: 来源: 题型:
【题目】二氧化氯(ClO2)与亚氯酸钠(NaClO2)都具有强氧化性。两者作漂白剂时,不伤害织物;作饮用水消毒剂时,不残留异味。某研究性学习小组由二氧化氯制备亚氯酸钠,并探究其性质的实验如下。
(资料査阅)①SO2可将 NaClO3还原为ClO2;② NaClO2酸化生成NaCl,并放出ClO2

实验步骤如下
I.组装仪器并检查气密性。仪器组装完毕(如图所示),关闭①②③三个止水夹及b活塞,打开a的活塞,向A的圆底烧瓶中注入水,检查装置的气密性。
Ⅱ.制备亚氯酸钠。在各装置中分别加入相应的试剂,关闭止水夹①③和b的活塞,打开止水夹②及a的活塞,向A的圆底烧瓶中滴入75%硫酸。
III.探究亚氯酸钠的性质。打开止水夹①和②,关闭止水夹③和a的活塞,通入一段时间空气;关闭止水夹①和②,打开止水夹③和b的活塞,向C的三颈烧瓶中滴入稀硫酸。
试回答下列问题
(1)步骤1中,装置气密性良好的现象是_________;仪器a或b在使用前应________。
(2)步骤Ⅱ中,B中反应的化学方程式为________,C中H2O2的作用为_______。
(3)步骤Ⅲ中,先通入一段时间空气的目的是________,试管D中的现象为_______。
(4)步骤Ⅲ中,开始时C中反应缓慢,稍后产生气体的速率却迅速加快。试解释可能的原因_____________________。
(5)步骤II,实验前若向C三颈烧瓶中加入25mL8.0mol/LH2O2溶液反应,分离提纯得到18.88gNaClO2晶体,则H2O2的有效利用率为________(保留两位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将NaOH溶液分别加到HA、HB两种弱酸溶液中,两溶液中pH与粒子浓度比值的对数关系如图所示,已知pK=-lgKa。下列有关叙述错误的是
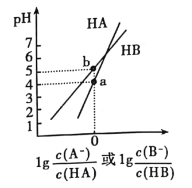
A. HA、HB两种酸中,HB的酸性弱于HA
B. b点时,c(B—)=c(HB)>c(Na+)>c(H+)>c(OH—)
C. 同浓度同体积的NaA和NaB溶液中,阴离子总数相等
D. 向HB溶液中加入NaOH溶液所得的混合溶液中![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】反应A(g)+3B(g)![]() 2C(g)+2D(g),在不同情况下测得反应速率,其反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率,其反应速率最快的是
A. υ(D)=0.4 mol / (L·s)
B. υ(C)=0.5 mol / (L·s)
C. υ(B)=0.6 mol / (L·s)
D. υ(A)=0.15 mol / (L·s)
查看答案和解析>>
科目: 来源: 题型:
【题目】VmLFe2(SO4)3溶液中含有Fe3+ag,取![]() mL溶液稀释到5VmL,则稀释后溶液中SO42﹣的物质的量浓度是
mL溶液稀释到5VmL,则稀释后溶液中SO42﹣的物质的量浓度是
A.![]() mol/LB.
mol/LB.![]() mol/L
mol/L
C.![]() mol/LD.
mol/LD.![]() mol/L
mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】2.0 molPCl3和1.0 molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:
PCl3(g)+ Cl2(g)![]() PCl5(g)达到平衡时, PCl5为0.40 mol,如果此时移走1.0 molPCl3和0.50 molCl2,在相同温度下再达平衡时 PCl5的物质的量是
PCl5(g)达到平衡时, PCl5为0.40 mol,如果此时移走1.0 molPCl3和0.50 molCl2,在相同温度下再达平衡时 PCl5的物质的量是
A. 0.40 mol B. 小于0.20 mol C. 0.20 mol D. 大于0.20 mol,小于0.40 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列反应中,单质只作氧化剂的是
A.2F2+2H2O═4HF+O2↑
B.Cl2+2NaOH═NaCl+NaClO+H2O
C.2Na+2H2O═2NaOH+H2↑
D.H2+CuO![]() H2O+Cu
H2O+Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的定容密闭容器中,当下列条件不再改变时,表明反应:A(s)+2B(g) ![]() C(g)+D(g)已达到平衡状态的现象是
C(g)+D(g)已达到平衡状态的现象是
A. 混合气体的压强 B. 混合气体的密度
C. 气体的总物质的量 D. 单位时间内生成n mol C的同时消耗2n molB
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组向一定量的NaHSO3溶液(加入少量淀粉)中加入稍过量的KIO3 溶液,一段时![]() 间后,溶液突然变蓝色。为进一步研究有关因素对反应速率的影响,探究如下。
间后,溶液突然变蓝色。为进一步研究有关因素对反应速率的影响,探究如下。
(1)查阅资料 知NaHSO3与过量KIO3反应分为两步进行,且其反应速率主要由第一步反应决定。已知第一步反应的离子方程式为IO3—+3HSO3—===3SO42—+I—+3H+,则第二步反应的离子方程式为________________。
(2)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响,记录如下。
编号 | 0.01mol/LNaHSO3溶液/mL | 0.01mol/L KIO3 溶液/mL | H2O/mL | 反应温度 /℃ | 溶液变蓝所用时间t/s |
① | 6.0 | 10.0 | 4.0 | 15 | t1 |
② | 6.0 | 14.0 | 0 | 15 | t2 |
③ | 6.0 | a | b | 25 | t3 |
实验①②是探究_______________对反应速率的影响,表中t1___________t2(填“>”、“=”或“<”);
实验①③是探究温度对反应速率的影响,表中a=_____________,b=_____________。、
(3)将NaHSO3溶液与KIO3溶液在恒温条件下混合,用速率检测仪检测出起始阶段反应速率 逐渐增大。该小组对其原因提出如下假设,请你完成假设二。
假设一:生成的SO42—对反应起催化作用;
假设二:___________________________;……
(4)请你设计实验验证上述假设一,完成下表中内容。
实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
在烧杯甲中将一定量的NaHSO3溶液与KIO3溶液混合,用速率检测仪测定起始时的反应速率v(甲) 在烧杯乙中先加入少量①_____,其他条件与甲完全相同,用速率检测仪测定起始时的反应速率v(乙) | ②若v(甲)___v(乙),则假设一不成立 ③若v(甲)___v(乙),则假设一成立 (填“>”、“=”或“<”) |
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如图所示。在0~60 s时段,反应速率v(N2O4)为____________mol·L-1·s-1;反应的平衡常数K1为________。

(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
①T________100 ℃(填“大于”或“小于”),判断理由是______________。
②列式计算温度T时反应的平衡常数K2________________________。
(3)温度T时反应达第一次平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,达到新的平衡后与第一次平衡相对比:颜色____________(填“变深”或“变浅”或“不变”),c(NO2)/c(N2O4)的值_______ (填“增大”、“减小”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com