
科目: 来源: 题型:
【题目】钛酸锂电池应用广泛, 电池放电后负极材料主要含有Li4Ti5O12、 铝箔及少量Fe, 可通过下列工艺流程回收钛、 锂。回答下列问题:
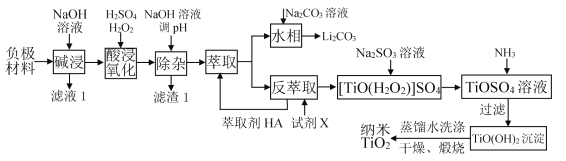
(1) Li4Ti5O12中, Ti元素的化合价为___, 滤液1中含金属的阴离子是___(填离子符号)。
(2) 酸浸时 Li4Ti5O12发生的反应是: Li4Ti5O12+7H2SO4+5H2O2=2Li2SO4+5[TiO(H2O2)]SO4+7H2O, 该反应是否属于氧化还原反应?___(填 “是” 或 “否”); 滤渣1是___。
(3) 向[TiO(H2O2)]SO4溶液中加入Na2SO3溶液发生反应的离子方程式为___。
(4) 向TiOSO4溶液中通入NH3发生反应的离子方程式为___。
(5) 沉淀TiO(OH)2用蒸馏水洗涤的目的是___。
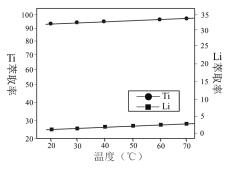
(6) 萃取时, 温度对萃取率的影响如图所示。由图分析知实验时选择在常温下进行即可, 理由是__。
(7)“萃取” 和 “反萃取” 可简单表示为:[TiO(H2O2)]2++2(HA)2![]() [TiO(H2O2)](HA2)2+2H+,则反萃取过程中加入的试剂X是___。
[TiO(H2O2)](HA2)2+2H+,则反萃取过程中加入的试剂X是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】钴、 铜及其化合物在工业上有重要用途, 回答下列问题:
(1) 请补充完基态Co的简化电子排布式: [Ar]_________, Co2+有_______个未成对电子。
(2) Na3[Co(NO2)6]常用作检验K+的试剂, 配位体NO2-的中心原子的杂化形式为________, 空间构型为_____。大π键可用符号![]() 表示, 其中m代表参与形成大π键的原子数, n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示, 其中m代表参与形成大π键的原子数, n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为![]() ),则NO2-中大π键应表示为____________。
),则NO2-中大π键应表示为____________。
(3) 配合物[Cu(En)2]SO4的名称是硫酸二乙二胺合铜(Ⅱ), 是铜的一种重要化合物。其中 En 是乙二胺(H2NCH2CH2NH2)的简写。
①该配合物[Cu(En)2]SO4中N、 O、 Cu的第一电离能由小到大的顺序是______________。
②乙二胺和三甲胺[N(CH3)3]均属于胺, 且相对分子质量相近, 但乙二胺比三甲胺的沸点高得多, 原因是______________________________________________________。
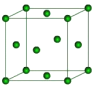
(4) 金属Cu晶体中的原子堆积方式如图所示, 其配位数为______, 铜的原子半径为a nm, 阿伏加德罗常数的值为NA, Cu的密度为_________g/cm3(列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】盐酸普鲁卡因 ( 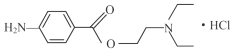 ) 是一种良好的局部麻醉药, 具有毒性小, 无成瘾性等特点。其合成路线如下图所示:
) 是一种良好的局部麻醉药, 具有毒性小, 无成瘾性等特点。其合成路线如下图所示:
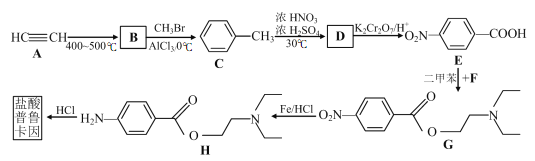
回答下列问题:
(1) 3molA可以合成1molB, 且B是平面正六边形结构, 则B的结构简式为_________。
(2) 有机物C的名称为____________, B→C的反应类型为_____________。
(3) 反应C→D的化学方程式为________________________________________。
(4) F和E发生酯化反应生成G, 则F的结构简式为___________________。
(5) H的分子式为____。
(6) 分子式为C9H12且是C的同系物的同分异构体共有__________种。
(7) 请结合上述流程信息, 设计由苯、 乙炔为原料合成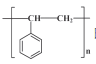 的路线_______________ 。(其他无机试剂任选)
的路线_______________ 。(其他无机试剂任选)
查看答案和解析>>
科目: 来源: 题型:
【题目】某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。

回答下列问题:
(1)写出A、B、C、D的结构简式:
A ____________,B____________C___________,D_____________。
(2)写出①②两步的化学方程式,并注明反应类型:
①__________________________________(反应类型________________)。
②_________________________________(反应类型________________)。
查看答案和解析>>
科目: 来源: 题型:
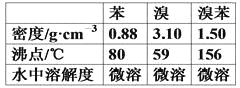
【题目】实验室合成溴苯的装置图及有关数据如下,按下列合成步骤回答:
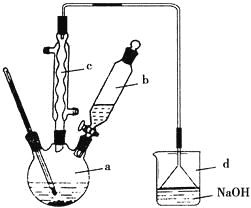
(1)实验装置中,仪器c的名称为________________,作用为_______________。
(2)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白雾产生,是因为生成了_______气体。继续滴加至液溴滴完。写出a中发生反应的化学方程式:_________________________________________。
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是____________________________________________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入无水氯化钙的目的是_______________。
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为____________,要进一步提纯,需进行的操作方法为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)按照系统命名法写出下列烷烃的名称:
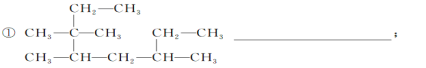 _____
_____
 ___
___
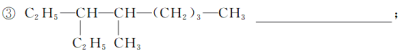 ___
___
 _____
_____
(2)根据下列有机物的名称,写出相应的结构简式:
①2,4二甲基戊烷_________________________
②2,2,5三甲基3乙基己烷__________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】以煤、石油综合利用的产品为原料合成最常用的增型剂(邻苯二甲酸二丁酯)的生产流程如图:
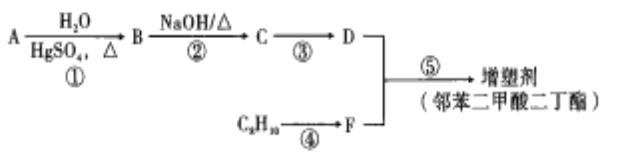
已知:
①烃A是在核磁共振氢谱中只有一组峰的直线型分子;
②R—CHO+CH3CHO![]() R—CHO+H2O;
R—CHO+H2O;
③烷基苯在高锰酸钾酸性溶液的作用下,侧链被氧化成羧基。
回答下列问题:
(1)下列说法正确的是__________(填序号)。
A.煤、石油均为常见的有机物
B.煤中含有苯和甲苯,可以用先干馏后分流的方法把它们分离出来
C.将煤在空气中加强热使之分解的过程,称为煤的干馏,也叫煤的焦化
D.石油催化裂化的过程是为了得到乙烯、丙烯、甲烷等重要化工原料
E.石油在加热和催化剂作用下,可通过结构重新调整,使链状烃转化为环状烃
(2)C8H10的名称为_______________。
(3)反应③和⑤和反应类型分别是__________、__________。
(4)写出反应⑤的化学方程式:______________________________。
(5)在F的同分异构体中,满足下列条件的共有__________种,所有的这些同分异构体中,不同化学环境氢原子的种数____________________(填“相同”和“不相同”)。
a.能与新制的Cu(OH)2悬浊液在加热的条件下反应生成砖红色沉淀
b.能与Na2CO3反应生成CO2
c.能使FeCl3溶液显色
(6)参照上述合成路线,设计一条以乙醇为原料制备1—丁醇的合成路线(无机试剂任用)。合成路线流程示例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH________________________________________________ 。
CH3CH2OH________________________________________________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(I)如图是几种烷烃的球棍模型:
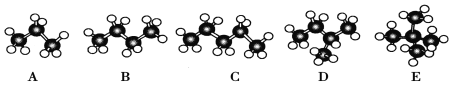
(1)A、B、E三种烷烃的关系为___________,C、D、E的关系为__________。
(2)D的名称是__________(习惯命名法)。
(3)E的一氯代物有_______种,请写出一氯代物的结构简式:________________。
(II)甲烷、乙烯、苯三种有机物中具有下列性质的是
(1)在催化剂作用下能与纯溴反应,不能使酸性高锰酸钾溶液褪色的是________。
(2)见光能跟氯气发生取代反应,不能使酸性高锰酸钾溶液褪色的是________。
(3)在催化剂作用下加氢生成乙烷,加水生成酒精的是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在现用周期表中氧族元素包括 ______________________(填元素名称)五种元素,其中Se的基态原子的电子排布式为______________________,元素X与Se同周期,X元素原子核外未成对电子数最多,X为______________________(填元素符号)。
(2)与氧同周期的相邻元素中,第一电离能有大到小的顺序______________________。
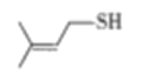
(3)臭鼬排放的臭气主要成分为3—MBT(3—甲基—2—丁烯硫醇,结构如图)。1mol3—MBT中含有σ键数目为____________(NA为阿佛加德罗常数的值)。沸点:3—MBT____________(CH3)2C==CHCH2OH(填“>”“<”或“=”),主要原因是________________________。
(4)S有+4和+6两种价态的氧化物。
①下列关于气态SO3和SO2的说法正确的是__________(填序号)。
A.中心原子的价层电子对数不相等
B.都是极性分子
C.中心原子的核对电子数目不相等
D.都含有极性键
②SO3分子的空间构型为__________,与其互为等电子体的阴离子为__________(举一例)。
(5)单质Po是有__________键形成的晶体;若已知Po的摩尔质量为Mg·mol-1,原子半径为rpm,阿伏加德罗常数的值为NA,则钋晶体的密度的表达式为____________________g·cm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】以黄铜矿(主要成分是CuFeS2)为原料炼铜的方法为火法炼铜和湿法炼铜两种。
(1)火法炼铜时产生大量SO2,根据原电池原理,稀硫酸作电解质溶液,使用惰性电极,一极通入SO2,另一极通入O2,治理SO2污染,负极反应的离子方程式为___________________________。
(2)火法炼铜的过程中,电解出铜制备精铜时产生的废电解液中含有较多Ni2+和Pb2+,从废电解液中除去Pb2+的方法是往其中通入H2S至饱和,使Pb2+转化为硫化物沉淀(已知饱和H2S溶液中c(H2S)为0.1mol/L,![]() ≈10-20;Ksp(NiS)≈10-11)。若废电解液的pH=5,为保证不生成沉淀,Ni2+浓度应控制在_________mol/L以下。
≈10-20;Ksp(NiS)≈10-11)。若废电解液的pH=5,为保证不生成沉淀,Ni2+浓度应控制在_________mol/L以下。
(3)近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐。某工厂运用该原理生产铜和绿矾(FeSO4·7H2O)的工艺如图:

①写出反应的化学反应方程式:___________________________;如果对该反应进行高温加热,发现化学反应速率降低乃至反应停止,请简述理由:___________________________。
②固体A的成分为___________________________。
③欲从滤液中获得绿矾晶体,分离操作I因为_________、_________、过滤。
④写出反应湿法炼铜的化学反应方程式:___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com