
科目: 来源: 题型:
【题目】W、X、Y、Z为原子序数依次增大的短周期主族元素,其中Y元素在同周期中离子半径最小;甲、乙分别是元素Y、Z的单质;丙、丁、戊是由W、X、Y、Z元素组成的二元化合物,常温下丁为液态;戊为酸性气体,常温下0.01mol·L-1戊溶液的pH大于2。上述物质转化关系如图所示。下列说法正确的是
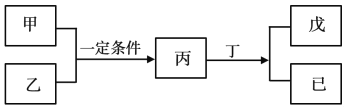
A. 原子半径:Z>Y>X>W
B. W、X、Y、Z不可能同存于一种离子化合物中
C. W和Ⅹ形成的化合物既可能含有极性键也可能含有非极性键
D. 比较X、Z非金属性强弱时,可比较其最高价氧化物对应的水化物的酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】为检验浓硫酸与木炭在加热条件下反应产生SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。

请回答下列问题:
(1)在A中发生的化学反应方程式为_____;
(2)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是_____(用操作编号填写);
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置c中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(3)若该实验中还需检测产物水蒸气,则应在C装置前添加干燥管,并在其中放置_____试剂。
(4)实验时,装置C中盛放的试剂是_____,现象时_____,可用来验证_____的存在。
(5)装置D中发生的反应方程式为_____,当D中_____现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)25℃,有pH=12的氢氧化钠溶液100mL,要使它的pH降为11.应加蒸馏水的体积为________mL;若加pH=10的氢氧化钠溶液,应加________mL.
(2)某温度下,纯水的c(H+)=3×10﹣7mol/L,Na2S和NaOH两溶液的pH均为12,则两溶液中由水电离出的c(OH﹣)的比值为 ________.
(3)已知 Na2SO4(s)+4H2(g)Na2S(s)+4H2O(g)该温度下,在2L盛有2.84g Na2SO4的密闭容器中通入H2气体,10分钟后测得固体质量为2.264g.则10分钟内H2的平均反应速率为________.
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是重要的化工产品,在基础化学试验中,有着重要的作用。
Ⅰ.物质的量浓度为18.4mol/L、质量分数为0.98的浓硫酸吸收水蒸气时,当其质量分数下降到0.87(密度1.8g/cm3)以下时,则失去干燥能力。质量分数为0.87的硫酸的物质的量浓度为_____(保留两位小数)。50mL8.4mol/L的浓硫酸作为干燥剂时,最多可吸水_____g.(保留两位小数)
Ⅱ.若用上述质量分数为0.98的硫酸,配制200mL物质的量浓度为0.46mol/L的硫酸,
(1)所需的浓硫酸的体积为_____mL,(保留一位小数)
(2)现有下列几种规格的仪器,本实验应选用_____(填序号);
①10mL量筒 ②50mL 量筒 ③100mL 量筒 ④100mL 容量瓶 ⑤200mL 容量瓶
(3)完成该实验除了烧杯外,还要的仪器有_____、_____;
(4)下列操作使所配溶液的物质的量浓度偏高的_____(填序号),对配制结果没有影响的是_____(填序号)。
a.用量筒量取浓H2SO4,慢慢地沿着玻璃棒注入盛有50mL蒸馏水的小烧杯,搅拌后,立即转移到容量瓶中。
b.往容量瓶转移溶液时,有少量液体溅出。
c.未洗涤稀释浓H2SO4的小烧杯。
d.定容时仰视。
e.容量瓶未干燥即用来配制溶液。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在常温下,有硫酸和盐酸的混合液20 mL,向该溶液中加入0.05 mol/L的Ba(OH)2时,生成的BaSO4沉淀的质量和混合溶液的pH有如图所示关系。计算:

①最初混合溶液中硫酸和盐酸的物质的量浓度。_____________
②A点溶液的pH值。_________________
(2)某温度时,Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,试求:
①在该某温度时AgCl的溶解度;(![]() =1.34,结果保留一位有效数字)_______________
=1.34,结果保留一位有效数字)_______________
②若把足量的AgCl固体分别放入①100 mL H2O ②100 mL 0.1 mol/L NaCl溶液 ③100 mL 0.1 mol/L AlCl3溶液 ④100 mL 0.1 mol/L MgCl2溶液,搅拌后溶解达到平衡,在相同温度下,求各溶液中Ag+浓度由大到小的顺序。_______________
查看答案和解析>>
科目: 来源: 题型:
【题目】一种免疫调节剂,其结构简式如图所示,关于该物质的说法不正确的是
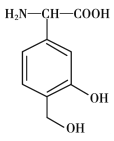
A. 属于芳香族化合物,分子式为C9H11O4N
B. 可以发生的反应类型有:加成反应、取代反应、氧化反应、聚合反应
C. 分子中所有碳原子有可能在同一平面上
D. 1mol该调节剂最多可以与3 mol NaOH反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各溶液中,微粒的物质的量浓度关系表述正确的是
A. pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等
B. 常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7
C. 将0.2 molL﹣1NaA溶液和0.1 molL﹣1盐酸溶液等体积混合所得碱性溶液中c(Na+)+c(H+)=c(A﹣)+c(Cl﹣)
D. 0.1 molL﹣1 Na2CO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-)
查看答案和解析>>
科目: 来源: 题型:
【题目】NA表示阿伏加德罗常数的值, 下列叙述正确的是
A. 1mol H2O中含有的极性共价键数目为2NA
B. 16 g16O2和18O2混合物中含有的质子数目为8NA
C. Zn和浓硫酸反应得到22.4LSO2和 H2混合气体时, 转移的电子数为4NA
D. 标准状况下2 mol NO与1 mol O2充分反应后分子数共2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某反应中反应物与生成物有:浓H2SO4、K2S、K2SO4、SO2、H2O和一种未知物质X。
(1)已知K2S在反应中失去电子,则该反应的氧化剂是_____,_____被氧化。
(2)已知0.5molK2S在反应中失去1mol电子生成X,则X的化学式为_____。
(3)按还原剂和氧化剂顺序将反应物填入下列空格中,配平,并标出电子转移的方向和数目:
![]() ___________________
___________________
(4)若反应中浓H2SO4过量,则产物中无X生成,请完成此反应的化学方程式:_____。在上述过程中,若有0.4mol浓硫酸被还原,反应中转移电子的物质的量为_____mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:H2(g)+![]() O2(g)=H2O(g) △H1
O2(g)=H2O(g) △H1
![]() N2(g)+O2(g)=NO2(g) △H2
N2(g)+O2(g)=NO2(g) △H2
![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) △H3
H2(g)=NH3(g) △H3
则反应2NH3(g)+![]() O2(g)=2NO2(g)+3H2O(g)的△H为
O2(g)=2NO2(g)+3H2O(g)的△H为
A. 2△H1+2△H2-2△H3 B. △H1+△H2-△H3
C. 3△H1+2△H2+2△H3 D. 3△H1+2△H2-2△H3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com