
科目: 来源: 题型:
【题目】标准状况下11.2LCH4在空气中完全燃烧,请完成下列问题:
(1)写出该反应的化学方程式_______;
(2)计算标准状况下11.2LCH4的质量_______;
(3)计算生成CO2的质量_______。[(2)(3)写出计算过程]
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,属于氧化还原反应的是
A. HCl+NaOH=NaCl+H2O B. Fe+CuSO4=Cu+FeSO4
C. CO2+2NaOH=Na2CO3+H2O D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子在同一溶液中一定能大量共存的是( )
A. 含大量Ba2+的溶液中:Cl-、K+、SO![]() 、CO
、CO![]()
B. 含大量H+的溶液中:Mg2+、Na+、CO![]() 、SO
、SO![]()
C. 含大量OH-的溶液中:K+、NO、SO![]() 、Cu2+
、Cu2+
D. 含大量Na+的溶液中:H+、K+、SO![]() 、NO
、NO
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学一一选修5:有机化学基础]
有机化合物K是有机合成中的一种重要的中间体,K的合成路线如下(部分产物及条件略去):

已知: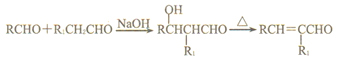
(1)A的核磁共振氢谱只有一组峰,A中官能团的名称为___________。
(2)B→C和(D+H)→K的反应类型分别是___________、___________。
(3)H的结构简式为___________。
(4)D的系统命名为___________。
(5)G→I的第①步反应方程式为___________;I→J的反应方程式为___________。
(6)同时满足下列条件的K的同分异构体有___________种(不考虑立体异构,也不包括K)。
①与K具有相同的官能团 ②分子中有一个甲基 ③具有六元碳环结构
(7)参照上述合成路线,设计一条由乙醛和乙炔为原料制备![]() 的合成路线(无机试剂任选):
的合成路线(无机试剂任选):![]() ___________。
___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
具有自主知识产权、中国制造的C919,是一款与波音737MAX同等体量的民用飞机。制造C919需要大量的合金材料,其中包括钢,钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为___________。
(2)NO3-的立体构型名称为___________,其中心原子的杂化方式为___________。
(3)C、O、Si三种元素第一电离能由大到小的顺序是___________。
(4)写出和CN-互为等电子体的一种离子的电子式___________。
(5)铵盐大多易分解,NH4F和NH4Br两种盐中较易分解的是___________(填化学式);理由是___________。
(6)氧化亚铁晶胞与NaC1的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=___________(列出计算式即可,用NA表示阿伏加德罗常数的值)。

查看答案和解析>>
科目: 来源: 题型:
【题目】25℃下,现有0.1mol·L-1的H2SO4和0.1 mol·L-1一元弱酸HA两种溶液。
(1)写出0.1 mol·L-1一元弱酸HA的电离方程式___________________。
(2)0.1mol·L-1的H2SO4中水电离出的C(H+)为_____________________。
(3)向0.1mol·L-1的硫酸中加入一定体积的pH=13的NaOH溶液,反应后溶液的pH为2,则所需NaOH溶液与硫酸的体积比为___________________;
(4)向0.1 mol·L-1一元弱酸HA加入一定体积的水,在此过程中,下列数值变大的是_________________。
①c(H+) ②n(A-) ③c(OH-) ④ Ka ⑤c(A-)/ c(HA)
(5)实验室在配制溶液时,一些物质存在水解的情况,在配制Fe2(SO4)3溶液时,Fe3+也存在水解,请书写水解离子方程式____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.现用物质的量浓度为0.100 0 mol·L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:
(1)从下表中选出正确选项______________

(2)某学生的操作步骤如下:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴部分充满溶液;
D.取标准NaOH溶液注入碱式滴定管至“0”刻度以上 2~3 mL;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是____→___→___→___→A→___(用字母序号填写)______________。判断到达滴定终点的实验现象是_____________________________________。
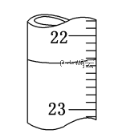
(3)若滴定达终点时,滴定管中的液面如上图所示,正确的读数为__________
A.22.30 mL B.23.65 mL
C.22.35 mL D.23.70 mL
(4)由于错误操作,使得上述所测盐酸溶液的浓度偏高的是________(填字母)。
A.中和滴定达终点时俯视滴定管内液面读数
B.酸式滴定管用蒸馏水洗净后立即取用25.00 mL待测酸溶液注入锥形瓶进行滴定
C.碱式滴定管用蒸馏水洗净后立即装标准溶液来滴定
D.用酸式滴定管量取待测盐酸时,取液前有气泡,取液后无气泡
(5)滴定结果如下表所示:
滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 20.00 | 1.02 | 21.03 |
2 | 20.00 | 2.00 | 21.99 |
3 | 20.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010 mol/L,则该样品的浓度是________________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮和氮的化合物在国防建设、工农业生产和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)NaCN广泛用于电镀工业上,实验测得浓度相同的NaCN溶液和NaHCO3溶液,前者的pH大,则酸性:HCN___________H2CO3(填“强于”或“弱于”)。
(2)亚硝酰氯(结构式为Cl-N=O)是有机合成中的重要试剂。它可由C12和NO在通常条件下反应制得,反应方程式为:2NO(g)+Cl2(g)![]() 2ClNO(g)。已知几种化学键的键能数据如下表:
2ClNO(g)。已知几种化学键的键能数据如下表:
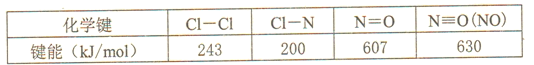
当Cl2与NO反应生成ClNO的过程中转移了5mol电子,理论上热量变化为___________kJ。
(3)在一个恒容密闭容器中充入2 mol NO(g)和1molCl2(g)发生(2)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示:

①T1___________T2(填“>”“≤”或“=”),理由是___________。
②若容器容积为1L,温度为T1℃时,反应开始到5min时,C12的平均反应速率为_______。
③温度为T2℃时,在相同容器中,充入1 molNO(g)和0.5mo1Cl2(g),则NO的平衡转化率___________50%(填“大于”、“等于”或“小于”)
④温度为T2℃时,起始时容器内的压强为p0,则该反应的平衡常数Kp=___________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-),其工作原理如图所示:
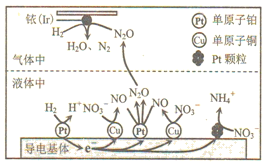
①Ir表面发生反应的方程式为___________。
②若导电基体上的Pt颗粒增多,造成的结果是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在一个容积为2 L 的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:
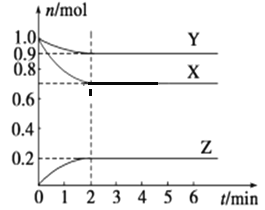
(1)该反应的化学方程式为:______________________。
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=____________。
(3)1min时,正逆反应速率的大小关系为:v正____________v逆(填“>”、“<”或“=”);4min时,v正____________v逆(同前);若X、Y、Z均为气体,反应达到平衡时:若此时将容器的体积缩小为原来的1/2倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________反应(填“放热”或“吸热”)。
(4)上述反应在t1~t6内反应速率与时间图像如图,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是____________。

A.在t1时增大了压强
B.在t3时加入了催化剂
C.在t4时降低了温度
D.t2~t3时X的转化率最高
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铜(CuC1)是有机合成中应用广泛的催化剂。它微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化,但在干燥的空气中稳定,见光会分解。实验室制备氯化亚铜的过程如下:
Ⅰ.检査下图装置气密性,依次向三颈瓶中加入铜丝、氯化氨、硝酸、盐酸,关闭K;
Ⅱ.加热至50℃时停止加热,铜丝表面产生无色气泡,液面上方气体逐渐变为红棕色,气囊鼓起;
Ⅲ.打开K,通入氧气,待气囊变瘪、瓶内红棕色气体消失时关闭K,冷却至室温,制得NH4[CuCl2];
Ⅳ.将液体转移至烧杯中用足量蒸馏水稀释,产生白色沉淀,过滤得氯化亚铜粗品和滤液;
V.粗品用95%乙醇洗涤、烘干得氯化亚铜。
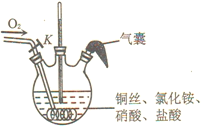
请回答下列问题:
(1)实验室中CuC1的保存方法是___________。
(2)实验开始时,温度计显示反应液温度低于室温,主要原因是___________。
(3)通入氧气的目的是___________。为便于观察和控制产生O2的速率,制备氧气的装置最好选用___________(填字母)
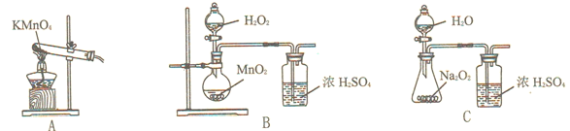
(4)三颈瓶中生成NH4[CuCl2]的总反应的离子方程式为_______。步骤Ⅳ中产生白色沉淀的化学方程式为_______。
(5)步骤V中洗涤时试剂选用95%乙醇的原因是___________。
(6)CuCl纯度测定:称取样品0.25g置于预先放入玻璃珠30粒和10mL过量的FeCl3溶液的锥形瓶中,不断摇动;待样品溶解后,加水50mL和指示剂2滴;立即用0.10mol·L-1硫酸铈标准溶液滴定至终点并记录读数,再重复实验两次,测得数据如下表。(已知:CuC1+FeCl3=CuCl2+FeCl2,Fe2++Ce4+=Fe3++Ce3+)

①玻璃珠的作用是___________。
②CuCl的纯度为___________(保留三位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com