
科目: 来源: 题型:
【题目】苯氧布洛芬钙G是评价较好的解热、镇痛、消炎药,下面是它的一种合成路线(具体反应条件和部分试剂略)
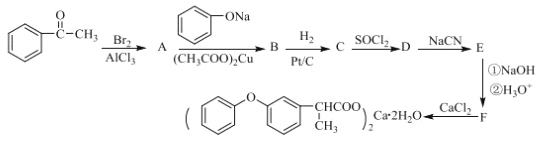
已知:
①氯化亚砜(SOCl2)可与醇发生反应,醇的羟基被氯原子取代而生成氯代烃。
②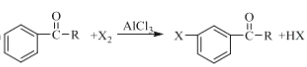 (X表示卤素原子)
(X表示卤素原子)
回答下列问题:
(1)写出D的结构简式:________________。F 中所含的官能团名称是___________。
(2)B→C的反应类型是_______________;D→E的反应类型是_______________。
(3)写出F和C在浓硫酸条件下反应的化学方程式__________________________。
(4)写出A的符合以下条件同分异构体的所有结构简式______________________。
①属于苯的二取代物;
②苯环上核磁共振氢谱图中共有2个吸收峰
③与FeCl3溶液发生显色反应。
(5)结合上述推断及所学知识,参照上述合成路线任选无机试剂设计合理的方案,以苯甲醇(![]() )为原料合成苯乙酸苯甲酯(
)为原料合成苯乙酸苯甲酯(![]() )写出合成路线,并注明反应条件_________________。
)写出合成路线,并注明反应条件_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知可逆反应2SO2+ O22SO3,当生成2 mol SO3时放出热量为Q,现将1 mol SO2和0.5 mol O2在相同条件下反应生成SO3放出的热量为Q1,则
A.Q1=![]() QB.Q1<
QB.Q1<![]() QC.2Q1>QD.无法判断
QC.2Q1>QD.无法判断
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在实验室浓盐酸和二氧化锰加热条件下可以反应生成氯化锰和Cl2等,某同学用此法制得标准状况下Cl2体积为22.4mL,据题意回答下列问题:
(1)写出其化学反应方程式并配平____________
(2)请计算共消耗MnO2多少克?_____________
(3)上述实验所用浓盐酸,其质量分数为36.5%,密度为1.19g/mL,为了使用方便,请计算该浓盐酸的物质的量浓度为多少?_______________
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用18.4molL-1的浓硫酸来配制480mL0.2molL-1的稀硫酸。可供选用的仪器有:①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有___(选填序号),还缺少的仪器有(写仪器名称)___。
(2)需要用量筒量取上述浓硫酸的体积为___mL,量取浓硫酸时应选用___(选填①10mL②50mL③100mL)规格的量筒。
(3)实验中两次用到玻璃棒,其作用分别是:___、___。
(4)下列对容量瓶及其使用方法的描述中正确的是___。
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后,必须烘干
C.配制溶液时,把量好的浓硫酸小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2cm处,改用胶头滴管加蒸馏水至刻度线
D.使用前要检查容量瓶是否漏水
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有___(填序号)
①未洗涤稀释浓硫酸时用过的烧杯和玻璃棒
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,仰视刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】已知常温下,Ksp(AgCl)=1×10-10,Ksp(AgI)=1×10-18。下列叙述中正确的是( )
A. 常温下,AgCl在NaCl溶液中的Ksp比在纯水中的Ksp小
B. 常温下,AgI若要在NaCl溶液中开始转化为AgCl,则NaCl的浓度必须大于0.1mol·L
C. 将0.001 mol·L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先析出AgI沉淀
D. 向AgCl饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-)
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年国庆阅兵上,新一代预警机、无人机、东风![]() 战略核导弹等一批国产武器装备精彩亮相、震撼人心。它们不仅是捍卫国家安全和民族尊严的利器,更是我们每个中国人幸福生活的保障。导弹、装备的制造和化学密不可分,请配平下列方程式:
战略核导弹等一批国产武器装备精彩亮相、震撼人心。它们不仅是捍卫国家安全和民族尊严的利器,更是我们每个中国人幸福生活的保障。导弹、装备的制造和化学密不可分,请配平下列方程式:
(1)______![]() ______
______![]() ______
______![]() ______
______![]() ______
______![]() ______
______![]()
(2)______![]() ______
______![]() ______S↓______
______S↓______![]() ______
______![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】无论以何种比例混合的10mL混和气,在50mL的氧气中燃烧生成CO2和液态的H2O,燃烧后所得气体的体积为35mL,则该混合物可能为
A. C3H6 C4H6 B. C2H6 C3H6
C. C2H4 C3H8 D. C2H2 C2H6
查看答案和解析>>
科目: 来源: 题型:
【题目】1500C、1.0×105Pa时,aL乙炔,aL甲烷和aL丙烯的混合气体与过量的bLO2混合,点燃使这两种烃充分燃烧后,再恢复到原状况,此时混合气体的体积为
A. 10aL B. (3a+b)L C. (b-a)L D. 无法计算
查看答案和解析>>
科目: 来源: 题型:
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18g/cm3,沸点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用如图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液。试管d中装有浓溴水(表面覆盖少量水)。
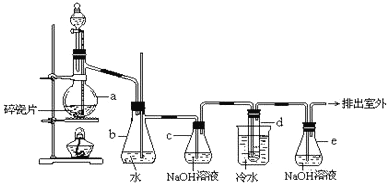
请填写下列空白:
(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速升高到170℃,否则容易发生副反应。请写出乙醇发生消去反应的方程式 ____________。
(2)写出制备1,2-二溴乙烷的化学方程式:____________。
(3)安全瓶b可以防止倒吸,并可以检査实验进行时试管d是否发生堵塞,请回答发生堵塞时瓶b中的现象:___________________。
(4)容器c中NaOH溶液的作用是:_________________。
(5)若产物中有少量副产物乙醚,可用_______________________的方法除去;
(6)反应过程中应用冷水冷却装置d,其主要目的是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com