
科目: 来源: 题型:
【题目】已知反应:CH2=CHCH3(g)+Cl2(g)![]() CH2=CHCH2Cl(g)+HCl(g)。在一定压强下,按
CH2=CHCH2Cl(g)+HCl(g)。在一定压强下,按![]() 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(![]() )与温度(T)、
)与温度(T)、![]() 的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的是
的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的是

A. 图甲中![]()
B. 若在恒容绝热装置中进行上述反应,达到平衡时,装置内的气体压强将不变
C. 温度T1、![]() , Cl2的转化率约为33.3%
, Cl2的转化率约为33.3%
D. 图乙中,线A表示正反应的平衡常数
查看答案和解析>>
科目: 来源: 题型:
【题目】用三个集气瓶收集满二氧化硫、二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量O2或Cl2,如图所示。一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余。(假设瓶内液体不扩散)

(1)写出装置E中反应的离子方程式:__________________________________________
(2)假设该实验条件下,气体摩尔体积为aL·mol-1。则装置D的集气瓶中所得溶液溶质的物质的量浓度为____________;发生反应的方程式____________________________。
(3)通入氧气前在F装置的水槽里滴加几滴紫色石蕊溶液,观察到的现象是_____________,通入氧气后,可能观察到的实验现象是_________________________________________,写出反应的总化学方程式:_________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应,H2(g)+I2(g)=2HI(g)△H<0(用“加快”、“减慢”、“不变”填空)
(1)保持容器容积不变,向其中加入1molH2,反应速率_________
(2)保持容器容积不变,向其中加入1molN2(N2不参加反应),反应速率________
(3)保持容器内压强不变,向其中加入1molN2(N2不参加反应),反应速率______
(4)保持容器内气体压强不变,向其中加入1molH2(g)和1molI2(g),反应速率______
(5)提高起始的反应温度,反应速率___________
(6)830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0若起始时c(CO)=2molL-1,c(H2O)=3molL-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=_________
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.将气体A、B置于容积为2L的密闭容器中,发生如下反应:4A(g)+B(g)2C(g),反应进行到4s末,测得A为0.5mol,B为0.4mol,C为0.2mol。则:
(1)用生成物C浓度的增加来表示该反应的速率应为________________ mol/(Ls);
(2)用反应物A浓度的减少来表示该反应的速率应为_________________ mol/(Ls);
(3)用反应物B浓度的减少来表示该反应的速率应为_________________ mol/(Ls)。
Ⅱ.恒温恒容下,将2 mol A气体和2 mol B气体通入体积为2 L的密闭容器中发生如下反应:2A(g)+B(g) xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为______________。
(2)x=_______________。
(3)下列各项不可作为该反应达到平衡状态的标志的是______________。
A.压强不再变化
B.气体密度不再变化
C.A的消耗速率与B的消耗速率之比为2:1
D.A的百分含量保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】在混合导体透氧膜反应器中一步同时制备氨合成气(N2、H2)和液体燃料合成气(CO、H2),其工作原理如图所示,下列说法错误的是
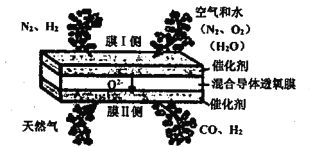
A. 膜I侧反应为: H2O+2e-=H2+O2- O2+4e-=2O2-
B. 膜II侧相当于原电池的负极
C. 膜II侧发生的反应为:CH4+O2--2e-=2H2+CO
D. 膜II侧每消耗1molCH4,膜I侧一定生成1mol H2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A. 用牺牲阳极的阴极保护法保护船舶时,将船舶与石墨相连
B. 往含硫酸的淀粉水解液中,先加氢氧化钠溶液,再加碘水,检验淀粉是否水解完全
C. 反应3Si(s)+2N2(g)=Si3N4(s)能自发进行,则该反应的△H<0
D. 已知BaSO4的Ksp= (Ba2+ )·c(SO42-),所以BaSO4在硫酸钠溶液中溶解达到饱和时有c(Ba2+)=c(SO42-)=![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】含镍(Ni)质量分数约20%废料,主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍,工艺流程如下:
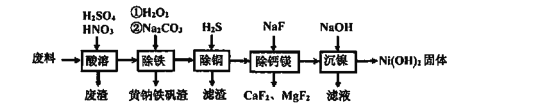
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,反应有N2生成。写出金属镍溶解的化学方程式______________________
(2)“除铁”时H2O2的作用是________________,为了证明添加的H2O2已足量,应选择的试剂是_______________ (填序号:“①铁氰化钾K3[Fe(CN)6]”或“②硫氰化钾KSCN”)溶液.黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点,则x:y:m:n=1:____:2:6
(3)“除铜”时,反应的离子方程式为________________
(4)已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF“除钙镁”后,所得滤液中![]() ________________(保留1位小数)。已知除杂过程在陶瓷容器中进行,NaF的实际用量不宜过大的原因是__________
________________(保留1位小数)。已知除杂过程在陶瓷容器中进行,NaF的实际用量不宜过大的原因是__________
(5)100kg废料经上述工艺制得Ni(OH)2固体的质量为31kg,则镍回收率为______________(保留1位小数)
(6)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:M+Ni(OH)2![]() MH+NiOOH(式中M为储氢合金)。写出电池充电过程中阳极的电极反应式___________
MH+NiOOH(式中M为储氢合金)。写出电池充电过程中阳极的电极反应式___________
查看答案和解析>>
科目: 来源: 题型:
【题目】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程为_________________________,工艺师常用____________(填物质名称)来雕刻玻璃,其所对应的方程式为___________
(2)用Na2SiO3溶液浸泡过的棉花不易燃烧,则Na2SiO3可作生产_______________的原料。
(3)工业上常用2C+SiO2![]() Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是____________(填化学式,下同),氧化剂是________________。
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是____________(填化学式,下同),氧化剂是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)1molN2(g)与适量O2(g)起反应生成NO2(g),吸收68 kJ热量。_______________________。
(2)1molCu(s)与适量O2(g)起反应生成CuO(s),放出157 kJ热量。________________________。
(3)卫星发射时可用(N2H4)作燃料,1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622 kJ热量___。
(4)汽油的重要成分是辛烷(C8H18),1molC8H18(l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出5 518 kJ热量。______________________________。
(5)1molC(s)与适量H2O(g)起反应生成CO(g)和H2(g),吸收131.5kJ热量。_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】11.2 g铁粉与2.2 g硫粉均匀混合,在密闭容器中加热,冷却后加入足量盐酸,在标准状况下收集到气体的体积是( )
A. 11.2 L B. 5.6 L C. 4.48 L D. 2.24 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com