
科目: 来源: 题型:
【题目】低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是
2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是
A. 其他条件不变,使用高效催化剂,会缩短反应时间且废气中氮氧化物的转化率增大
B. 其他条件不变,加入足量的NH3,再次平衡后氮氧化物的转化率增大,氮气的体积分数减小
C. 其他条件不变,升高温度会提高反应物的转化率且使该反应的平衡常数增大
D. 其他条件不变,缩小容器的体积会使平衡正向移动,再次平衡后氨气的浓度变小
查看答案和解析>>
科目: 来源: 题型:
【题目】某混合物浆液含Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见下图),使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答I和II中的问题。
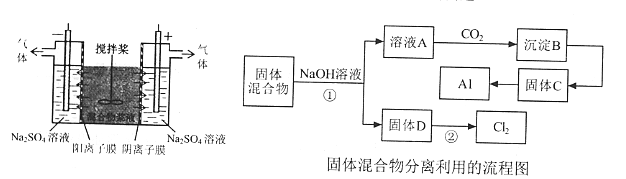
I.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)Cl在元素周期表中的位置为_____,CO2的电子式为___,NaOH中存在的化学键类型为_____。
(2)B-C的反应条件为_____,C→Al的制备反应化学方程式为__________。
(3)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化:加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)______。
a.温度 b.Cl的浓度 c.溶液的酸度
II.含铬元素溶液的分离和利用
(4)用情性电极电解时,CrO42-能从浆液中分离出来的原因是____,分离后含铬元素的粒子是____;阴极室生成的物质为_______(写化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】将下列物质进行分类(填序号)
①O2与O3
②126C与136C
③白磷与红磷
④冰与水
⑤H2、D2、T2
⑥乙醇与二甲醚
⑦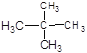 和
和![]()
(1)互为同位素的是_____________
(2)互为同素异形体的是___________
(3)互为同分异构体的是_________
(4)属于同一化合物的是___________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)根据结构对有机物进行分类,有助于对其性质的掌握。
①下列有机物中属于芳香烃的是________(填字母),它与苯的关系是________,写出苯与溴发生反应的化学方程式:__________________________。
预测该芳香烃________(填“能”或“不能”)发生该类反应。
![]()
②下列有机物中属于羧酸类的是________(填字母)。
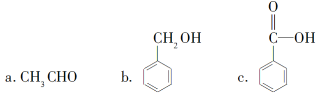
③下列有机物中属于糖类的是________(填字母)。
a.油脂 b.纤维素 c.蛋白质
(2)化合物X的结构简式为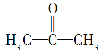 。
。
①一个X分子中有________种等效氢原子。
②X的一种同分异构体Z的结构简式为H2C===CH—CH2OH,请写出Z与Br2发生加成反应的化学方程式: ______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述中,不正确的是( )
A. 淀粉![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B. 纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C. 油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D. 蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:下列描述正确的是

A. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B. 平衡时的压强是起始压强的1.2倍
C. 反应开始到10s时,Y的转化率为79.0%
D. 反应的化学方程式为:X(g)+ Y(g)![]() Z(g)
Z(g)
查看答案和解析>>
科目: 来源: 题型:
【题目】向足量H2SO4溶液中加入100mL0.4mol·L-1Ba(OH)2溶液,放出的热量是5.12kJ。如果向足量Ba(OH)2溶液中加入100mL0.4mol·L-1HCl溶液时,放出的热量为2.2kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为
A. Ba2+(aq)+SO42-(aq)![]() BaSO4(s) △H=-2.92 kJ·mol-1
BaSO4(s) △H=-2.92 kJ·mol-1
B. Ba2+(aq)+SO42-(aq)![]() BaSO4(s) △H=-0.72 kJ·mol-1
BaSO4(s) △H=-0.72 kJ·mol-1
C. Ba2+(aq)+SO42-(aq)![]() BaSO4(s) △H=-18 kJ·mol-1
BaSO4(s) △H=-18 kJ·mol-1
D. Ba2+(aq)+SO42-(aq)![]() BaSO4(s) △H=-73 kJ·mol-1
BaSO4(s) △H=-73 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。请回答下列问题:
(1)晒制蓝图时,用)K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3![]() ]2FeC2O4+3K2C2O4+2CO2↑:显色反应的化学反应式为___FeC2O4+___K3[Fe(CN)6]一___Fe3[Fe(CN)6]2+_______,配平并完成该显色反应的化学方程式。
]2FeC2O4+3K2C2O4+2CO2↑:显色反应的化学反应式为___FeC2O4+___K3[Fe(CN)6]一___Fe3[Fe(CN)6]2+_______,配平并完成该显色反应的化学方程式。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
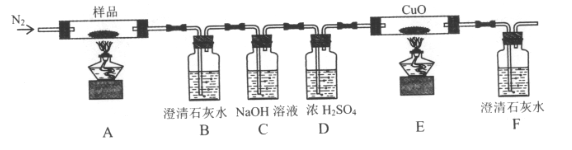
①通入氮气的目的是_________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有______________,_____________。
③为防止倒吸,停止实验时应进行的操作是______________。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:______________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1KMnO4,溶液滴定至终点。在滴定管中装入KMnO4溶液的前一步,应进行的操作为____。滴定终点的现象是__________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为_____________________。若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,则测定结果_____________________。
③过滤、洗涤实验操作过程需要的玻璃仪器有__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】砷(As)与氮同一主族,As原子比N原子多两个电子层。可以形成As2S3、As2O5、H3AsO3、H3AsO4,等化合物,有着广泛的用途。回答下列问题:
(1)As的原子序数为______________________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式____________。该反应需要在加压下进行,原因是___________。
(3)己知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s)
H2(g)+2O2(g)=H3AsO4(s) ![]()
H2(g)+![]() O2(g)=H2O(l)
O2(g)=H2O(l) ![]()
2As(s)+![]() O2(g)=As2O5(s)
O2(g)=As2O5(s) ![]()
则反应As2O5(s)+3 H2O(l)=2 H3AsO4(s)的![]() =______________________。
=______________________。
(4)298K肘,将2OmL 3xmol·L-1 Na3AsO3、20m L3xmol·L-1 I2和20 mL NaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-![]() AsO43-(aq) +2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq) +2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
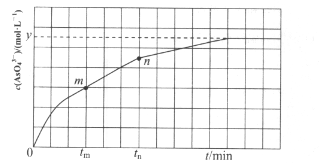
①下列可判断反应达到平衡的是_____(填标号)。
a.v(I-)=2v(AsO33-) b.溶液的pH不再变化
c.c(I-)=ymol·L-1 d.c(AsO43-)/c(AsO33-)不再变化
②tm时,v正____v逆(填“大于”、“小于”或“等于”)。
③) tm时v逆____tn时v逆(填“大于”、“小于”或“等于”),理由是___________。
④若平衡时溶液的pH=14,则该反应的平衡常数为_____(用x、y表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各表述与示意图一致的是
A. 
25℃时,用0.1mol·L-1盐酸滴定20mL 0.1mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
B. 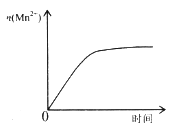
10mL 0.01mol·L-1 KMnO4酸性溶液与过量的0.1mol·L-1 H2C2O4溶液混合时,n(Mn2-)随时间的变化
C. 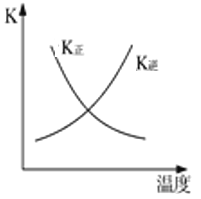
曲线表示反应2SO2(g)+O2(g) ![]() 2SO3(g) △H<0 正、逆反应的平衡常数K随温度的变化
2SO3(g) △H<0 正、逆反应的平衡常数K随温度的变化
D. 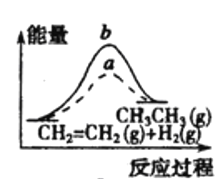
a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g) △H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com