
科目: 来源: 题型:
【题目】ClO2 与 Cl2 的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小 组通过图1 装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
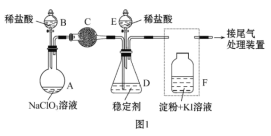
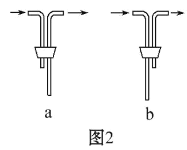
(1)仪器 D 的名称是___________。安装 F 中导管时,应选用图2中的___________。
(2)打开 B 的活塞,A 中发生反应:2NaClO3+4HCl![]() 2ClO2↑+Cl2↑+2NaCl+2H2O。为使 ClO2 在 D 中被稳定剂充 分吸收,滴加稀盐酸的速度宜___________ (填“快”或“慢”)。
2ClO2↑+Cl2↑+2NaCl+2H2O。为使 ClO2 在 D 中被稳定剂充 分吸收,滴加稀盐酸的速度宜___________ (填“快”或“慢”)。
(3)关闭 B 的活塞,ClO2 在 D 中被稳定剂完全吸收生成 NaClO2,此时 F 中溶液的颜色不变,则装置 C 的作用是___________ 。
(4)已知在酸性条件下 NaClO2 可发生反应生成 NaCl 并释放出 ClO2,该反应的离子方程式为___________,在 ClO2 释放实验中,打开 E 的活塞,D 中发生反应,则装置 F的作用是___________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】苯环结构中,不存在单双键交替结构,可以作为证据的事实是( )
①苯不能使酸性 KMnO4 溶液褪色②苯分子中碳原子间的距离均相等 ③苯能在一定条件下跟 H2 加成生成环己烷④经实验测得间二甲苯仅一种结构 ⑤苯在 FeBr3 存在条件下与液溴发生取代反应,但不因化学变化而使溴水褪色
A.②③⑤B.①②④⑤C.①②⑤D.①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献,他以饱和食盐水、NH3、CO2为原料先制得NaHCO3,进而生产出纯碱。回答下列问题:
某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计方案实验。一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。

(1)乙装置中的试剂是_________________。
(2)另一位同学用图中戊装置(其他装置未画出)进行实验。实验时,须先从____________管通入________气体。
(3)有同学建议在戊装置的b管下端连接己装置,理由是____________________。
(4)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100 g 水):
0 ℃ | 10 ℃ | 20 ℃ | 30 ℃ | 40 ℃ | 50 ℃ | |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析丙、戊装置中使用冷却水或者冰水的原因:____________。
(5)该小组同学为了测定丙中所得晶体的碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为a g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行下图所示实验:

①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是___________(填字母)。
a 在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
b 在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
c 在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②所得晶体中碳酸氢钠的纯度为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是
A. 用惰性电极电解MgCl2 溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B. 向氯化铝溶液中滴加少量Na2CO3溶液:2Al3++3CO32-=Al2(CO3)3↓
C. 一定量明矾溶液中滴加Ba(OH)2溶液至沉淀的质量最大时:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O
D. FeCl3溶液与NaAlO2溶液混合:Fe3++ 3AlO2-=Fe(AlO2)3↓
查看答案和解析>>
科目: 来源: 题型:
【题目】符合分子式“C6H6”的多种可能结构如图所示,下列说法正确的是
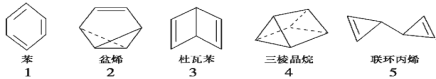
A.1~5 对应的结构中所有原子均可能处于同一平面的有 1 个
B.1~5 对应的结构中一氯取代物只有 1 种的有 3 个
C.1~5 对应的结构中能使溴的四氯化碳溶液褪色的有 4 个
D.1~5 对应的结构均能与氢气在一定条件下发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】二氯化二硫(S2Cl2)是一种常用于橡胶硫化、有机物氯化的试剂,甲同学查阅资料:①将干燥的氯气在110~140 ℃ 间与硫反应,即可得S2Cl2粗品;②有关物质的部分性质如表所示:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77 | 137 | ①一种橙黄色的液体,遇水易水解,有淡黄色固体出现,同时产生能使品红溶液褪色的气体。 ②300 ℃以上完全分解。③S2Cl2+Cl2=2SCl2 |
设计如图所示实验装置在实验室合成S2Cl2:
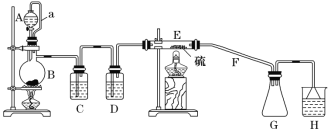
回答以下问题:
(1)仪器A的名称是_______________。
(2)B中所发生反应的离子方程式为___________________________________。
(3)C装置的作用是___________________________________ 。
(4)S2Cl2粗品中可能混有的杂质是_______________ (写其中一种,填化学式)。
(5)乙同学发现,该装置中除了E处的温度不能过高外,还有一处重大缺陷需改进,否则会导致S2Cl2的产率大大降低,原因是______________________________ (用化学方程式表示);请简要提出改进方案:________________________________________________。
(6)H中的溶液可以选择下列试剂中的__________ (填字母)。
A 碳酸钠溶液 B 氯化铁溶液 C 高锰酸钾溶液 D 亚硫酸钠溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干种离子,离子浓度均为0.1mol/L,某同学进行了如下实验:

下列说法正确的是
A. 无法确定原试液中是否含有Al3+、Cl-
B. 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C. 原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-
D. 无法确定沉淀C的成分
查看答案和解析>>
科目: 来源: 题型:
【题目】四元轴烯 t、苯乙烯 b 及立方烷 c 的分子式均为 C8H8。下列说法正确的是( )

A. b 的同分异构体只有 t 和 c 两种
B. t 和b 能使酸性 KMnO4 溶液褪色而c不能
C. t、b、c 的二氯代物均只有三种
D. t、b、c 中只有 t 的所有原子可以处于同一平面
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,V mL不饱和NaNO3溶液a g,蒸发掉b g水或加入b g NaNO3固体(恢复到原温度)均可使溶液达到饱和,则下列各量的计算结果正确的是( )
A. 该温度下NaNO3的溶解度为50 g
B. 原不饱和溶液的密度为![]() g·mL-1
g·mL-1
C. 原不饱和溶液中NaNO3的质量分数为![]() %
%
D. 原不饱和溶液中NaNO3的物质的量浓度为![]() mol·L-1
mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 最外层电子数是次外层电子数的2倍 |
X | L层有三个未成对电子 |
Y | L层p电子数比s电子数多两个 |
Z | 元素的最高正价为+7价 |
下列说法正确的是
A. Z离子的结构示意图为:![]()
B. 分子TY2中各原子均满足8电子稳定结构
C. T元素在周期表中的表示为:
D. XZ3含有非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com