
科目: 来源: 题型:
【题目】(1)下列氮原子的电子排布图表示的状态中,能量由低到高的顺序是_______(填字母代号)。

(2)P4S3可用于制造火柴,其分子结构如图所示。
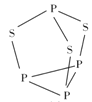
①P4S3分子中硫原子的杂化轨道类型为_______________。
②每个P4S3分子中含有的孤电子对的数目为__________________。
(3)科学家合成了一种阳离子“N5n+,其结构是对称的,5个N排成"V"形,每个N都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”的化学式为”N8”的离子晶体,其电子式为_________________。分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子的最外层均满是8电子稳定结构,其结构式为_____。
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为_________________。
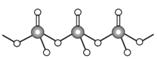
(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径
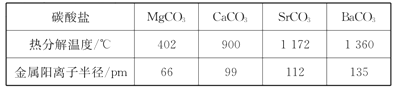
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是_______________。
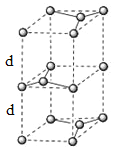
(6)石墨的晶体结构和晶胞结构如下图所示。已知石墨的密度为pgcm3,C—C键的键长为![]() cm,阿伏加德罗常数的值为NA,则石墨品体的层间距为_________cm。
cm,阿伏加德罗常数的值为NA,则石墨品体的层间距为_________cm。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙各取300mL同浓度的盐酸,加入不同质量的同一镁铝合金粉末进行下列实验,有关数据列表如下:
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 510 | 765 | 918 |
(标准状况)气体体积/mL | 560 | 672 | 672 |
求:(1)盐酸的物质的量浓度是多少___?
(2)合金中镁铝的质量分数各是多少___、___?
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)200mL2mol/L的Al2(SO4)3溶液中SO42-的物质的量浓度为___;
(2)标准状况下,36gH2和O2组成的混合气体的体积是67.2L,则混合气体中H2和O2的体积比为___;
(3)标准状况下,将33.6LNH3溶于水配成500mL溶液,该溶液的物质的量浓度为___;
(4)已知1.505×1023个A气体分子的质量为31g,则A气体的摩尔质量是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是
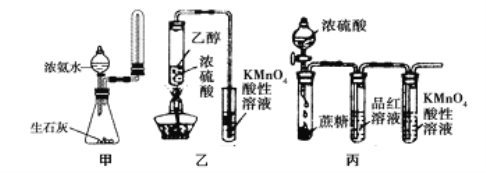
A. 实验室用图甲所示装置制取少量氨气
B. 为使100mL0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50mL水
C. 利用图乙装置,可制取乙烯并验证其易被酸性KMnO4溶液氧化
D. 利用图丙装置,可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
科目: 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用。不仅可以提高经济效益,而且还能防止环境污染,生产流程如下:

已知石油裂解已成为生产C的主要方法,E的溶液能发生银镜反应,G是具有果香味的液体,试填空:
(1) B的名称:_________________;D中官能团的名称:___________________。
(2) 写出C发生加聚反应的方程式:___________________。
(3) D→E的化学方程式:_____________________;F→G的化学方程式:_____________________。
(4)已知HCOOCH3也具有果香味,则该物质与G的关系互称为_________________,与F的关系互称为:_________________。
下图为实验室制取G的装置图,图中a试剂名称为________________,实验结束后分离a和G的方法为_________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
I. 分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况下),则该物质的实验式是__________.
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为__________,该物质的分子式是__________.
(3)根据价键理论,预测A的可能结构并写出结构简式__________.
II.结构式的确定:
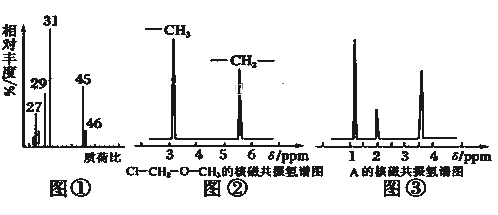
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl﹣CH2﹣O﹣CH3)有两种氢原子如图②.经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________.
查看答案和解析>>
科目: 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是___。
(2)反应①的化学方程式为___。
(3)反应③的离子方程式为___。
(4)反应⑧的化学方程式为___。
(5)反应⑥过程中的现象是____。
(6)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占___L。
查看答案和解析>>
科目: 来源: 题型:
【题目】配制100 mL0.020mol/L KMnO4溶液的过程如下图所示:
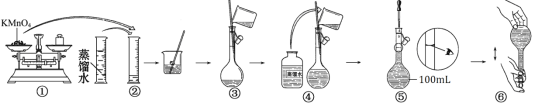
回答下列问题:
(1)图示中有两步操作不正确,它们是_____和_____ (填序号)。
(2)操作⑤图示中的两种仪器分别是________、 __________(填名称)。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将_______(填“偏大”或“偏小”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】中科院大连化学物理研究所的一项最新成果实现了甲烷高效生产乙烯,如图所示,甲烷在催化作用下脱氢,在不同温度下分别形成![]() 等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)
等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)

(1)已知相关物质的燃烧热如上表所示,写出甲烷制备乙烯的热化学方程式______________。
(2)现代石油化工采用Ag作催化剂,可实现乙烯与氧气制备X(分子式为C2H4O,不含双键)该反应符合最理想的原子经济,则反应产物是____________(填结构简式)。
(3)在400℃时,向初始体积为1L的恒压密闭反应器中充入1 molCH4,发生(1)中反应,测得平衡混合气体中C2H4的体积分数为20.0%。则:
①在该温度下,其平衡常数K=________。
②若向该反应器中通入高温水蒸气(不参加反应,高于400℃),则C2H4的产率将_______(填“増大”“减小”“不变”或“无法确定”),理由是__________________________________。
③若反应器的体积固定,不同压强下可得变化如下图所示,则压强的关系是____________。

④实际制备C2H4时,通常存在副反应2CH4(g)![]() C2H6(g)+H2(g)。反应器和CH4起始量不変,不同温度下C2H6和C2H4的体积分数与温度的关系曲线如下图所示。
C2H6(g)+H2(g)。反应器和CH4起始量不変,不同温度下C2H6和C2H4的体积分数与温度的关系曲线如下图所示。

I.在温度高于600℃时,有可能得到一种较多的双碳有机副产物的名称是____________。
II.若在400℃时,C2H4、C2H6的体积分数分别为20.0%、6.0%,其余为CH4和H2,则体系中CH4的体积分数是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了将混有Na2SO4、NaHCO3的NaCl固体提纯,制得纯净的氯化钠溶液,某学习小组设计了如下图所示的实验方案:
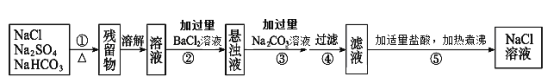
回答下列问题:
(1)操作①加热过程中,发生反应的化学方程式是_______。
(2)操作②不用Ba(NO3)2溶液的理由是:__________。
(3)进行操作②中,判断“BaCl2溶液是否过量”的方法是:_________。
(4)操作③“加入过量Na2CO3溶液”的目的是:________。
(5)操作⑤中“加适量盐酸”的主要目的是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com