
科目: 来源: 题型:
【题目】草酸(![]() )广泛存在于食品中,人们对其及相关产品进行了深入研究。
)广泛存在于食品中,人们对其及相关产品进行了深入研究。
(1)已知![]() 时,
时,![]() :
:![]() ,
,![]() 溶液显酸性。解释
溶液显酸性。解释![]() 溶液显酸性的原因:______;(用化学用语并配以必要文字说明)
溶液显酸性的原因:______;(用化学用语并配以必要文字说明)
(2)已知反应:![]() ,为了使草酸分解,通过
,为了使草酸分解,通过![]() 燃烧反应提供能量:
燃烧反应提供能量:![]() ,已知分解的草酸与所需空气(其中氧气的体分数为
,已知分解的草酸与所需空气(其中氧气的体分数为![]() )的物质的量之比为
)的物质的量之比为![]() ,则
,则![]() ______
______
(3)草酸分解生成的![]() 燃料燃烧不足以提供足够的能量,还可通过甲烷来制备
燃料燃烧不足以提供足够的能量,还可通过甲烷来制备![]() 。在密闭容器中通入物质的量浓度均为
。在密闭容器中通入物质的量浓度均为![]() 的
的![]() 和
和![]() ;在一定条件下发生反应
;在一定条件下发生反应![]() ,测得
,测得![]() 的平衡转化率与温度、压强的关系如下图1所示。
的平衡转化率与温度、压强的关系如下图1所示。

①由图判断压强![]() 、
、![]() 、
、![]() 、
、![]() 由小到大的顺序为:______;该反应的
由小到大的顺序为:______;该反应的![]() ______0(填“<”“>”“=”):
______0(填“<”“>”“=”):
②![]() 该反应的平衡常数为______(结果保留两位小数)
该反应的平衡常数为______(结果保留两位小数)
(4)常温下,向![]() 的
的![]() 溶液中逐滴加入
溶液中逐滴加入![]()
![]() 溶液,所得滴定曲线如图所示。下列说法正确的是______
溶液,所得滴定曲线如图所示。下列说法正确的是______

①![]() 点时:
点时:![]()
②![]() 点时:
点时:![]()
③![]() 点时:
点时:
④![]() 点时:
点时:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学按下图所示的装置进行实验。![]() 、
、![]() 为两种常见金属,它们的硫酸盐可溶于水,当
为两种常见金属,它们的硫酸盐可溶于水,当![]() 闭合时,
闭合时,![]() 从右向左通过交换膜移向
从右向左通过交换膜移向![]() 极。下列分析不正确的是
极。下列分析不正确的是

A. 溶液中![]() 增大
增大
B. ![]() 极的电极反应:
极的电极反应:![]()
C. ![]() 电极上有
电极上有![]() 产生,发生氧化反应
产生,发生氧化反应
D. 反应初期,![]() 电极周围出现白色胶状沉淀
电极周围出现白色胶状沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】观察下列实验装置图,按要求作答:
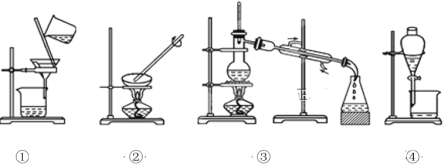
(1)写出图中四种实验操作的名称:___________________________________________________。
(2)装置④中所有玻璃仪器的名称:____________,____________。
(3)下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
A从海水中获取蒸馏水____________;B从KCl溶液中获取KCl晶体____________;
C分离CaCO3和水____________;D分离植物油和水____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,两种碳酸盐![]() ,(
,(![]() 分别为Ca2+和Ba2+两种离子)的沉淀溶解平衡曲线如图所示。已知:
分别为Ca2+和Ba2+两种离子)的沉淀溶解平衡曲线如图所示。已知:![]() ,
,![]() 。已知
。已知![]() 比
比![]() 溶解度更大(不考虑阴离子的水解)。下列说法正确的是
溶解度更大(不考虑阴离子的水解)。下列说法正确的是

A. 向![]()
![]() 的
的![]() 溶液中加入固体
溶液中加入固体![]() ,当加入
,当加入![]() 固体的质量为
固体的质量为![]() 时,
时,![]() 恰好沉淀完全(离子浓度为
恰好沉淀完全(离子浓度为![]() 时认为沉淀完全;忽略溶液体积变化)
时认为沉淀完全;忽略溶液体积变化)
B. ![]() 的
的![]()
C. 该温度下,向![]() 的饱和溶液中加入
的饱和溶液中加入![]() 溶液,一定能产生沉淀
溶液,一定能产生沉淀
D. 线![]() 表示
表示![]() 的溶解平衡曲线
的溶解平衡曲线
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于阿伏加德罗常数的说法中不正确的是( )
A.6.02×1023叫做阿伏加德罗常数
B.12g12C含有的碳原子数就是阿伏加德罗常数的值
C.含有阿伏加德罗常数值个微粒的物质是1mol
D.1.5molH2O含有9.03×1023个水分子
查看答案和解析>>
科目: 来源: 题型:
【题目】某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,盐桥中装有饱和![]() 溶液。下列叙述中正确的是
溶液。下列叙述中正确的是

A. 甲烧杯中溶液的![]() 逐渐减小 B. 乙烧杯中发生还原反应
逐渐减小 B. 乙烧杯中发生还原反应
C. 外电路的电流方向是从![]() 到
到![]() D. 电池工作时,盐桥中的
D. 电池工作时,盐桥中的![]() 移向甲烧杯
移向甲烧杯
查看答案和解析>>
科目: 来源: 题型:
【题目】臭氧是常见的强氧化剂,广泛用于水处理系统。制取臭氧的方法很多,其中高压放电法和电解纯水法原理如下图所示,下列有关说法不正确的是

A. 高压放电法,反应的原理为3O2![]() 2O3
2O3
B. 高压放电出来的空气中,除含臭氧外还含有氮的氧化物
C. 电解时,![]() 由电极
由电极![]() 经聚合固体电解质膜流向电极
经聚合固体电解质膜流向电极![]()
D. 电解时,电极![]() 周围发生的电极反应有
周围发生的电极反应有![]() 和
和![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作、现象及结论均正确的是
实验操作、现象 | 结论 | |
A | 取1 mL 20%的蔗糖溶液,加入3~5滴稀硫酸。水浴加热5 min后取少量溶液,加入少量新制Cu(OH)2,加热,无砖红色沉淀产生 | 蔗糖没有发生水解 |
B | 向装有溴水的分液漏斗中加入裂化汽油,充分振荡并静置,下层为橙色 | 裂化汽油可以萃取溴 |
C | 将SO2通入紫色石蕊溶液中,溶液先变红后褪色 | SO2是酸性氧化物,还具有漂白性 |
D | 分别向盛有KI3溶液的a、b试管中滴加淀粉溶液、AgNO3溶液,a中溶液变蓝,b中产生黄色沉淀 | 溶液中存在:I3- |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】用两支惰性电极插入50mLAgNO3溶液中,通电电解。当电解液的PH值从6.0变为3.0时(设电解时阴极没有氢气析出,且电解液在电解前后体积变化可以忽略),电极上析出银的质量大约是:
A. 27mg B. 54mg C. 108mg D. 216mg
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入1 mol·L-1的H2SO4溶液中,乙同学将电极放入1mol·L-1的NaOH溶液中,如图所示。

①写出甲中负极的电极反应式:__________。
②乙中负极反应式为__________,总反应的离子方程式:_______。
(2)将用导线相连的两个铂电极插入KOH溶液中,然后向两极分别通入CH3OH(甲醇)和O2 ,则发生了原电池反应,该原电池中的负极反应式为________________;正极反应式为______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com