
科目: 来源: 题型:
【题目】中学教材上介绍的干冰晶体是一种立方面心结构,如图所示,即每8个CO2构成立方体,且在6个面的中心又各占据1个CO2分子,在每个CO2周围距离![]() a(其中a为立方体棱长)的CO2有( )
a(其中a为立方体棱长)的CO2有( )

A. 4个 B. 8个 C. 12个 D. 6个
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用以下装置制备并检验Cl2的性质。下列说法正确的是( )

A. Ⅰ图:若MnO2过量,则浓盐酸可全部消耗完
B. Ⅱ图:证明新制氯水具有酸性和漂白性
C. Ⅲ图:产生了棕黄色的雾
D. Ⅳ图:有色布条均褪色
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)高铁酸钾![]() 不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为
不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为![]()
![]()
![]() ,如图是高铁电池的模拟实验装置:
,如图是高铁电池的模拟实验装置:

①该电池盐桥中盛有饱和![]() 溶液,此盐桥中氯离子向______(填“左”或“右”)移动。
溶液,此盐桥中氯离子向______(填“左”或“右”)移动。
②该电池放电时正极的电极反应式为______;充电时每转移0.3mol电子,有______mol![]() 生成,正极附近溶液的碱性______(填“增强”,“不变”或“减弱”)。
生成,正极附近溶液的碱性______(填“增强”,“不变”或“减弱”)。

③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_________________。
(2)“![]() ”电池可将
”电池可将![]() 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“![]() ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为![]()
![]()
![]() 。放电时该电池“吸入”
。放电时该电池“吸入”![]() ,其工作原理如图所示:
,其工作原理如图所示:

①充电时,正极的电极反应式为________________________________。
②放电时,若生成的![]() 和
和![]() 全部沉积在电极表面,当转移0.2mol
全部沉积在电极表面,当转移0.2mol![]() 时,两极的质量差为______。
时,两极的质量差为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2CO3是重要的化工原料,工业上采用NH3、CO2、NaCl为原料来制备。某兴趣小组用NH4HCO3固体替换NH3和CO2,按照下列流程在实验室模拟制备Na2CO3。

完成下列填空:
(1)步骤1中,为控制反应温度在30~35℃,应选用的加热方式是_______________;实验前NH4HCO3固体须在____________里(填仪器名称)磨成粉末,且加入时要不断搅拌,这些操作的目的是_____________________________________________________________。
(2)步骤3中,使用饱和NaHCO3溶液洗涤白色固体的原因是____________________________。
(3)步骤4中,恒温炉内发生的化学反应为______________________________(书写化学方程式)。
为检验产品纯度,该小组按如下流程操作:

(4)判断操作II中滴加Ba(OH)2溶液是否过量的方法是___________________________________。
(5)若样品中杂质不与Ba(OH)2反应,则Na2CO3的质量分数为____________(小数点后保留两位)。
(6)若样品中所含杂质是NaHCO3、NaCl中的一种或两种,①如何确定样品中是否含有NaCl,设计实验方案_________________________________________________________________。
②有同学认为,根据上述实验数据就可以判断出样品中一定含有NaCl,无需再实验检验,判断的理由是____________________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】丁烷在一定条件下裂解可按两种方式进行:
C4H10 ![]() C2H6 +C2H4,C4H10
C2H6 +C2H4,C4H10 ![]() CH4 +C3H6
CH4 +C3H6
如图是某化学兴趣小组进行丁烷裂解的实验流程。(注:![]() 能将烃氧化成
能将烃氧化成![]() 和
和![]() ,G后面装置与答题无关,省略)
,G后面装置与答题无关,省略)

按上图连好装置后,需进行的实验操作有:
①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等
(1)这三步操作的先后顺序依次是______。
(2)氧化铝的作用是______,甲烷与氧化铜反应的化学方程式是______。
(3)B装置所起的作用是______。
(4)若对E装置中的混合物(溴水足量),再按以下流程实验:

①操作Ⅰ、操作Ⅱ分别是______、______。
②![]() 溶液的作用是(用离子方程式表示)__________________________。
溶液的作用是(用离子方程式表示)__________________________。
③已知B只有一种化学环境的氢原子,则B的结构简式为__________________、
(5)假定丁烷完全裂解,当(E+F)装置的总质量比反应前增加了1.82g,G装置的质量减少了4.16g,则丁烷的裂解产物中甲烷和乙烷的物质的量之比![]() ______(假定流经D、G装置中的气体能完全反应)
______(假定流经D、G装置中的气体能完全反应)
查看答案和解析>>
科目: 来源: 题型:
【题目】EPR橡胶(![]() )和PC塑料(
)和PC塑料( )的合成路线如下:
)的合成路线如下:

(1)A的名称是 ___________。E的化学式为______________。
(2)C的结构简式____________。
(3)下列说法正确的是(选填字母)_________。
A.反应Ⅲ的原子利用率为100%
B.CH3OH在合成PC塑料的过程中可以循环利用
C.1 mol E与足量金属 Na 反应,最多可生成22.4 L H2
D.反应Ⅱ为取代反应
(4)反应Ⅰ的化学方程式是_________。
(5)反应Ⅳ的化学方程式是_________。
(6)写出满足下列条件F的芳香族化合物的同分异构体________。
①含有羟基,
②不能使三氯化铁溶液显色,
③核磁共振氢谱为五组峰,且峰面积之比为1:2:2:2:1;
(7)已知:![]() ,以D和乙酸为起始原料合成
,以D和乙酸为起始原料合成![]() 无机试剂任选,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明反应试剂和条件)_______。
无机试剂任选,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明反应试剂和条件)_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a,![]() 、
、![]() 是两块电极板,通过导线与直流电源相连。请回答下列问题:
是两块电极板,通过导线与直流电源相连。请回答下列问题:

(1)若![]() 、
、![]() 都是惰性电极,a是饱和
都是惰性电极,a是饱和![]() 溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中
溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中![]() 极现象为______,电极反应式为______,电解
极现象为______,电极反应式为______,电解![]() 溶液的离子方程式是______。
溶液的离子方程式是______。
(2)如要在铁上镀银,电解液选用硝酸银,则![]() 电极的材料是______,电极反应式是______。
电极的材料是______,电极反应式是______。
(3)若![]() 极为铜锌合金,
极为铜锌合金,![]() 极为纯铜,且电解质溶液中含有足量的
极为纯铜,且电解质溶液中含有足量的![]() ,通电一段时间后,若阳极恰好完全溶解,此时阴极质量增加7.68g,溶液质量增加0.03g,则合金中
,通电一段时间后,若阳极恰好完全溶解,此时阴极质量增加7.68g,溶液质量增加0.03g,则合金中![]() 、
、![]() 的物质的量之比为______。
的物质的量之比为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某烃A0.2mol在氧气中完全燃烧后,生成![]() 、
、![]() 各1.2mol。回答下列问题:
各1.2mol。回答下列问题:
(1)烃A的分子式为______。
(2)若烃A不能使溴水褪色,但在一定条件下能氯气发生取代反应,其—氯取代物只有一种,则烃A的结构简式为______。
(3)若取一定量的该烃A完全燃烧后,生成![]() 和
和![]() 各3mol,则有______g烃A参加了反应,燃烧时消耗标准状况下的氧气______L。
各3mol,则有______g烃A参加了反应,燃烧时消耗标准状况下的氧气______L。
(4)若烃A能使溴水褪色,在催化剂作用下,与![]() 加成,其加成产物经测定分子中含有4个甲基,则烃A可能的机构简式有(不考虑立体异构)______。
加成,其加成产物经测定分子中含有4个甲基,则烃A可能的机构简式有(不考虑立体异构)______。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳、氢元素可形成种类繁多的烃类物质。
(1)下图表示某些烃分子的模型:
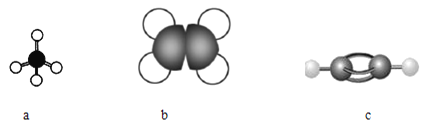
①写出a分子的空间构型______。
②c分子中的一个氢原子被![]() —取代后的物质共直线的原子最多有______个。
—取代后的物质共直线的原子最多有______个。
③取等质量的上述三种烃充分燃烧,耗氧量最大的是______(填分子式)。
④25℃和101kPa时,取a、b和c组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了56mL,原混合烃中c的体积分数为______。
(2)某烯烃的结构简式如下所示:
![]()
①用系统命名法对该烃与![]() 的加成产物命名:______,该加成产物的—氯取代物有______种。
的加成产物命名:______,该加成产物的—氯取代物有______种。
②该烯烃可以加聚生成高分子,写出该高聚物的结构简式______。该烯烃还能与乙烯以1:1比例反应形成一种环状化合物,请写出该环状化合物的键线式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com