
科目: 来源: 题型:
【题目】如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。下列说法正确的是

A. N极的电极反应式为2HSO3-+2H++e-==S2O42-+2H2O
B. M极的电极反应式为SO2+2H2O-2e-==SO42-+4H+
C. 离子交换膜为阴离子交换膜
D. b为直流电源的正极
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用如下图所示装置(Ⅰ)制取溴苯和溴乙烷。

已知
(1)已知溴乙烷为无色液体,难溶于水,沸点为38.4℃,熔点为-119℃,密度为1.46 g·cm-3。
(2)CH3CH2OH+HBr![]() CH3CH2Br+H2O,
CH3CH2Br+H2O,
CH3CH2OH![]() CH2=CH2↑+H2O,
CH2=CH2↑+H2O,
2CH3CH2OH![]() C2H5—O—C2H5+H2O
C2H5—O—C2H5+H2O
主要实验步骤如下:
①检查装置的气密性后,向烧瓶中加入一定量的苯和液溴。
②向锥形瓶中加入乙醇和浓H2SO4的混合液至恰好没过进气导管口。
③将A装置中的纯铁丝小心向下插入混合液中。
④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10分钟。
请填写下列空白:
(1)写出A中反应的化学方程式__________________________________________________,导管a的作用是____________________。
(2)C装置中U形管内部用蒸馏水封住管底的作用是______________________________。
(3)反应完毕后,U形管中分离出溴乙烷时所用的最主要仪器的名称是(只填一种)__________。
(4)步骤④中能否用大火加热,理由是____________________。
(5)为证明溴和苯的上述反应是取代反应而不是加成反应。该同学用装置(Ⅱ)代替装置B、C直接与A相连重新反应。装置(Ⅱ)的锥形瓶中,小试管内的液体是_________________________(填名称),其作用是__________________;小试管外的液体是__________________(填名称),其作用是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在标准状况下14.4 g CO与CO2的混合气体,体积为8.96 L。则:
(1)混合气体的密度是_________(保留三位有效数字)。
(2)混合气体的平均摩尔质量是_______。
(3)CO2和CO的体积之比_______。
(4)CO的体积分数是__________。
(5)CO2和CO的质量之比是_________。
(6)混合气体中所含氧原子的物质的量是______________。
(7)混合气体中所含碳原子的数目是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某烃A相对分子质量为140,其中碳的质量分数为0.857。A分子中有两个碳原子不与氢直接相连。A在一定的条件下氧化只生成G,G能使石蕊试液变红
已知:

(1)A的分子式____________。化合物G的结构简式:G____________。
(2)A分子加氢后生成的烷烃的一氯取代物有____________种。将足量A加入溴水中充分反应,现象为________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】今年为门捷列夫发现元素周期律150周年。门捷列夫预言了很多未知元素,锗是其中一种,工业上用精硫锗矿(主要成分为GeS2)制取高纯度锗,其工艺流程如图所示。请回答:
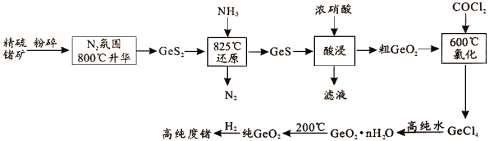
(1)锗在元素周期表中的位置是__________。
(2)800℃,在N2氛围中使精硫锗矿升华的目的是______________。
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式____。酸浸时温度不能过高的原因是_____
(4)GeCl4易水解生成GeO2·nH2O,此过程化学方程式为_____。温度对GeCl4水解率的影响如图所示,为提高水解率,实验时可采取的措施为______(填序号)。

A.冰水浴
B.冰盐水浴
C.49℃水浴
(5)请判断25℃时0.1mol·L-1NaHGeO3溶液pH________(填“>”=”或“<”)7,理由是____(已知25℃时,H2GeO3的Ka1=1.7×10-9,Ka2=1.9×10-13)。
查看答案和解析>>
科目: 来源: 题型:
【题目】标准状况下有①6.72LCH4;②3.01x1023个HCl;③13.6gH2S;④0.2molNH3。下列对四种气体的关系从小到大表示不正确的是( )
A.体积:④<①<②<③
B.密度:①<④<③<②
C.质量:④<①<③<②
D.氢原子数:②<④<③<①
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关气体体积的叙述正确的是( )
A.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子大小决定
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定
C.不同的气体,若体积不同,则它们所含的分子数也不同
D.气体摩尔体积指1mol任何气体所占的体积约为22.4L
查看答案和解析>>
科目: 来源: 题型:
【题目】18-Ⅰ分子中只有两种不同化学环境的氢,且数目比为3:2的化合物(________)
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
Ⅱ奥沙拉秦是曾用于治疗急、慢性溃疡性结肠炎的药物,其由水杨酸为起始物的合成路线如下:
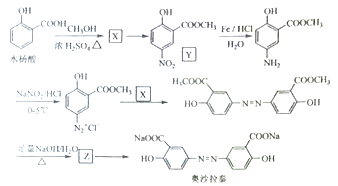
回答下列问题:
(1)X的结构简式为____;由水杨酸制备X的反应类型为_____。
(2)由X制备Y的反应试剂为_________。
(3)工业上常采用廉价的![]() ,与Z反应制备奥沙拉秦,通入的
,与Z反应制备奥沙拉秦,通入的![]() 与Z的物质的量之比至少应为____。
与Z的物质的量之比至少应为____。
(4)奥沙拉秦的分子式为______,其核磁共振氢谱为______组峰,峰面积比为______。
(5)若将奥沙拉秦用![]() 酸化后,分子中含氧官能团的名称为____。
酸化后,分子中含氧官能团的名称为____。
(6)W是水杨酸的同分异构体,可以发生银镜反应;W经碱催化水解后再酸化可以得到对苯二酚。W的结构简式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 将TiCl4溶于水、加热,得到沉淀TiO2·xH2O,继续焙烧可得到TiO2
B. 可采取加热蒸发的方法使FeCl3从水溶液中结晶析出
C. 配制FeCl3溶液时,为了防止溶液出现浑浊,可以向溶液中滴入少量盐酸
D. 为了除去MgCl2酸性溶液中的FeCl3,可在加热搅拌的条件下加入MgCO3,过滤后,再向滤液中加入适量盐酸
查看答案和解析>>
科目: 来源: 题型:
【题目】化学家们合成了如图所示的一系列的星烷,如三星烷、四星烷、五星烷等。下列说法正确的是


A. 它们之间互为同系物
B. 六星烷的化学式为C18H22
C. 三星烷与丙苯互为同分异构体,四星烷与 互为同分异构体
互为同分异构体
D. 它们的一氯代物均只有两种而三星烷得二氯代物有四种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com