
科目: 来源: 题型:
【题目】(1)分别按如图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸。请回答下列问题:

①以下叙述中,正确的是__(填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.装置乙中存在“化学能→电能→光能”的转化
D.乙的外电路中电流方向Zn→Cu
E.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
F.乙溶液中SO42-向铜片方向移动
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是___。
③在乙实验中,如果把硫酸换成硫酸铜溶液,当负极材料消耗的质量为2.6g时,则电路中转移电子数为___。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
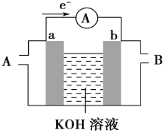
①电池工作时,空气从__口通入(填“A”或“B”);
②若使用的燃料为甲醇(CH3OH),a极的电极反应式为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)①④⑥三种元素构成的化合物的电子式:__;⑨的最高价氧化物对应水化物的化学式:__。
(2)⑤、⑦、⑧的简单离子半径由大到小的顺序:__(用离子符号填写)。
(3)用一个化学方程式表示④、⑤二种元素非金属性的强弱__。
(4)⑦的单质与⑥的最高价氧化物对应水化物的水溶液反应的离子方程式为__。
(5)元素①、元素④以原子个数比为1∶1形成化合物Q,元素①、元素③形成化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终产物对空气没有污染,写出该反应的化学方程式:__。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化合物的结构如图所示,W、X、Y均为短周期元素,W+离子为短周期金属阳离子中半径最大的元素,Y元素形成的单质是理想的气体燃料。下列说法不正确的是( )

A.该化合物是强还原剂
B.Y-与Li+具有相同的电子层结构
C.X可能是碳元素或者是硅元素
D.原子半径大小关系为:W>X>Y
查看答案和解析>>
科目: 来源: 题型:
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药 I 的合成路线如下:

已知:a. 
b.  RCHO
RCHO
回答下列问题:
(1)反应①所需试剂、条件分别是_____;F 的化学名称为_____。
(2)②的反应类型是_____;A→B 的化学方程式为_____。
(3)G 的结构简式为_____;H 中所含官能团的名称是_____。
(4)化合物 W 的相对分子质量比化合物 C 大 14,且满足下列条件,W 的可能结构有_____种,其中核磁共振氢谱显示有 5 种不同化学环境的氢,峰面积比为 2∶2∶2∶1∶1 的结构简式为_____。
①遇 FeCl3 溶液显紫色 ②属于芳香族化合物 ③能发生银镜反应
(5)设计用甲苯和乙醛为原料制备 的合成路线_____(无机试剂任选)。
的合成路线_____(无机试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

(1)B极上的电极反应式为 。
(2)若用该燃料电池做电源,用石墨做电极电解硫酸铜溶液,当阳极收集到11.2L(标准状况)气体时,消耗甲醇的质量为 克,若要使溶液复原,可向电解后的溶液中加入的物质有 。
(3)目前已开发出用电解法制取ClO2的新工艺。

①上图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。若用上述甲醇燃料电池进行电解,则电解池的电极a接甲醇燃料电池的 极( 填A或B) ,写出阳极产生ClO2的电极反应式:__________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为_________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH ![]() CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)25 ℃时,浓度均为0.1mol/L的盐酸和醋酸溶液,下列说法正确的是___________;
①两溶液的pH相同
②两溶液的导电能力相同
③由水电离出的c(OH-)相同
④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
(2)25℃时,pH =5的稀醋酸溶液中,由水电离的c(OH-)=____________mol·L-1 ,c(CH3COO-)=_____________mol·L-1 (填数字表达式);
(3)25 ℃时,向pH均为1的盐酸和醋酸溶液中分别加水,随加水量的增多,两溶液pH的变化如图所示,则符合盐酸pH变化的曲线是_______________;

(4)25 ℃时,向体积为Va mLpH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与的Vb关系是Va________________Vb(填“>”、“<”或“=”)。
(5)25 ℃时,若向氨水中加入稀盐酸至溶液的pH=7,此时c(NH4+)=a mol/L,则c(Cl-)=________ mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制取氯气的反应化学方程式如下:(用元素符号或化学式表示)
MnO2+4HCl(浓)= MnCl2+Cl2↑+2H2O
(1)还原剂是:______;氧化产物是 _________;
(2)被氧化的原子与被还原的原子个数之比为____
(3)请用双线桥法表示反应的电子转移方向和数目
查看答案和解析>>
科目: 来源: 题型:
【题目】黑色金属是指铁、铬、锰及其合金,在生产生活中有着广泛的用途。请回答下列问题:
(l)基态铬原子核外存在___ 对自旋相反的电子,其未成对电子有____种空间伸展方向。铁和锰的第三电离能(I3)较大的是____(填元素符号),原因是____。
(2)环戊二烯![]() ,无色液体,熔点-97.5℃,沸点40. 0℃,存在于煤焦油中。
,无色液体,熔点-97.5℃,沸点40. 0℃,存在于煤焦油中。
①环戊二烯物质中存在的微粒间相互作用有____
A 范德华力 B 氢键 C δ键 D π键
②环戊二烯分子中碳原子的杂化轨道类型是_____
③配合物中配体提供电子对的方式包括孤对电子、π电子等。二茂铁的分子结构如图所示,其中铁的配位数是____。

(3)金属锰的一种面心立方晶胞结构示意图如图所示,已知锰原子半径为141. 4pm,则该晶胞参数a= ___。由于晶体缺陷造成晶体结构中部分原子缺失,测得实际密度为5. 52g·cm-3,Mn元素相对原子质量按为54. 94计算,此晶胞的缺陷率为____(缺陷率为单位体积内缺失原子数占应有原子总数的百分比)。

查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) △H
CH3OH(g) △H
(1)化学平衡常数表达式为K=___________________。
(2)下图是该反应在不同温度下CO的转化率随时间变化的曲线。

① 该反应的焓变ΔH______0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1____________K2(填“>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是_________。
a. 升高温度 b. 将CH3OH(g)从体系中分离
c. 使用合适的催化剂 d. 充入He,使体系总压强增大
(3)已知在常温常压下:① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)ΔH =-a kJ·mol-1② 2CO(g)+O2(g)=2CO2(g) ΔH =-b kJ·mol-1③ H2O(g)= H2O(l) ΔH=-c kJ·mol-1,则,CH3OH(l)+O2(g) =CO(g)+2H2O(l)ΔH=___kJ·mol-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

(1)c中证明氯水含有________粒子(用粒子符号表示)。
(2)d过程中的现象是____________________,
(3)b过程中反应的离子方程式___________________。
(4)a过程中反应的化学方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com