
科目: 来源: 题型:
【题目】下列关于试剂存放的叙述正确的是( )
A.硝酸银溶液存放在无色试剂瓶中
B.金属钠保存在CCl4中(钠的密度小于CCl4)
C.氢氧化钠溶液保存在带玻璃塞的玻璃瓶中
D.浓硫酸的装运包装箱应贴上如图所示的标识

查看答案和解析>>
科目: 来源: 题型:
【题目】在酸性溶液中用400mL 0.075molL-1的KMnO4溶液处理2gCu2S和CuS的混合物,发生如下反应: ① 8MnO4- + 5Cu2S + 44H+ = 10Cu2+ + 5SO2↑+ 8Mn2+ + 22H2O② 6MnO4- + 5CuS + 28H+ = 5Cu2+ + 5SO2↑+ 6Mn2+ + 14H2O,反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL 0.1molL-1的(NH4)2Fe(SO4)2溶液完全反应。已知该反应的化学方程式如下:2KMnO4+10(NH4)2Fe(SO4)2+8H2SO4=K2SO4+2MnSO4+10(NH4)2SO4+5Fe2(SO4)3+8H2O
(1)反应①的氧化剂为____;还原剂为_______;氧化产物为___________。
(2)用双线桥法标出反应②的电子转移情况____ 6MnO4- + 5CuS + 28H+ = 5Cu2+ + 6Mn2++ 5SO2↑ + 14H2O
(3)反应②中每转移3mol电子,可生成标准状况下气体的体积为_________L。
(4)KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为 ______ mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组同学进行如下实验,以检验化学反应中的能量变化。请回答下列问题:
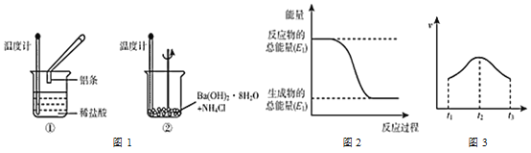
(1)实验中发现,反应后①中的温度___,②中的温度___。(填“升高”或“降低”)
(2)上述反应过程中的能量变化可用图2表示的是___(填“①”或“②”)。
(3)实验①中测得产生气体的速率与时间的关系如图3所示,则t2-t3反应速率逐渐小的主要原因是___;
(4)写出①中发生反应的离子方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是元素周期表的一部分,请回答下列问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质最不活泼的是___(填元素符号)。
(2)③的气态氢化物的电子式___,②④形成的气态化合物的结构式___。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为___(填物质的化学式),写出它的电子式:___;酸性最强的含氧酸为___(填物质的化学式),写出它的电离方程式:___。
(4)在②和③两种元素中,非金属性较强的是___(填元素名称),②的单质可以和③的最高价氧化物的水化物反应,请写出有关化学方程式___。
(5)②与Si元素分别形成的最高价氧化物,___的熔点更高,原因是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】以下事实不能用勒夏特利原理来解释的是: ( )
A. 用排饱和食盐水的方法收集氯气
B. 增大压强,有利于N2和H2反应生成NH3
C. 合成氨工业选择高温(合成氨反应为放热反应)
D. 在Fe3++3SCN - ![]() Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
查看答案和解析>>
科目: 来源: 题型:
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测合理的是

A. 由①、②可知, pH越大,+2价铁越易被氧化
B. 由②、③推测,若pH>7,+2价铁更难被氧化
C. 由①、③推测,FeCl2被O2氧化的反应为放热反应
D. 60℃、pH=2.5时, 4 h内Fe2+的平均消耗速率大于 0.15a mol/(L·h)
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在一恒容密闭容器中,能表示反应 X(g)+2Y(g)![]() 2Z(g) 一定达到化学平衡状态的是
2Z(g) 一定达到化学平衡状态的是
①容器中气体的密度不再发生变化
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成2n mol Z,同时消耗2n mol Y
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,将2molSO2和1molO2充入一定容积的密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
2SO3(g) △H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
A.达到反应限度时,生成SO3为2mol
B.达到反应限度时反应放出的热量小于197kJ
C.达到反应限度时SO2、O2、SO3的分子数之比一定为2∶1∶2
D.达到反应限度时O2的消耗速率等于SO3的消耗速率
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作或现象不能用平衡移动原理解释的是
A. 卤化银沉淀的转化

B. 配制FeCl3溶液

C. 淀粉在不同条件下水解

D. 探究石灰石与稀盐酸在密闭环境下的反应

查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应2NO2![]() 2N0+O2在密闭容器中反应,达到平衡状态的标志是( )
2N0+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时生成2nmolNO2
②单位时间内生成nmolO2的同时生成2nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : l 的状态
④混合气体的颜色不再改变的状态
A. ①④ B. ②③ C. ①③④ D. ①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com