
科目: 来源: 题型:
【题目】将Mg、Cu组成的混合物26.4g投入到适量的稀硝酸中,固体完全溶解,收集到标准状况下的NO气体8.96L,向反应后的溶液中加入过量的5mol·L-1的NaOH溶液300mL,金属离子完全沉淀。则形成沉淀的质量是 ( )
A. 43.2gB. 46.8gC. 53.6gD. 63.8g
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验现象预测正确的是( )
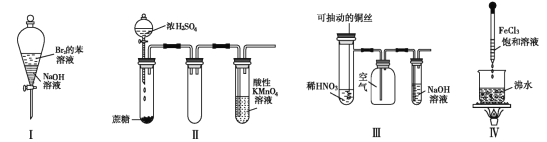
A. 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
B. 实验Ⅱ :酸性 KMnO4 溶液中出现气泡,且颜色逐渐褪去
C. 实验Ⅲ:微热稀 HNO3 片刻,溶液中有气泡产生,广口瓶内始终保持无色
D. 实验Ⅳ:滴入 FeCl3 后,可形成带电的胶体,该分散系导电能力增强
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:①C(s)+O2 (g)=CO2 (g);△H1,
②C(s)+1/2O2 (g)=CO (g) ;△H2
③C(s)+CO2 (g)=2CO(g) ;△H3
④4Fe(s)+3O2(g)=2Fe2O3(s) ;△H4
⑤3CO (g)+Fe2O3(s)=2Fe(s)+3CO2(g) ;△H5。下列叙述正确的是
A. △H4是Fe的燃烧热B. △H1>△H2
C. △H3=2△H2-△H1D. 3△H1-3△H2-![]() △H4+△H5=0
△H4+△H5=0
查看答案和解析>>
科目: 来源: 题型:
【题目】铜锌原电池(如图)工作时,下列叙述正确的是

A. 正极反应为:Zn-2e-=Zn2+
B. 一段时间后铜片增重,盐桥中K+移向CuSO4溶液
C. 电流从锌片经导线流向铜片
D. 电池工作时Zn2+和Cu2+的浓度保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】硫黄在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,溴水褪色,乙变成丙。在丙里加入Na2S生成气体丁,把丁通入乙得到沉淀戊。甲、乙、丙、丁、戊均含有硫元素,则它们正确的顺序是
A. SO3、H2SO4、H2SO3、H2S、SB. SO2、H2SO3、H2SO4、SO2、SO3
C. SO3 、H2SO4、H2SO3、SO2、Na2S2O3D. SO2、H2SO3、H2SO4、H2S、S
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图中的实验,能达到实验目的的是( )
A.  证明稳定性:Na2CO3>NaHCO3
证明稳定性:Na2CO3>NaHCO3
B.  证明非金属性:Cl>Br>I
证明非金属性:Cl>Br>I
C.  验证镁和盐酸反应的热效应
验证镁和盐酸反应的热效应
D. 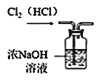 除去 Cl2 中的杂质气体 HCl
除去 Cl2 中的杂质气体 HCl
查看答案和解析>>
科目: 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是________,D是________,G是________,H是________(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:_____________________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为__________________________。
(3)A中元素的原子结构示意图为________________。
(4)上述反应中属于氧化还原反应的是_________(填写序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在四个不同的容器中,分别进行不同条件下的合成氨反应N2(g)+3H2(g)![]() 2NH3(g)。在相同时间内表示该反应速率最快的是
2NH3(g)。在相同时间内表示该反应速率最快的是
A. v(H2)=0.1mol/(Ls) B. v(N2)=0.1mol/(Ls) C. v(N2)=0.2mol/(Ls) D. v(NH3)=0.3mol/(Ls)
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用0.1 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20mL待测盐酸注入洁净的锥形瓶中,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上1~2cm 处;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)__________AF。
(2)上述B步骤操作的目的是_____________。
(3)在进行C步操作滴定前排气泡时,应选择下图2中的___________(填序号),若用25mL滴定管进行实验,当滴定管中的液面在“10”处,则管内液体的体积(填序号)____________(①=10mL,②=15mL,③<10mL,④>15mL)。

(4)判断以下操作,对测定结果盐酸浓度的影响(填“偏高”、“偏低”或““无 影响”)
①上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响是__________。
②若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对滴定结果产生的影响是____________。
③如果滴定前装有待测溶液的酸式滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com