
科目: 来源: 题型:
【题目】(1)含氢原子为0.2×6.02×1024个的NH4HCO3,其质量是___,其中含氧原子的物质的量为___。3.6克水中含有质子数为___(阿伏伽德罗常数为NA)。
(2)现实验室要用12mol·L-1氢氧化钠溶液来配制浓度为0.6mol·L-1的稀氢氧化钠溶液100mL,则需要这种浓碱的体积是___mL。需要用托盘天平称量___克氢氧化钠才能配制成0.5mol·L-1的氢氧化钠溶液100mL。
(3)将标况下aLHCl气体溶于配制成1L盐酸溶液,所得溶液密度为dg/cm3,则所得溶液物质的量浓度为___mol/L,该溶液中溶质的质量分数为___。
(4)在标准状况下,某气体A的密度是1.25g·L-1,则它的摩尔质量是___,同温同压下该气体相对于氢气的密度是___;在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,此混合气体的平均相对分子质量是___,混合物中CO和CO2物质的量之比是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.10molL1的NaOH溶液分别滴定20.00mL浓度均为0.10molL1的CH3COOH溶液和HCN溶液,所得滴定曲线如图所示,下列说法正确的是( )

A. 点①和点②所示溶液中:c(CH3COO)<c(CN)
B. 点④所示溶液中:c(Na+)>c(OH)>c(CH3COO)>c(H+)
C. 点①和点②所示溶液中:c(CH3COO)c(CN)=c(HCN)c(CH3COOH)
D. 点③所示溶液中:c(CH3COO)+c(OH)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
I.(1)AlCl3的水溶液pH______7(填>、=、<=,其原因为______________(用离子方程式表示),将其溶液加热蒸干并灼烧最终得到物质是_____________________(填化学式)。
(2)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH)=1032,要使c(Cr3+)降至105mol/L,溶液的pH应调至___。
(3)物质的量浓度相同的三种溶液:①(NH4)2SO4 ②氨水 ③NH4HSO4,c(NH4+)大小顺序正确的是______。(用序号表示)
(4)常温下两种溶液:a.pH=4 NH4Cl b.pH=4盐酸溶液,其中水电离出C(H+)之比为______。
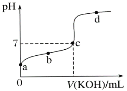
II.室温下,某一元弱酸HA的电离常数K=1.6×10-6。 向20.00 mL 浓度约为0.1 mol·L-1 HA溶液中逐滴加入0.1000 mol·L-1 的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
(1)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用________作指示剂,滴定终点在___(填“c点以上”或“c点以下”)。
(2)滴定过程中部分操作如下,下列各操作使测量结果偏高的是___________(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(3)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_______mol/L。(保留4位有效数字)
实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
1 | 21.01 | 20.00 |
2 | 20.99 | 20.00 |
3 | 21.60 | 20.00 |
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,不满足如图所示转化关系的是(反应条件略去,箭头表示一步转化)( )
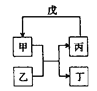
选项 | 甲 | 乙 | 丙 | 戊 |
A | NH3 | Cl2 | N2 | H2 |
B | C | SiO2 | CO | CuO |
C | Al(OH)3 | NaOH | NaAlO2 | CO2 |
D | Br2 | FeI2 | FeBr3 | Cl2 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
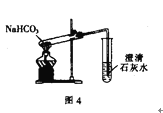
【题目】用下列实验装置进行相应的实验,能达到实验目的的是( )
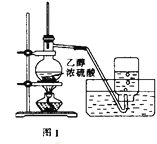


A. 利用图1装置制备乙烯
B. 利用图2装置除去Cl2中的HCl
C. 利用图3装置证明酸性强弱:盐酸>H2CO3>醋酸
D. 利用图4装置探究NaHCO3的热稳定性
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室配制500mL0.1mol/LNa2CO3,溶液回答下列问题
(1)配制Na2CO3溶液时需用的主要仪器有托盘天平、滤纸、烧杯、药匙、量筒、___、___、___。
(2)配制溶液过程如下:
A.用托盘天平称取Na2CO3·10H2O晶体___g;
B.将固体置于烧杯中,用量筒向其中加水溶解,并恢复至室温;
C.用玻璃棒引流,将溶液转移至容量瓶;
D.洗涤玻璃棒和烧杯2-3次,将洗涤液都转移入容量瓶中;
E.___;
F.继续向容量瓶中注水,至液面离容量瓶颈刻度线下___cm时,改用___滴加蒸馏水至液面与刻度线相切;
G.盖好瓶塞,用食指抵住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次摇匀;
H.将溶液转移至试剂瓶中,贴上标签,标注试剂名称、浓度及配制时间。
(3)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A.加水时超过刻度线___;
B.溶解后未冷却到室温就转入容量瓶___;
C.容量瓶内壁附有水珠而未干燥处理___;
D.定容时仰视___;
E.上下颠倒摇匀后液面低于刻度线___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作、现象和结论均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 植物油和溴水混合后振荡、静置 | 溶液分层,溴水褪色 | 植物油萃取了溴水中的Br2 |
B | 将硫酸酸化的H2O2滴入Fe(NO3)2溶液中 | 溶液变黄色 | H2O2的氧化性比Fe3+弱 |
C |
| 出现白色沉淀 | 氨气、二氧化碳与饱和食盐水反映生成碳酸钠 |
D | 将盛有铜与浓硫酸的试管加热,发现试管底部出现白色固体,倒去试管中液体,再加入适量水 | 白色固体溶解,溶液显蓝色 | 白色固体为无水硫酸铜 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示,电极为惰性电极。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42—等离子。下列叙述中正确的是( )

A. A膜是阳离子交换膜
B. 通电后,海水中阴离子往b电极处移动
C. 通电后,b电极上产生无色气体,溶液中出现白色沉淀
D. 通电后,a电极的电极反应式为4OH--4e-=O2↑+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】化学家正在研究尿素动力燃料电池,尿液也能发电。用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电,尿素燃料电池结构如图所示,下列有关描述正确的是( )

A. 电池工作时H+移向负极
B. 该电池用的电解质溶液是KOH溶液
C. 甲电极反应式:CO(NH2)2+H2O-6e-=CO2+N2+6H+
D. 电池工作时,理论上每净化1 mol CO(NH2)2,消耗33.6 L O2
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是分离混合物时常用的仪器,回答下列问题:

(1)写出仪器A、E的名称____、____。
(2)若向C装置中加入碘水和少量CCl4,振荡后静置,会观察到什么现象?____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com