
科目: 来源: 题型:
【题目】下列检验方法和结论正确的是 ( )
A. 加入硝酸银溶液有白色沉淀生成,证明原溶液中一定有Cl-
B. 在加入稀硝酸后的溶液中,再滴加氯化钡溶液有白色沉淀生成,证明原溶液中一定有SO![]()
C. 加入盐酸后加热,放出能使澄清石灰水变浑浊的无色无味气体,证明原溶液中一定含有CO![]()
D. 加入紫色石蕊试液,溶液显红色,证明溶液一定呈酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钾的冶炼可采用如下方法:2KF+CaC2![]() CaF2+2K↑+2C,下列有关说法合理的是( )
CaF2+2K↑+2C,下列有关说法合理的是( )
A.该反应的氧化剂是KF,氧化产物是K
B.该反应能说明C的还原性大于K
C.电解KF溶液不可能制备金属钾
D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铁矿(主要成分FeS2)是工业制硫酸的主要原料,暴露在空气中会被缓慢氧化,其氧化过程如下图所示。

下列有关说法不正确的是
A. 经氧化后的黄铁矿可能呈现与铁锈类似的红褐色
B. a步反应中每生成1 mol FeSO4转移电子的物质的量为7 mol
C. 氧化过程会产生较多酸性废水破坏矿区生态环境
D. 标准状况下,0.1 mol FeS2完全被氧化时大约消耗空气40 L
查看答案和解析>>
科目: 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为 2NO2(g)+O3(g) ![]() N2O5(g)+O2(g)。有关说法正确的是( )
N2O5(g)+O2(g)。有关说法正确的是( )
A. 增大压强可增大反应速率 B. 升高温度可减小反应速率
C. 达到平衡时,v(正)=v(逆)=0 D. 达到平衡时,NO2转化率为100%
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙(CaO2)是一种白色、无毒、难溶于水的固体,加热至350 ℃左右开始分解放出氧气。过氧化钙能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。其工业制备的主要流程如下:
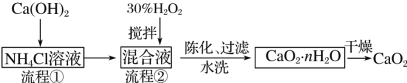
(1)搅拌的目的是______。流程②中没有采用加热措施的可能原因是______、______。流程②的化学反应方程式为________________。
(2)整个流程中,除水外还可以循环使用的物质是______。
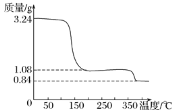
(3)取上述制得的CaO2·nH2O晶体进行热重分析,其热分解时晶体的质量随温度变化的曲线如右图。请通过计算给出过氧化钙晶体(CaO2·nH2O)的化学式(写出计算过程) __________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是 ( )
A. 标准状况下,22.4LH2O含有的分子数为1 NA
B. 常温常压下,16g O2含有的原子数为1 NA
C. 通常状况下,1NA 个SO2分子占有的体积约为22.4L
D. 物质的量浓度为0.5mol/L的K2SO4溶液中,含有SO42-个数为0.5 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】运用已学知识完成下列计算:
(1)17gNH3共有___mol原子,0.1molH2S共有___个氢原子;同质量的NH3和H2S中分子个数比为___。
(2)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则该气体的物质的量为___mol,该气体所含原子总数为___个,在标准状况下该气体的体积为____L,若该气体不与水反应,将其溶于1L水(密度为1g·cm-3)中,所得溶液中溶质的质量分数为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示实验室某浓盐酸试剂瓶上的标签,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸的物质的量浓度为___mol·L-1。
(2)取用任意体积的该浓盐酸时,下列物理量中不随所取体积的多少而变化的是__(填字母代号)。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400mol·L-1的稀盐酸。
①该学生需要量取__mL(保留一位小数)上述浓盐酸进行配制。如果实验室有5mL、10mL、20mL量筒,应选用__mL量筒最好。若量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将___(偏高、偏低、无影响)。
②配制时所需仪器除了量筒外,还需要的仪器有:___。
③下列情况会导致所配溶液的浓度偏低的是__(填字母代号)。
A.浓盐酸挥发,浓度不足 B.配制前容量瓶中有少量的水
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
查看答案和解析>>
科目: 来源: 题型:
【题目】现有CO和CO2的混合气体20克,其在标准状况下的体积为11.2L。据此回答下列问题:
(1)该混合气体总的物质的量为______,其平均摩尔质量为_______。
(2)混合气体中碳原子的个数为________。(用NA表示阿伏加德罗常数的值)
(3)若将该混合气体全部通过下图装置进行实验。

则:①气球中收集的气体是______,其质量为_______ 克
②从A瓶中获得沉淀质量的操作是_____、称量。
③若要证明A瓶溶液中的阳离子是否沉淀完全,其方法为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】将过量的氯气通入含Fe2+、I-、Br-的溶液,溶液中四种粒子的物质的量的变化如图所示。已知b=a+5,线段Ⅳ表示一种含氧酸,且线段I和Ⅳ表示的物质中含有相同的元素。下列说法错误的是

A. 线段I表示I-的变化情况
B. a点时消耗Cl2的体积为134.4 L
C. 原溶液中n(Fe2+):n(Br-) =2:3
D. 线段Ⅳ表明氧化性:C12>HIO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com