
科目: 来源: 题型:
【题目】用分液漏斗向锥形瓶中滴加液体至过量,下列对锥形瓶中现象的预测符合实际情况的是
选项 | 锥形瓶 | 分液漏斗 | 预测现象 |
A | 酸性KMnO4溶液 | H2O2溶液 | 溶液紫红色逐渐褪去且产生大量气泡 |
B | Na2S溶液 | 久置氯水 | 生成淡黄色沉淀 |
C | Fe(OH)3胶体 | 盐酸 | 产生红褐色沉淀 |
D | Na2CO3溶液 | H2BO3溶液 | 产生大量气泡 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯在催化剂的作用下可发生氧化反应,其反应机理为:PdCl2+C2H4+H2O![]() Pd+2HCl+CH3CHO,Pd+2CuCl2 PdCl2+2CuCl,4CuCl+4HCl+O2 4CuCl2+2H2O,下列说法错误的是
Pd+2HCl+CH3CHO,Pd+2CuCl2 PdCl2+2CuCl,4CuCl+4HCl+O2 4CuCl2+2H2O,下列说法错误的是
A. 催化剂加快反应速率的原理是通过改变反应路径降低了活化能
B. 该催化氧化反应的总方程式是2C2H4+O2![]() 2CH3CHO
2CH3CHO
C. 该催化氧化过程可在无水条件下进行
D. CuCl2和PdCl2的混合溶液可作为该反应的催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验兴趣小组利用易拉罐(主要成分是Al、Fe)制备明矾的过程如下图所示:

⑴ 写出“反应Ⅰ”时的离子反应方程式:________。
⑵ 写出“反应Ⅱ”时的化学反应方程式:________。
⑶ 过滤所得Al(OH)3需进行洗涤,检验Al(OH)3已洗涤干净的方法是:________。
⑷ 明矾能够净水的原因是________。
⑸ Fe和水蒸气在高温下反应后所得固体产物X可用于制取FeCl2溶液。请从下列试剂中选择合适的将X转化为FeCl2溶液。试剂:盐酸、NaCl溶液、Cu粉、Fe粉。依次选用的试剂为:________、________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某种自热食品的自热包上标注的成分是铝粉、生石灰、小苏打,自热包打开后加水即可大量放热。加水过程中发生的主要反应不可能是
A. 2Al+Ca(OH)2+2H2O=Ca(AlO2)2+3H2↑
B. Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O
C. 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
D. CaO+H2O=Ca(OH)2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g)ΔH=-283.0kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
则下列说法正确的是( )

A. H2的燃烧热为241.8kJ·mol-1
B. 由反应①、②可知上图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)ΔH=-41.2 kJ·mol-1
C. H2(g)转变成H2O(g)的化学反应一定要放出能量
D. 根据②推知反应H2(g)+1/2O2(g)=H2O(l)ΔH>-241.8 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】目前世界上海水淡化的主要方法有蒸馏法、电渗析法、反渗透法等。电渗析法是在直流电源作用下通过离子交换膜对海水进行处理(原理如图所示);反渗透法是利用压强差使海水一侧的水分子通过渗透膜进入淡水一侧,从而得到淡水和浓缩的盐溶液(原理如图所示)。下列说法正确的是
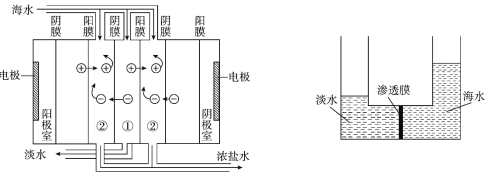
A. 蒸馏法、电渗析法、反渗透法均不发生化学反应
B. 反渗透法所用渗透膜的微孔直径范围是1~100nm
C. 蒸馏法具有设备简单、成本低等优点
D. 浓缩的盐溶液可用于提取或制备食盐、镁、溴等物质
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸锂广泛应用于陶瓷和医药等领域,在水中的溶解度比较小。以锂辉石(主要成分为Li2O,含有少量SiO2、Al2O3、Fe2O3)为原料制备Li2CO3的流程如下:
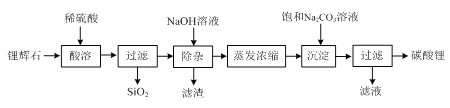
⑴ 写出“酸溶”时Li2O发生反应的离子方程式:________。
⑵ “除杂”时所用NaOH溶液不能过量,原因是________。
⑶ “除杂”时检验铁元素已完全除去的方法是________。
⑷ 写出“沉淀”时反应的化学方程式:________。
⑸ 检验最终所得碳酸锂样品中是否含有Na2CO3的方法是:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃组成的混合物共0.1 mol,完全燃烧得0.16 mol二氧化碳和3.6 g水。下列说法正确的是( )
A. 一定有甲烷 B. 一定是甲烷和乙烯 C. 可能有乙烷 D. 一定有乙炔
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量的工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。 乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体。由此他提出必须先除去杂质,再与溴水反应。请回答下列问题:
(1)写出甲同学实验中两个主要的化学方程式: ___________、_______。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙炔与溴发生加成反应,其理由是________。
a.使溴水褪色的反应,未必是加成反应
b.使溴水褪色的反应,就是加成反应
c.使溴水褪色的物质,未必是乙炔
d.使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体与溴水反应的化学方程式是__________,在验证过程中必须全部除去。
(4)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性。理由是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com