
科目: 来源: 题型:
【题目】研究燃煤烟气的脱硫(除SO2)和脱硝(除NOx)具有重要意义,请回答下列问题。
(1)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx,获得(NH4)2SO4的稀溶液。已知常温下,该溶液的pH=5,则![]() =_________(该温度下NH3· H2O的Kb=1.7×10-5)。往(NH4)2SO4溶液中再加入少量(NH4)2SO4固体,
=_________(该温度下NH3· H2O的Kb=1.7×10-5)。往(NH4)2SO4溶液中再加入少量(NH4)2SO4固体,![]() 的值将________(填“变大”、“不变”或“变小”)。
的值将________(填“变大”、“不变”或“变小”)。
(2)用乙烯作为还原剂将氮的氧化物还原为N2的脱硝技术,其脱硝机理示意图如下图1,脱硝率与温度,负载率(分子筛中催化剂的质量分数)的关系如图2所示。
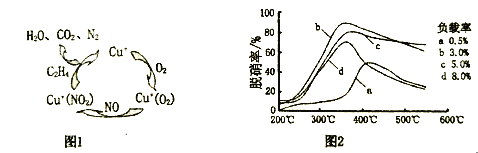
①写出该脱硝过程中乙烯和NO2反应的化学方程式:___________________。
②要达到最佳脱硝效果,应采取的条件是:___________________。
(3)利用如图装置可实现用Na2SO4溶液吸收SO2,再用离子膜电解法电解吸收液得到单质硫。
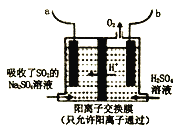
①a端应连接电源的_____(填“正极”或“负极”)。
②用Na2SO4溶液代替水吸收烟气中的SO2使之转化为H2SO3,其目的是_______________。
③电解过程中,阴极的电极反应式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA代表阿伏加德罗常数,以下说法正确的是
A. 标准状况下,11.2LH2O含H2O分子0.5NA
B. 1molFe与1molCl2充分反应转移电子3NA
C. 常温常压下,32g O2与O3的混合气中含氧原子2NA
D. 将0.1molFeCl3滴入沸水所形成胶体中含有氢氧化铁胶体粒子数目为 0.1 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某中学化学兴趣小组,将一包白色粉末(NaHCO3和Na2CO3的混合物)进行定量分析。现称取一份质量为27.4 g的样品,将此样品加热灼烧至质量不再变化,取出剩余物质,冷却后称重,质量为21.2g。
(1)写出加热时发生反应的化学方程式:___。
(2)分别求出该样品中NaHCO3和Na2CO3的物质的量。____、____(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的化学方程式。
①碳酸钙高温分解反应:____。
②有氢氧化铜和硫酸钡生成的复分解反应:____。
③铁粉与硫酸铜发生的置换反应:____。
④有水生成的化合反应:____。
以上四个反应中,属于氧化还原反应的是___(填标号)。请写出一个既属于氧化还原反应又属于分解反应且有水生成的反应的化学方程式:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. Ba(HCO3)2溶液与少量的NaOH溶液反应:Ba2++HCO![]() +OH-=BaCO3↓+H2O
+OH-=BaCO3↓+H2O
B. 次氯酸钙溶液中通入过量的二氧化碳 Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
C. 用氨水吸收少量二氧化硫 OH-+SO2=HSO3-
D. 硫酸与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
查看答案和解析>>
科目: 来源: 题型:
【题目】现有m g某气体,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体在标况下的密度为__________g/L。
(3)该气体在标准状况下的体积为____________L。
(4)该气体溶于0.1L水中(水的密度:1g·mL-1,且不考虑反应),其溶液中溶质的质量分数为_____。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)等质量的O2和O3所含分子个数比为___,原子个数比为___。
(2)400mL2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为___,从中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中SO42-的物质的量浓度为___。
(3)0.5 molCH4的质量为___;标准状况下,4.48LNH3所含分子数为___。
(4)等物质的量的CH4和N2,所含原子数之比为___,等质量的CH4和N2物质的量之比为___。
(5)3.5molBa(OH)2中含有___个OH-,2.5molNaOH的摩尔质量为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题.

(1)该浓盐酸中HCl的物质的量浓度为 ______ molL-1.
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______ .
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl-的数目
D.溶液的密度
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次并在操作步骤空白处填上适当仪器名称) ______ .
A.用30mL水洗涤 ______ 2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用 ______ 加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括 号内填“偏大”,“偏小”,或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面 ______
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水 ______ .
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计的微型实验装置验证SO2的性质,通过分析实验,下列结论表达正确的是

A. a棉球褪色,验证SO2具有氧化性
B. b棉球褪色,验证SO2具有酸性氧化物的通性
C. c棉球蓝色褪去,验证SO2漂白性
D. 可以使用浓硫酸吸收尾气
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨是人类科学技术发展史上的一项重大突破,2018年是合成氨工业先驱哈伯(P·Haber)获得诺贝尔奖100周年
(1)合成氨反应是一个可逆反应:N2(g)+3H2(g)![]() 2NH3(g),已知298K时:ΔH=-92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据正反应的焓变和熵变分析,常温下合成氨反应____(填“能”或“不能”)自发进行。实验研究表明,在特定条件下,合成氨反应的速率与参加反应的物质的浓度的关系式如下,v=kc(N2)c1.5(H2)c-1(NH3),k为速率常数,请根据该关系式分析,如果想增大合成氨反应的速率,从浓度的角度可以采用的措施为________。根据合成氨反应的特点,请再说出一项能够提高合成氨反应速率的措施_________。
2NH3(g),已知298K时:ΔH=-92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据正反应的焓变和熵变分析,常温下合成氨反应____(填“能”或“不能”)自发进行。实验研究表明,在特定条件下,合成氨反应的速率与参加反应的物质的浓度的关系式如下,v=kc(N2)c1.5(H2)c-1(NH3),k为速率常数,请根据该关系式分析,如果想增大合成氨反应的速率,从浓度的角度可以采用的措施为________。根据合成氨反应的特点,请再说出一项能够提高合成氨反应速率的措施_________。
(2)研究表明,在Fe催化剂作用下合成氨的反应历程为(*表示吸附态):
化学吸附:N2(g)→2N*;H2(g)→2H*;
表面反应:N*+H*![]() NH*;NH*+H*
NH*;NH*+H*![]() NH2*;NH2*+H*
NH2*;NH2*+H*![]() NH3*
NH3*
脱 附:NH3*![]() NH3(g)
NH3(g)
其中,N2的吸附分解反应速率慢,解决了合成氨的整体反应速率。
实际生产中,合成氨常用工艺条件:Fe作催化剂,控制温度773K,压强3.0×107Pa,原料中N2和H2物质的量之比为1:2.8。请回答:
①分析说明原料中N2过量的理由____________。
②近年来,中国科学院大连化学物理研究所陈平研究团队经过近二十年的积累,先后在催化剂分解、催化氨合成、化学链合成氨等方面取得重要进展。关于合成氨工艺的下列理解,正确的是______。
A.人们对合成氨研究的重要目的之一是要实现氨的低温高效合成
B.控制温度(773K)远于室温,是为了保证尽可能高的平衡转化率和快的反应速率
C.陈平团队首次报道了具有优异低温活性的LiH-3d过渡金属这一复合催化剂体系,它可以大大提高反应的平衡转化率
D.N2的吸附分解反应活化能高,是合成氨反应条件苛刻的重要原因
E.陈平团队构建了一条基于可再生能源的化学链合成氨工艺流程,可以显著提高能效
(3)若N2和H2生成NH3的反应为:![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g),的标准平衡常数
NH3(g),的标准平衡常数 ,其中
,其中![]() 为标准大气压(1×105Pa),
为标准大气压(1×105Pa),![]() 、
、![]() 和
和![]() 为各组分的平衡分压,如P(NH3)=x(NH3) P,P为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。
为各组分的平衡分压,如P(NH3)=x(NH3) P,P为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。
①N2和H2起始物质的量之比为1:3,反应在恒定温度和标准压强下进行,NH3的平衡产率为![]() ,则
,则![]() _________(用含
_________(用含![]() 的最简式表示)
的最简式表示)
②根据合成氨反应的特点,标准平衡常数![]() 随温度T升高而逐渐______(填“增大”或“减小”)。
随温度T升高而逐渐______(填“增大”或“减小”)。
(4)希腊两位科学家曾经采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶体薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。钯电极A为______极(填“阴”或“阳”),该极上的电极反应式是___________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com