
科目: 来源: 题型:
【题目】高铁电池是一种新型可充电电池,高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A. 放电时每转移3mol电子,正极有1molK2FeO4被氧化
B. 充电时阳极反应为:Fe(OH)3+5OH-3e-=FeO42-+4H2O
C. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,水的电离达到平衡:H2O![]() H+ + OH-。下列叙述正确的是
H+ + OH-。下列叙述正确的是
A. 将水加热,平衡向正反应方向移动,Kw不变
B. 向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大
C. 向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH-)降低
D. 向水中加入少量CH3COONa固体,平衡向正反应方向移动,c(OH-)= c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 同等质量的氧气和臭氧中,电子数相同
C. 1 mol重水与1 mol水中,中子数比为2∶1
D. 1 mol乙烷和1 mol乙烯中,化学键数相同
查看答案和解析>>
科目: 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,其中NH3被氧化为常见的无毒物质。下列说法错误的是( )

A. 溶液中OH-向电极a移动
B. 电极b上发生还原反应
C. 负极的电极反应为2NH3-6e-+6OH-![]() N2+6H2O
N2+6H2O
D. 理论反应消耗的NH3与O2的物质的量之比为3:4
查看答案和解析>>
科目: 来源: 题型:
【题目】以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( )

A.该电池能够在高温下工作
B.电池的负极反应为:C6H12O6+6H2O-24e-6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体 L
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学利用如图所示实验装置进行铁与水蒸气反应的实验,并对反应后硬质试管中固体物质的组成进行了探究。
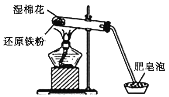
请回答下列问题:
(1)硬质试管中湿棉花的作用是________________。
(2)铁与水蒸气的反应中,氧化剂是________(填化学式,下同),还原剂是________。
(3)该同学对反应后硬质试管中固体物质的组成提出了如下假设:
假设1:只有Fe;
假设2:只有________;
假设3:既有Fe也有Fe3O4。
(4)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6 g,反应后固体物质的质量为6.6 g。从上述数据分析,反应后硬质试管中固体物质的组成为__________________。写出该反应的化学方程式________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,氧化剂与还原剂物质的量之比为1∶2的是( )
A. 3S+6NaOH===2Na2S+Na2SO3+3H2O
B. 2CH3COOH+Ca(ClO)2===2HClO+Ca(CH3COO)2
C. 4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
D. I2+2NaClO3===2NaIO3+Cl2
查看答案和解析>>
科目: 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
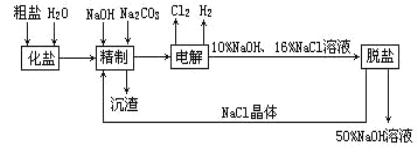
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生的电极反应式为_______;与电源负极相连的电极附近,溶液pH______(选填:不变、升高或下降)。
(2)如果粗盐中SO42-含量较高,必须加钡剂除去,该钡试剂可以是______
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为______、_______
(4)电解饱和食盐水的总反应化学方程式为_________
查看答案和解析>>
科目: 来源: 题型:
【题目】碘是人体不可缺乏的元素,为了防止碘缺乏,一般是在食盐中添加一定量的KIO3。但碘添加量也不能过多,过多会导致甲亢等。国家标准GB14880-1994中规定每千克食盐中碘的含量(以碘原子计)应为20-60mg/kg。实验研究小组为了检测某加碘盐中碘含量是否合格,查阅了有关的资料,发现其检测原理是:![]() (方程式未配平)。试根据相关信息回答下列问题:
(方程式未配平)。试根据相关信息回答下列问题:
(1)检测原理中,氧化剂为_______,氧化产物为_______。请在下面配平该方程式,同时用单线桥标明电子转移的方向和数目:_______
____![]() ____
____ ![]() ____
____![]() —____
—____![]() + ____
+ ____ ![]() +____
+____ ![]()
(2)取10g加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液(H2SO4和KI都稍过量),充分反应后,将反应液转入分液漏斗中,再加入一定量的CCl4,振荡,静置,此时观察到的现象是________________________________________________。然后分液,即得到I2的CCl4溶液。
(3)查阅资料,CCl4的沸点为78℃,I2的升华温度约为120~130℃。实验小组拟采用下图所示实验装置将CCl4和I2的混合溶液分离。该分离方法的名称是___________,冷凝管的进水口是_______(填“a”或“b”)。
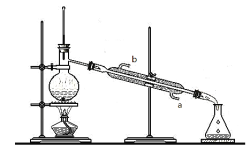
(4)上述实验结束,用电子天平称量出圆底烧瓶中I2的质量为1.5 mg,由此计算出该加碘盐中碘的含量为__________mg/kg,该加碘盐_______(填“合格”或“不合格”)。
(5)KIO3虽稳定性较好,但在高温下也可分解为KI等物质,所以在使用加碘盐时最佳的添加时间是菜肴快出锅时。请书写出KIO3在锅中长时间高温爆炒时可能发生的分解反应的化学方程式____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有四瓶失去标签的无色溶液,可能是CaCl2、AgNO3、HCl、Na2CO3中的其中一种,为了确定具体成分,随意将四瓶溶液标记为A、B、C、D后,进行了下列四组实验。
实验顺序 | 实验内容 | 实验现象 |
① | A+B | 无明显现象 |
② | B+D | 有气体放出 |
③ | B+C | 有沉淀生成 |
④ | A+D | 有沉淀生成 |
根据表中实验现象回答下列问题:
(1)A、B、C、D分别对应的溶质化学式为____________、___________、___________、___________;
(2)请分别写出上述实验②和③的离子方程式:
②________________________________________________________;
③________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com