
科目: 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子形式存在(Cl2可与碘离子反应生成碘单质)。实验室从海藻中提取碘的流程如下:
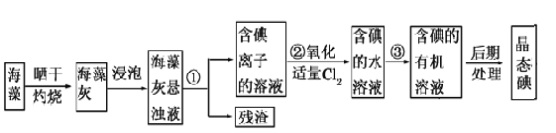
(1)指出提取碘的过程中有关实验操作的名称:③______;
(2)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有漏斗、烧杯、玻璃棒、 集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持装置、物品,尚缺少的玻璃仪器是_______。
(3)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出图中所示的实验装置中的错误之处:
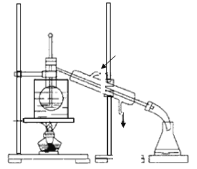
①______,
②______,
③______。
查看答案和解析>>
科目: 来源: 题型:
【题目】图甲是一种利用微生物将废水中的尿素CO(NH2)2]转化为环境友好物质的原电也装置示意图,利用该电池在图乙装置中的铁上镀铜。下列说法正确的是
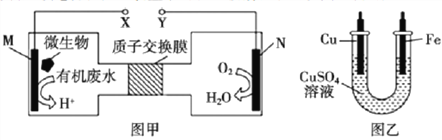
A. 图乙中Fe电极应与图甲中Y相连接
B. 图甲中H+透过质子交护膜由右向左移动
C. 图甲中M电极反应式:CO(NH2)2+5H2O-14e=CO2+2NO2+14H+
D. 当图甲中M电极消耗0.5mol尿素时,图乙中铁电极增重96g
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求写出反应的化学方程式:
(1)由2-溴丙烷转化为丙烯________________;
(2)由1-溴丁烷和必要的无机试剂制取1,2-二溴丁烷_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】18.0 mol·L-1的浓硫酸稀释成2.00 mol·L-1的稀硫 酸100 ml,实验操作如下:
(1)计算并用量筒量取 ml的18.0 mol·L-1的浓硫酸;
(2)将 沿烧杯内壁慢慢注入盛有少量 的烧杯中;
(3)将已冷却至室温的硫酸溶液沿玻璃棒注入 ___________;
(4)用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中;
(5)继续向容量瓶中加蒸馏水,直到液面接近刻度线1~2cm处,改用胶头滴管逐滴加蒸馏水,至液面与刻度线相切
(6)盖好容量瓶塞,反复颠倒摇匀,将配好的稀硫酸倒入试剂瓶中,贴好标签保存。
试分析下列操作对实验结果的影响(偏高、偏低或无影响)
①没有洗涤烧杯和玻璃棒
②定容时俯视读数
③容量瓶使用前有少许水残留
查看答案和解析>>
科目: 来源: 题型:
【题目】(14分)溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
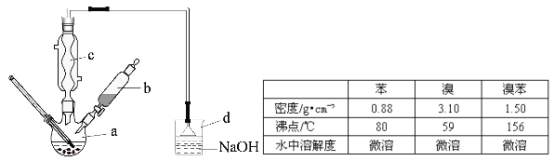
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是 ③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须的是 (填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是 (填入正确选项前的字母)。
A.25mL B. 50mL C.250mL D.500mL
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解槽装置如图所示,用Cu-Si合金作硅源,在950℃利用三层液熔盐进行电解精炼,有关说法正确的是

A.电子由液态Cu-Si合金流出,流入液态铝电极
B.液态铝电极与正极相连,作为电解池的阳极
C.在该液相熔体中Cu优先于Si被氧化,Si4+优先于Cu2+被还原
D.三层液熔盐的作用是使电子能够在三层间自由流动
查看答案和解析>>
科目: 来源: 题型:
【题目】“立方烷”是新合成的一种烃,其分子呈正方体结构。该分子的碳架结构如下图所示,其中每个顶点表示一个碳原子,棱表示碳碳单键,氢原子未画出。
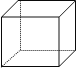
(1)“立方烷”的分子式为___________;
(2)其一氯代物共有_______种;
(3)其二氯代物共有_______种。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是_____,X的相对原子质量是_____。
(2)将30mL0.5mol/L的NaOH溶液加水稀释到500mL,稀释后NaOH的物质的量浓度为_____。
(3)VL硫酸铁溶液中含有mgFe3+离子,则溶液中SO42-离子的物质的量浓度是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】Bodensteins研究反应H2(g)+I2(g)![]() 2HI(g) △H<0 ,温度为T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如下表:
2HI(g) △H<0 ,温度为T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如下表:
容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
Ⅰ | 0.5molI2、0.5molH2 | w(HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
Ⅱ | xmolHI | w(HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
研究发现上述反应中:v正=kaw(H2)w(I2),v逆=kbw2(HI),其中ka、kb为常数。下列说法不正确的是( )
A. 温度为T时,该反应![]() =64
=64
B. 容器I中在前20min的平均速率v(HI)=0.025molL-1min-1
C. 若起始时,向容器I中加入物质的量均为0.1mol的H2、I2、HI,反应逆向进行
D. 无论x为何值,两容器中达平衡时w(HI)%均相同
查看答案和解析>>
科目: 来源: 题型:
【题目】将117 g NaCl溶于水配制成1 L溶液。
(1)该溶液中NaCl的物质的量浓度为________,溶液中Cl-的物质的量浓度为________。
(2)配制1 mol·L-1的NaCl溶液500 mL,需该溶液的体积为________。
(3)向该溶液中再通入一定量的HCl气体后,溶液中Cl-的物质的量浓度为3 mol·L-1(假设溶液体积不变),则溶液中H+的物质的量浓度为________,通入HCl气体的体积(标准状况下)为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com