
科目: 来源: 题型:
【题目】铜锌原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )

A. 锌电极上发生的反应:Zn2++2e-===Zn
B. 电池工作一段时间后,甲池的c(SO![]() )减小
)减小
C. 电流由锌电极经电流表流向铜电极
D. 电池工作一段时间后,乙池溶液的总质量增加
查看答案和解析>>
科目: 来源: 题型:
【题目】赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:2Cu2O+Cu2S![]() 6Cu+SO2↑,对于该反应,下列说法正确的是
6Cu+SO2↑,对于该反应,下列说法正确的是
A. 该反应的氧化剂只有Cu2O B. Cu既是氧化产物,又是还原产物
C. Cu2S既是氧化剂又是还原剂 D. 还原产物与氧化产物的物质的量之比为1∶6
查看答案和解析>>
科目: 来源: 题型:
【题目】碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法不正确的是

A. 可用KI淀粉试纸和食醋检验加碘盐中是否含有碘
B. 足量Cl2能使湿润的KI淀粉试纸变白的原因可能是5Cl2+I2+6H2O==2HIO3+10HCl
C. 由图可知氧化性的强弱顺序为Cl2>I2>IO3-
D. 途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为_______、_________、___________
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有_________、________,将该化合物溶于水,得到常温下pH=a的溶液,此时水电离的c(H+)=________
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是______。此化合物在酸性条件下与高锰酸钾反应的离子方程式为______,此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为:_______
(4)有一瓶固体药品的标签被损坏了,残留部分如图,已知该固体溶于水呈碱性,请推测该固体的化学式可能是(写3种)______
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL,下列叙述不正确的是( )

A.某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。则烧杯的实际质量为27.4 g
B.要完成本实验该同学应称出10.0g NaOH
C.氢氧化钠固体溶解后必须恢复至室温再进行转移
D.容量瓶使用前需洗涤、并保持干燥
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两同学研究Na2SO3溶液与FeCl3溶液反应的情况。

(1)常温下,FeCl3溶液的pH____7(填“<”、“>”或“=”)。
(2)分析红褐色产生的原因。
①甲同学认为步骤Ⅰ中溶液呈红褐色是因为生成了Fe(OH)3,用化学平衡移动原理解释溶液呈红褐色的原因______________
②乙同学认为可能是发生了氧化还原反应,完成并配平其反应的离子方程式:__________
![]() Fe3++
Fe3++![]() SO
SO![]() +
+![]() ________——
________——![]() Fe2++
Fe2++![]() ________+
________+![]() ________
________
乙同学查阅资料得知:
ⅰ.Fe2+与![]() 反应生成墨绿色的絮状沉淀FeSO3
反应生成墨绿色的絮状沉淀FeSO3
ⅱ.墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色
(3)甲同学为了确认溶液呈红褐色的原因是生成了Fe(OH)3,设计并完成了如下实验:

甲同学因此得出结论:溶液呈红褐色是因为生成了Fe(OH)3。而乙同学认为甲同学得出结论的证据仍然不足,乙同学的理由是____。
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:

①经检验步骤Ⅲ中红褐色溶液含有Fe2+,检验Fe2+选用的试剂是________(填字母)。
a.K3[Fe(CN)6]溶液 b.KSCN溶液 c.KMnO4溶液
②已知H2SO3是弱酸,请结合电离方程式说明步骤Ⅲ中出现红褐色的原因:_____________
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关溶液中粒子浓度的关系式中,正确的是
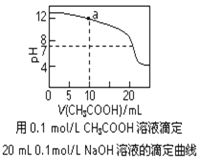
A. pH相同的①CH3COONa、②NaHCO3、③Na2CO3三份溶液中的c(Na+):③>②>①
B. 0.1mol·L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C. 图中pH=7时:c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
D. 图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是向MgCl2、AlCl3混合溶液中,开始滴加7mL试剂A,之后改滴试剂B,所得沉淀y(mol)与试剂体积V(mL)间的关系.以下结论不正确的是( )

A. A是NaOH,B是盐酸,且c(NaOH)︰c(HCl)=2︰1
B. 原混合液中,c(Al3+)︰c(Mg2+)︰c(Cl-)=1︰1︰5
C. A是NaOH,B是盐酸,且c(NaOH)︰c(HCl)=1︰2
D. 从6到9,相应离子反应式H+ + OH-===H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.0.01molNH4+含有质子数为0.1NA
B.4.48 L N2与CO的混合物所含分子数为0.2NA
C.6.2 g白磷与红磷的混合物中所含磷原子数为0.2NA
D.10.0mL 12 mol·L-1浓盐酸与足量二氧化锰反应,转移电子数为0.06NA
查看答案和解析>>
科目: 来源: 题型:
【题目】如图某工厂用NO气体制取NH4NO3溶液,下列说法正确的是
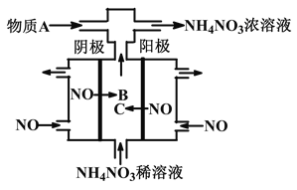
A. 阳极的电极反应式为:NO-3e-+2H2O=NO2-+4H+
B. 物质B与物质C是同一种物质
C. A物质可为氨气
D. 阴、阳两极转移的电子数之比为5∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com