
科目: 来源: 题型:
【题目】普洱茶具有独特的香气,是云南的旅游名片之一。橙花叔醇是影响其香气的物质之一,结构如图所示。下列说法正确的是
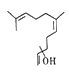
A. 该物质的化学式是C15H26O
B. 该物质不能使酸性高锰酸钾溶液褪色
C. 该物质的同分异构体可以是芳香族化合物
D. 该物质可以发生加成反应,不能发生消去反应
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)将30mL0.5mol/L的H2SO4溶液加水稀释到500mL后,从中取出50mL溶液的物质的量浓度为___。
(2)常温下,将20.0g14%的NaOH溶液跟30.0g24%的NaOH溶液混合,混合后得到1.2g/mL的混合液,试计算:
①混合后的溶液中NaOH的质量分数为___。
②混合后的溶液中NaOH的物质的量浓度为___mol/L。
③配制100mL同浓度溶液需要溶解___g的NaOH才能使其浓度与上述混合液浓度相等。
(3)在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,该混合气体中,CO和CO2的物质的量之比为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于电解质溶液的叙述中正确的是 ( )
A. pH=0的H2SO4溶液与1 mol·L-1 的Ba(OH)2溶液中水的电离程度相同
B. 0.2mol·L-1 CH3COOH溶液中的c(H+)是0.1mol·L-1 CH3COOH中的c(H+)的2倍
C. 室温时,pH=2的CH3COOH和0.01mol·L-1 NaOH溶液等体积混合,混合后pH=7
D. 等物质的量浓度的Na2S和NaHS的混合溶液中:2c(Na+)=3[c(S2-)+c(HS-)+c(H2S)]
查看答案和解析>>
科目: 来源: 题型:
【题目】用NaOH固体配制500mL1.0mol/L的NaOH溶液,操作步骤如下:
①把称好的NaOH固体放入小烧杯中,加适量蒸馏水溶解,冷却至室温;
②把①所得溶液小心转入容量瓶中;
③继续向容量瓶中加蒸馏水至液面距刻度线1cm~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶;
⑤将容量瓶瓶塞塞紧,充分摇匀;
⑥计算、称量NaOH固体的质量。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)⑥→①→②→___→___→⑤;
(2)所需仪器除托盘天平、药匙、烧杯、玻璃棒、胶头滴管外,还需用到的仪器有___;实验所需称量的NaOH固体为___g。
(3)试分析下列操作对所配溶液的浓度有何影响。(填“偏高”“偏低”或“无影响”)
①为加速固体溶解,可稍微加热并不断搅拌,在未降至室温时,立即将溶液转移至容量瓶定容。对所配溶液浓度的影响:___;
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响:___;
③定容时俯视液面。对所配溶液浓度的影响:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应属于氧化还原反应的是( )
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】氮氧化铝(AlON)具有多晶陶瓷在材料制备方面的优势,有着广阔的应用前景。工业上利用某铝土矿(含Al2O3及少量的MgO等杂质)生产氮氧化铝的流程如图所示。回答下列问题:
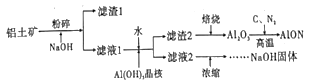
(1)为提高铝土矿碱浸的速率,除粉碎外,还可以采取的措施是_____(写出一项即可)
(2)滤液1的溶质有NaOH、_____。滤渣2的成分是_____。向滤液1中加水的目的是_______。该过程也可用通入足量的_____气体的方法来代替。
(3)滤液2浓缩的过程中常会吸收空气中的CO2,为得到纯净的NaOH,需要加入适量____(填化学式)。整个流程中,可循环的物质是_____。
(4)写出制备AlON的化学方程式_______。
(5)取1吨Al2O3质量分数为91.8%的铝土矿样品,利用上述流程AlON,最终制得氮氧化铝820.8kg,则氮氧化铝的产率为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解,在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
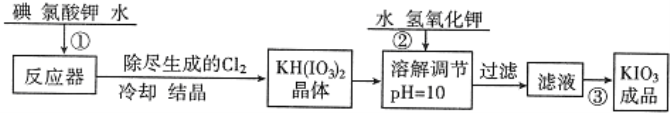
(1)已知步骤①反应器中发生的反应中,单质碘和氯酸钾的物质的量之比为6:11,反应器中发生的化学方程式为6I2+11KClO3+3H2O→6KH(IO3)2+5KCl+3Cl2↑。参照碘酸钾的溶解度:
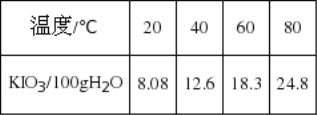
操作③得到碘酸钾晶体,方法是____________、____________:
(2)已知: KIO3+ 5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32—=2I—+S4O62—
检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应。用四氯化碳检验碘单质时,看到的明显现象有____________
(3)检验加碘食盐中碘的含量,学生乙设计的实验步骤如下:
①准确称取wg食盐,加适量蒸馏水使其完全溶解;
②用稀硫酸酸化所得食盐溶液,加入过量KI溶液充分混合;
③以淀粉为指示剂,逐滴加入2.0╳10—3mol/L的Na2S2O310.0mL,恰好反应完全。
则加碘食盐样品中的碘元素含量是_____ mg/kg (以含w 的代数式表示)。
(4)学生丙又对纯净的NaCl进行了下列实验:

请推测实验中产生蓝色现象的可能原因____________,用化学方程式表示。
(5)根据学生丙的实验结果,学生乙测得的食盐中碘元素的含量可能____________ (填“偏高”、“偏低"或“准确")。原因是____________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列方程式书写正确的是 ( )
A. HCO3的电离方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. 泡沫灭火器的原理:Al3++3HCO3- ![]() Al(OH)3↓+3CO2↑
Al(OH)3↓+3CO2↑
C. AgCl电离方程式:AgCl(s)![]() Ag+ (aq)+ Cl-(aq)
Ag+ (aq)+ Cl-(aq)
D. Na2S显碱性原因:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com