
科目: 来源: 题型:
【题目】取10g粗铁加入足量稀硫酸中,共收集到5.6L氢气(标准状况),则粗铁中混有的杂质不可能是( )
A. Cu和Mg B. Mg和Al C. Al 和 Si D. SiO2和Zn
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年3月8日,联合国妇女署在推特上发布了一张中国女科学家屠呦呦的照片。致敬她从传统中医药中找到了治疗疟疾的药物----青蒿素。
已知:青蒿素是烃的含氧衍生物,为无色针状晶体。乙醚沸点为35℃。
(1)我国提取中草药有效成分的常用溶剂有:水;或亲水性溶剂(如乙醇,与水互溶);或亲脂性溶剂(如乙醚,与水不互溶)。诺贝尔奖获得者屠呦呦及其团队在提取青蒿素治疗疟疾过程中,记录如下:“青蒿素的水煎剂无效;乙醇提取物的效用为30%~40%;乙醚提取物的效用为95%”。下列推测不合理的是_____;
A | 青蒿素在水中的溶解度很大 | B | 青蒿素含有亲脂的官能团 |
C | 在低温下提取青蒿素,效果会更好 | D | 乙二醇提取青蒿素的能力强于乙醚 |
(2)用下列实验装置测定青蒿素实验式的方法如下:
将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。

①装置D的作用是______,装置E中吸收的物质是______,装置F中盛放的物质是______。
②实验装置可能会产生误差,造成测定含氧量偏低,改进方法是______。
③合理改进后的装置进行实验,称得:
装置 | 实验前/g | 实验后/g |
E | 22.6 | 42.4 |
F | 80.2 | 146.2 |
则测得青蒿素的实验式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
(1)有机物A样品3.0g,对其进行如下操作:充分燃烧得3.36 L CO2(标准状况)和3.6 g H2O;质谱分析得A的相对分子质量为60,A的分子式为____________。A在催化剂Cu的作用下能被氧气氧化成C,C不能发生银镜反应,则A的名称是____________,C中官能团名称为____________。
(2)![]() 的同分异构体中,既能发生银镜反应,又能与FeCl3溶液发生显色反应的共有________种,其中核磁共振氢谱为5组峰,且峰面积比为2∶2∶2∶1∶1的为_____________ (写结构简式)。
的同分异构体中,既能发生银镜反应,又能与FeCl3溶液发生显色反应的共有________种,其中核磁共振氢谱为5组峰,且峰面积比为2∶2∶2∶1∶1的为_____________ (写结构简式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在Al2(SO4)3和MgSO4的混合液中滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原溶液中Al2(SO4)3和MgSO4的物质的量之比为
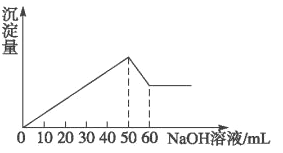
A. 1 :2B. 3 : 1C. 3 : 2D. 2 : 1
查看答案和解析>>
科目: 来源: 题型:
【题目】为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化剂作用下,通过下列反应:CCl4+H2 ![]() CHCl3+HCl使CCl4转化为重要的化工原料氯仿(CHCl3)。此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4 等。已知CCl4的沸点为77 ℃,CHCl3的沸点为61.2 ℃。
CHCl3+HCl使CCl4转化为重要的化工原料氯仿(CHCl3)。此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4 等。已知CCl4的沸点为77 ℃,CHCl3的沸点为61.2 ℃。
(1)在密闭容器中,该反应达到平衡状态后,测得如下数据(假设不考虑副反应)。
实验 序号 | 温度/℃ | 初始CCl4的浓度 (mol·L-1) | 初始H2的浓度 (mol·L-1) | CCl4的平衡转化率 |
1 | 110 | 0.8 | 1.2 | A |
2 | 110 | 1 | 1 | 50% |
3 | 100 | 1 | 1 | B |
①此反应的化学平衡常数表达式为_____________。
②实验1中,CCl4的转化率A________50%(填“大于”“小于”或“等于”)。
③实验2中,10 h后达到平衡,H2的平均反应速率为________________。
④实验3中,B的值________(填序号)。
A 等于50% B 大于50% C 小于50% D 从本题资料无法判断
(2)120 ℃时,在相同条件的密闭容器中,分别进行H2 的初始浓度为2 mol·L-1和4 mol·L-1的实验,测得反应消耗CCl4的百分率(x%)和生成物中CHCl3的百分含量(y%)随时间(t)的变化关系如图(图中实线是消耗CCl4的百分率变化曲线,虚线是产物中CHCl3的百分含量变化曲线)。
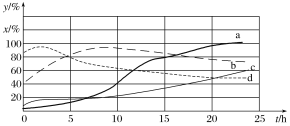
①在图中的四条线中,表示H2的起始浓度为2 mol·L-1的实验消耗CCl4的百分率变化曲线的是________(填序号)。
②根据上图曲线,氢气的起始浓度为________ mol·L
查看答案和解析>>
科目: 来源: 题型:
【题目】下列选项中所示的物质转化过程中未涉及到氧化还原反应的是
A.Fe3O4![]() FeI2
FeI2![]() Fe(OH)2
Fe(OH)2
B.SiO2![]() Si
Si![]() SiCl4
SiCl4
C.NaCl![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
D.SO2![]() H2SO4
H2SO4![]() Na2SO4
Na2SO4
查看答案和解析>>
科目: 来源: 题型:
【题目】镇咳药沐舒坦可由化合物甲和化合物乙在一定条件下制得:
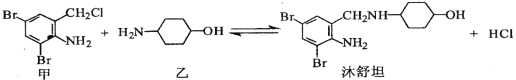
下列有关叙述正确的是( )
A. 甲的分子式为C7H4NBr2Cl
B. 沐舒坦分子中最多有13个碳原子共平面
C. 乙遇FeCl3溶液显紫色
D. 反应过程中加入适量K2CO3可提高沐舒坦的产率
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的有机物充分燃烧后的产物通入足量的石灰水中完全吸收,经过滤得沉淀20g ,滤液质量比原石灰水减少5.8g,该有机物不可能是( )
A. 乙烯B. 乙醇C. 乙烷D. 乙二醇
查看答案和解析>>
科目: 来源: 题型:
【题目】图甲表示叶绿体的结构,图乙表示暗反应过程。请据图回答下列问题:

(l)叶绿体中的色素分布于图甲中的____ (填序号);四种色素能在滤纸条上分离,是因为____。
(2)叶绿体进行光合作用时,ATP的移动方向是从____到____(填序号),合成ATP所需的能量来自____。
(3)在光照强度、温度和CO2浓度三种环境因素中,能直接影响图乙所示过程的是 _________。若突然降低光照强度,则在短时间内叶绿体中C3和C5的含量变化分别是 _________、________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:

(1)将标准状况下___L氯化氢气体通入1.00L水中可得36.5%的浓盐酸,该浓盐酸中HCl的物质的量浓度为___mol·L-1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是_____。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取___mL上述浓盐酸进行配制。
②配制仪器除烧杯、量筒和玻璃棒,还需要的仪器是___、____。
③配制时,下列操作正确的顺序是(用字母表示)____。
A.洗涤 B.定容 C.溶解 D.摇匀 E.冷却 F.称量 G.转移
④在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填“偏大”、“偏小”或“无影响”)。
Ⅰ.未等稀释后的溶液冷却到室温就转移到容量瓶(______)
Ⅱ.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水。(______)
Ⅲ.配制时,容量瓶有少量蒸馏水(______)
Ⅳ.定容时仰视刻度线。(_______)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com