
科目: 来源: 题型:
【题目】下列有关反应的离子方程式正确的是( )
A.氯气溶于水:Cl2+H2O=H++Cl-+HClO
B.Fe跟稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
C.将浓盐酸与MnO2混合加热:MnO2+2H++2Cl-![]() Mn2++Cl2↑+H2O
Mn2++Cl2↑+H2O
D.过氧化钠投入水中:Na2O2+2H2O=O2↑+2OH-+2Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】已知饱和氯化铵溶液与亚硝酸钠晶体混合加热可制备氮气。利用如下装置制取氮气,并用氮气制备Ca3N2,Ca3N2遇水发生水解反应。下列说法错误的是
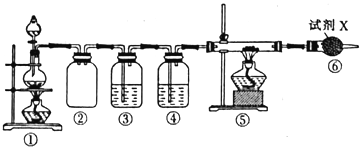
A. ①中发生的化学反应为NaNO2+NH4Cl![]() NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
B. ④、⑥中依次盛装的试剂可以是浓H2SO4、碱石灰
C. ③中盛放的试剂是NaOH 溶液
D. 实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊试纸变蓝
查看答案和解析>>
科目: 来源: 题型:
【题目】浓硫酸分别和三种钠盐反应,下列分析正确的是

A. 对比①和②可以说明还原性Br->Cl-
B. ①和③相比可说明氧化性Br2>SO2
C. ②中试管口白雾是HCl遇水蒸气所致,说明酸性H2SO4>HCl
D. ③中浓H2SO4被还原成SO2
查看答案和解析>>
科目: 来源: 题型:
【题目】Cl2O黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会发生燃烧并爆炸。种制取Cl2O 的装置如图所示。

已知:C12O的熔点为-116℃,沸点为3.8℃,Cl2 的沸点为-34.6℃;HgO+2Cl2=HgCl2 +Cl2O
下列说法不正确的是
A. 装置②、③中盛装的试剂依次是饱和食盐水和浓硫酸
B. 通入干燥空气的目的是将生成的Cl2O稀释减少爆炸危险
C. 从装置⑤中逸出气体的主要成分是Cl2O
D. 装置④与⑤之间不用橡皮管连接,是为了防止橡皮管燃烧和爆炸
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:
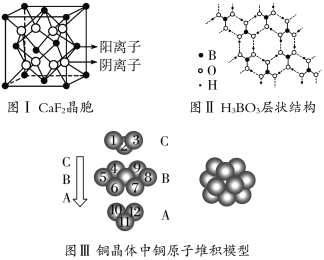
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为________。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________,H3BO3晶体中B原子个数与极性键个数比为________。
(3)三种晶体中熔点最低的是________,其晶体受热熔化时,克服的微粒之间的相互作用为________________________________________________________________。
(4)结合CaF2晶体的晶胞示意图,已知,两个距离最近的Ca2+核间距离为a×10-8 cm,计算CaF2晶体的密度为________g·cm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为Ca(ClO)2+4HCl(浓)===CaCl2+2Cl2↑+2H2O
(1)浓盐酸在反应中显示出来的性质是_____(填写字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为______mol。
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在新制饱和氯水中,若只改变某一条件,下列叙述正确的是
A. 再通入少量氯气,![]() 减小
减小
B. 通入少量SO2,溶液漂白性增强
C. 加入少量的碳酸钠粉末,pH增大,溶液漂白性减弱
D. 光照过程中,有气泡冒出,溶液的导电性增强
查看答案和解析>>
科目: 来源: 题型:
【题目】(一)Na、Cu、O、Si、S、Cl是常见的六种元素.
(1)Na位于元素周期表第__周期第__族;S的基态原子核外有__个未成对电子;
Si的基态原子核外电子排布式为__.
(2)用“>”或“<”填空:
第一电离能 | 离子半径 | 熔点 | 酸性 |
Si______S | O2-______Na+ | NaCl ______ Si | H2SO4 __________HClO4 |
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取.写出该反应的离子方程式,并标出电子转移的方向和数目___
(二).某元素的原子序数为33,请回答:
(1)该元素原子核外有_______个电子层,______个能级,______个原子轨道。
(2)它的最外层电子排布式为____________,它的电子排布式为________,轨道表示式为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.下列 A、B、C、D 是中学常见的混合物分离或提纯的基本装置。
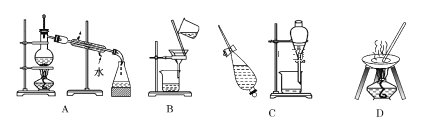
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将 A、B、C、D 填入适当的空格中。
(1)从碘水中提取碘____________________;
(2)分离酒精与水的混合物____________________;
(3)除去粗盐中的泥沙制精盐________________。
Ⅱ.实验室配制一定物质的量浓度溶液要用到量筒和图Ⅱ仪器等。配制某浓度的稀硫酸,用 10 mL 量筒量取浓硫酸的体积如图Ⅰ所示,
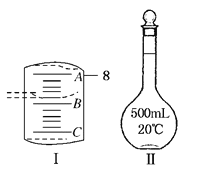
(1)A 与 B,B 与 C 刻度间相差 1mL,如果刻度 A 为8,量筒中浓硫酸的体积是________mL。
(2)要用 CuSO4·5H2O 晶体配制 480mL 0.1mol/L CuSO4 溶液,应该用托盘天平称取CuSO4·5H2O____
(3)图Ⅱ所示仪器的名称是_________仪器有下列情况,对配制溶液的浓度有何影响?(填“偏高”、 “偏低”或“无影响”)
A.仪器中有少量蒸馏水______________;
B.定容时加水超过刻度线______________;
C.最终定容时俯视观察液面____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化硅(SiO2)又称硅石,是制备硅及其化合物的重要原料(各种转化见图)。下列说法正确的是
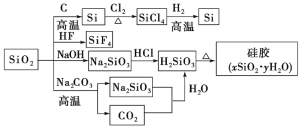
A. SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物
B. SiO2和Si都是光导纤维材料
C. 硅胶吸水后可重复再生
D. 图中所示转化反应都是非氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com